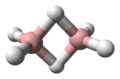Boranes - Boranes

Boranes er navnet på forbindelser med formlen B x H y og beslægtede anioner. Mange sådanne boraner er kendt. Mest almindelige er dem med 1 til 12 boratomer. Selvom de har få praktiske anvendelser, udviser boranerne strukturer og binding, der adskiller sig stærkt fra de mønstre, der ses i kulbrinter. Hybrider af boraner og kulbrinter, carboranerne er også veludviklede.
Historie
Udviklingen af boranens kemi førte til innovationer inden for syntetiske metoder samt struktur og binding. For det første var der brug for nye syntetiske teknikker til håndtering af diboran og mange af dets derivater, som er både pyroforiske og flygtige. Alfred Stock opfandt glasvakuumslangen til dette formål.
Diborans struktur blev korrekt forudsagt i 1943 mange år efter dens opdagelse. Strukturerne af borhydridklyngerne blev bestemt begyndende i 1948 med karakteriseringen af decaboran . William Lipscomb blev tildelt Nobelprisen i kemi i 1976 for denne og mange efterfølgende krystallografiske undersøgelser . Disse undersøgelser afslørede forekomsten af deltahedrale strukturer, det vil sige netværk af trekantede arrays af BH -centre.
Klyngernes binding indledte polyhedral skeletpar elektronteori og Wades regler, som kan bruges til at forudsige strukturer af boraner. Disse regler viste sig at beskrive strukturer af mange klyngeforbindelser.
Interessen for boraner steg under anden verdenskrig på grund af uranborhydridets potentiale for berigelse af uranisotoperne og som en kilde til brint til oppustning af vejrballoner. I USA udviklede et team ledet af Schlesinger den grundlæggende kemi for de anioniske borhydrider og de relaterede aluminiumhydrider. Schlesinger arbejde lagde grunden til en masse af borhydrid reagenser for organisk syntese , hvoraf de fleste blev udviklet af hans elev Herbert C. Brown . Boranbaserede reagenser bruges nu meget i organisk syntese. Brown blev tildelt Nobelprisen i kemi i 1979 for dette arbejde.
Kemisk formel og navngivningskonventioner
Boranklynger er klassificeret som følger, hvor n er antallet af boratomer i en enkelt klynge:
| Klyngetype | Kemisk formel | Eksempel | Noter |
|---|---|---|---|
| hypercloso - | B n H n | Ustabil; derivater kendes | |
| closo - | B n H n 2− | Cæsium dodecaborate | |
| nido - | B n H n+4 | pentaborane (9) | |
| arachno - | B n H n+6 | pentaborane (11) | |
| bindestreg - | B n H n+8 | Findes kun i addukter |
Den Internationale Union for ren og anvendt kemi regler for systematisk navngivning er baseret på et præfiks, der angiver en klasse af forbindelser, efterfulgt af antallet af boratomer og til sidst antallet af hydrogenatomer i parentes. Forskellige detaljer kan udelades, hvis der ikke er nogen tvetydighed om betydningen, for eksempel hvis kun en strukturel type er mulig. Nogle eksempler på konstruktionerne er vist nedenfor.
Borane
BH 3Diborane (6)
B 2 H 6arachno -Tetraborane (10)
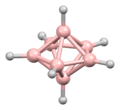
B 4 H 10Pentaborane (9)
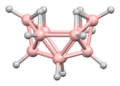
B 5 H 9Decaborane (14)
B 10 H 14
Udarbejde (12)
B 12 H 12 2−
Navngivningen af anioner illustreres af
- octahydridopentaborate, B 5 H 8 -
Hydrogentællingen angives først efterfulgt af boretallet. Endelsen -ate anvendes med anioner . Den ioniske ladningsværdi er inkluderet i den kemiske formel, men ikke som en del af det systematiske navn.
Binding i boraner
Boraner er ikke-klassisk bundne forbindelser, det vil sige, at der ikke er nok elektroner til at danne 2-center, 2-elektronbindinger mellem alle par tilstødende atomer i molekylet. En beskrivelse af bindingen i de større boraner blev formuleret af William Lipscomb . Det indebar:
- 3-center 2-elektron BHB-hydrogenbroer
- 3-center 2-elektron BBB-bindinger
- 2-center 2-elektronbindinger (i BB, BH og BH 2 )
Lipscombs metode er stort set blevet afløst af en molekylær orbital tilgang. Dette gør det muligt at udvide begrebet multi-center limning. For eksempel i den icosahedral ion [B 12 H 12 ] 2- er den totalt symmetriske (A g symmetri) molekylære orbital ligeligt fordelt mellem alle 12 boratomer. Wades regler giver en kraftfuld metode, der kan bruges til at rationalisere strukturerne med hensyn til antallet af atomer og forbindelsen mellem dem.
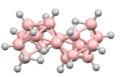
Multicluster boraner
Selvom det er relativt sjældent, er flere multi-cluster boraner blevet karakteriseret. For eksempel omsætning af en boran klynge med B 2 H 6 (som kilde for BH 3 ), kan føre til dannelsen af en conjuncto -borane arter, hos hvilke boran cluster underenheder samles ved deling af boronatomer.
- B 6 H 10 + (BH 3 ) → B 7 H 11 + H 2
- B 7 H 11 + B 6 H 10 → B 13 H 19 + H 2
Andre konjunktobboraner , hvor underenhederne er forbundet med en BB -binding , kan fremstilles ved ultraviolet bestråling af nido -boraner. Nogle BB -koblede konjunktoboraner kan fremstilles ved anvendelse af PtBr 2 som katalysator.
Analogt med Wades regler er elektrontællingsskema blevet udviklet til at forudsige eller rationalisere multicluster -boraner.
| Præfiks | Betyder | Eksempel |
|---|---|---|
| klado - | forgrenede klynger | |
| conjuncto - | sammenkoblede klynger | |
| megalo - | flere sammenkoblede klynger |
Boraners reaktivitet
Den laveste boran, BH 3 eksisterer kun forbigående, dimererer øjeblikkeligt for at danne diboran, B 2 H 6 . Dens addukter BH 3 -THF og BH 3 · DMSO er tilstrækkeligt stabile til anvendelse i hydroboreringsreaktioner reaktioner. Nogle minder om boraners reaktion på diborans adfærd, og reagerer meget eksotermt med luft, selv eksplosivt. Derimod mange Closo -borane klynge, såsom B 12 H 12 2- , ikke reagerer med luft.
Borhydridklyngerne er så forskellige, at generaliseringer af deres reaktioner ikke er mulige.
Lewis syre/base adfærd
nogle fungerer som elektrondonorer på grund af den relative grundlæggende karakter af BH -terminalgrupperne . Boraner kan fungere som ligander i koordineringsforbindelser . Hapticities af η 1 til η 6 er fundet, med elektrondonation, der involverer brodannelse af H -atomer eller donation fra BB -bindinger. For eksempel nido- B 6 H 10 kan erstatte ethen i Zeise salt for at fremstille Fe (η 2 -B 6 H 10 ) (CO) 4 .
De kan også fungere som Lewis -syrer med samtidig åbning af klyngen. Et eksempel på trimethylphosphin :
- B 5 H 9 + 2 PMe 3 → B 5 H 9 (PMe 3 ) 2
Bronsted syre/base adfærd
Nogle højere boraner, især dem med brodannende hydrogenatomer, kan deprotoneres med en stærk base. Et eksempel:
- B 5 H 9 + NaH → Na (B 5 H 8 ) + H 2
Surhed øges med størrelsen af boranen. B 10 H 14 har en pK -værdi på 2,7.
- B 5 H 9 <B 6 H 10 <B 10 H 14 <B 16 H 20 <B 18 H 22
Aufbau reaktioner
For borhydridkemikeren er en af de vigtigste reaktioner opbygningsprocessen, ved hvilken mindre borhydridklynger tilføjer boran for at give større klynger.
Hydroboration
Minder om adfærden hos diboran og dets addukter, højere boraner deltager i hydroborering. Når borhydrider tilføje en alkyn , bliver det carbonatom inkorporeret i klynge, der producerer carboraner , fx C 2 B 10 H 12 .
Ansøgninger
Diboran og dets monomere addukter boran -tetrahydrofuran eller boran -dimethylsulfid er nyttige reagenser. De bruges ofte til hydroborering i organisk syntese . De højere borhydridklynger har ikke givet mange eller nogen anvendelser. Nogle koboltderivater af carboraner er blevet kommercialiseret til sekvestering af 137 C fra radioaktivt affald .
Aspiration bruger
Fordi borhydridklynger let absorberer neutroner, er deres derivater ofte blevet undersøgt for anvendelser i Neutron capture -behandling af kræft . Et foretrukket forbindelse er Na 2 [B 12 H 11 (SH)]. Det gør brug af det faktum, at 10 B har et meget højt neutronfangstværsnit , så neutronbestråling er yderst selektiv for det område, hvor forbindelsen bor.
- 10 B + 1 n → ( 11 B*) → 4 He + 7 Li + γ (2,4 Mev)
Boraner har en høj specifik forbrændingsenergi sammenlignet med kulbrinter , hvilket gør dem potentielt attraktive som brændstoffer. Der blev udført intensiv forskning i 1950'erne om deres anvendelse som flybrændstofadditiver , men indsatsen førte ikke til praktiske resultater.
Se også
- Kategori: Boraner , der indeholder alle specifikke boranforbindelsesartikler