c -Fos - c-Fos
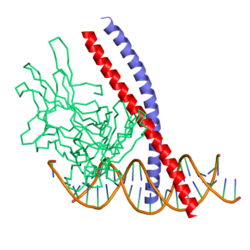
Inden for molekylærbiologi og genetik er c-Fos et proto-onkogen, der er den humane homolog for det retrovirale onkogene v-fos. Det blev først opdaget i rottefibroblaster som det transformerende gen for FBJ MSV (Finkel – Biskis - Jinkins murine osteogen sarkomvirus) (Curran og Tech, 1982). Det er en del af en større Fos-familie af transkriptionsfaktorer, som omfatter c-Fos, FosB , Fra-1 og Fra-2 . Det er blevet kortlagt til kromosomområde 14q21 → q31. c-Fos koder for et 62 kDa-protein, som danner heterodimer med c-jun (en del af Jun-familien af transkriptionsfaktorer), hvilket resulterer i dannelsen af AP-1 (Activator Protein-1) -kompleks, som binder DNA på AP-1-specifikke steder ved promotor- og forstærkerregionerne af målgener og konverterer ekstracellulære signaler til ændringer i genekspression. Det spiller en vigtig rolle i mange cellulære funktioner og har vist sig at være overudtrykt i en række kræftformer.
Struktur og funktion
c-Fos er et 380 aminosyreprotein med en basisk leucin-lynlåsregion til dimerisering og DNA-binding og et transaktiveringsdomæne ved C-terminal, og ligesom Jun-proteiner kan det danne homodimerer. In vitro- undersøgelser har vist, at Junod-Fos heterodimerer er mere stabile og har stærkere DNA-bindende aktivitet end juni-juni-homodimerer.
En række stimuli, herunder serum , vækstfaktorer , tumorpromotorer, cytokiner og UV -stråling fremkalder deres ekspression. C-fos mRNA og protein er generelt blandt de første, der skal udtrykkes og omtales derfor som et umiddelbart tidligt gen . Det induceres hurtigt og forbigående inden for 15 minutter efter stimulering. Dens aktivitet reguleres også af posttranslational modifikation forårsaget af phosphorylering af forskellige kinaser, som MAPK , CDC2, PKA eller PKC, som påvirker proteinstabilitet, DNA-bindingsaktivitet og transaktionsfaktorernes transaktiverende potentiale. Det kan forårsage genundertrykkelse såvel som genaktivering, selvom forskellige domæner menes at være involveret i begge processer.
Det er involveret i vigtige cellulære begivenheder, herunder celleproliferation, differentiering og overlevelse; gener forbundet med hypoxi ; og angiogenese ; hvilket gør dens dysregulering til en vigtig faktor for kræftudvikling. Det kan også forårsage tab af cellepolaritet og epitel-mesenkymal overgang , hvilket fører til invasiv og metastatisk vækst i brystepitelceller.
Betydningen af c-fos i biologisk kontekst er blevet bestemt ved at eliminere endogen funktion ved hjælp af anti-sense mRNA, anti-c-fos antistoffer, et ribozym, der spalter c-fos mRNA eller en dominerende negativ mutant af c-fos. De således genererede transgene mus er levedygtige, hvilket viser, at der er c-fos-afhængige og uafhængige veje til celleproliferation, men viser en række vævsspecifikke udviklingsdefekter, herunder osteoporose , forsinket gametogenese , lymfopeni og adfærdsmæssige abnormiteter.
Klinisk betydning
|
|
AP-1-komplekset har været impliceret i transformation og progression af kræft . Ved osteosarkom og endometriumkræft var c-Fos-overekspression forbundet med læsioner af høj kvalitet og dårlig prognose. I en sammenligning mellem precancerøs læsion af livmoderhalsen og invasiv livmoderhalskræft var c-Fos-ekspressionen signifikant lavere i precancerøse læsioner. c-Fos er også blevet identificeret som uafhængig forudsiger for nedsat overlevelse i brystkræft .
Det blev fundet, at overekspression af c-fos fra klasse I MHC-promotor i transgene mus fører til dannelse af osteosarkomer på grund af øget proliferation af osteoblaster, hvorimod ektopisk ekspression af de andre Jun- og Fos-proteiner ikke fremkalder nogen ondartede tumorer. Aktivering af c-Fos-transgenet i mus resulterer i overekspression af cyclin D1, A og E i osteoblaster og chondrocytter, både in vitro og in vivo , hvilket kan bidrage til den ukontrollerede vækst, der fører til tumor. Menneskelige osteosarkomer analyseret for c-fos-ekspression har givet positive resultater i mere end halvdelen af tilfældene, og c-fos-ekspression har været forbundet med højere tilbagefaldsfrekvens og dårlig respons på kemoterapi.
Flere undersøgelser har rejst tanken om, at c-Fos også kan have tumorundertrykkende aktivitet, som det kan være i stand til at fremme såvel som at undertrykke tumorigenese. Understøttende er observationen af, at tab af c-Fos-ekspression i ovariecarcinomer korrelerer med sygdomsprogression. Denne dobbeltaktion kan aktiveres af differentiel proteinsammensætning af tumorceller og deres miljø, for eksempel dimeriseringspartnere, co-aktivatorer og promotorarkitektur. Det er muligt, at den tumorundertrykkende aktivitet skyldes en proapoptotisk funktion. Den nøjagtige mekanisme, hvormed c-Fos bidrager til apoptose, er ikke klart forstået, men observationer i humane hepatocellulære carcinomceller indikerer, at c-Fos er en mediator for c-myc-induceret celledød og kan fremkalde apoptose gennem p38 MAP-kinasebanen. Fas-ligand (FASLG eller FasL) og tumornekrosefaktorrelateret apoptose-inducerende ligand (TNFSF10 eller TRAIL) kan afspejle en yderligere apoptotisk mekanisme induceret af c-Fos, som observeret i en human T-celle leukæmicellelinje. En anden mulig mekanisme for c-Fos-involvering i tumorsuppression kunne være den direkte regulering af BRCA1, en veletableret faktor i familiær bryst- og æggestokkræft.
Derudover er rollen som c-fos og andre Fos-familieproteiner også blevet undersøgt ved endometriecarcinom, livmoderhalskræft, mesotheliomer, kolorektal cancer, lungekræft, melanomer, thyreoideacancer, spiserørskræft, hepatocellulære carcinomer osv.
Kokain, metamfetamin, morfin og andre psykoaktive lægemidler har vist sig at øge c-Fos-produktionen i den mesokortiske vej (præfrontal cortex) såvel som i den mesolimbiske belønningsvej (nucleus accumbens), samt vise variation afhængig af tidligere sensibilisering. c-Fos-undertrykkelse af ΔFosB 's AP-1-kompleks inden for D1-typen medium spiny neuroner i nucleus accumbens fungerer som en molekylær switch, der muliggør kronisk induktion af ΔFosB, hvilket tillader det at akkumulere hurtigere. Som sådan finder c-Fos-promotoren udnyttelse i forskning i stofmisbrug generelt såvel som med kontekstinduceret tilbagefald til narkotikasøgning og andre adfærdsændringer forbundet med kronisk medicinoptagelse.
En stigning i c-Fos-produktion i androgenreceptorholdige neuroner er blevet observeret hos rotter efter parring.
Ansøgninger
Ekspression af c-fos er en indirekte markør for neuronal aktivitet, fordi c-fos ofte udtrykkes, når neuroner affyrer handlingspotentialer. Opregulering af c-fos mRNA i et neuron indikerer nylig aktivitet.
C-fos-promotoren er også blevet brugt til forskning i stofmisbrug. Forskere bruger denne promotor til at tænde transgener hos rotter, så de kan manipulere specifikke neuronale ensembler for at vurdere deres rolle i narkotikarelaterede minder og adfærd. Denne neuronale kontrol kan replikeres med optogenetik eller DREADD'er
Interaktioner
c-Fos har vist sig at interagere med:
- BCL3 ,
- COBRA1 ,
- CSNK2A1 ,
- CSNK2A2 ,
- DDIT3 ,
- JUN
- NCOA1 ;,
- NCOR2 ,
- RELA ,
- RUNX1 ,
- RUNX2 ,
- SMAD3 og
- TBP .

|

Se også
Referencer
Yderligere læsning
- Murphy LC, Alkhalaf M, Dotzlaw H, Coutts A, Haddad-Alkhalaf B (juni 1994). "Regulering af genekspression i T-47D humane brystkræftceller af progestiner og antiprogestiner". Hum. Reprod . 9 Suppl 1: 174–80. doi : 10.1093/humrep/9.suppl_1.174 . PMID 7962462 .
- Pompeiano M, Cirelli C, Arrighi P, Tononi G (1995). "c-Fos udtryk under vågenhed og søvn". Neurophysiol Clin . 25 (6): 329–41. doi : 10.1016/0987-7053 (96) 84906-9 . PMID 8904195 . S2CID 23760149 .
- Herrera DG, Robertson HA (oktober 1996). "Aktivering af c-fos i hjernen". Prog. Neurobiol . 50 (2–3): 83–107. doi : 10.1016/S0301-0082 (96) 00021-4 . PMID 8971979 . S2CID 31105978 .
- Velazquez Torres A, Gariglio Vidal P (2002). "[Mulig rolle for transkriptionsfaktor AP1 i den vævsspecifikke regulering af humant papillomavirus]". Rev. Invest. Clin. (på spansk). 54 (3): 231–42. PMID 12183893 .
eksterne links
- c-fos+Proteiner på US National Library of Medicine Medical Subject Headings (MeSH)
- c-fos+gener på US National Library of Medicine Medical Subject Headings (MeSH)
- FactorBook c-Fos
- Drosophila kajak - Den interaktive flue
- Menneskelig FOS -genomplacering og FOS -gendetaljeside i UCSC -genombrowseren .
- Oversigt over alle de tilgængelige strukturoplysninger i FBF for UniProt : P01100 (Human Proto-oncogen c-Fos) på PDBe-KB .
- Oversigt over alle de strukturelle oplysninger, der er tilgængelige i FBF for UniProt : P01101 (Mouse Proto-oncogen c-Fos) på PDBe-KB .