Medfødt hjertefejl - Congenital heart defect
| Medfødt hjertefejl | |
|---|---|
| Andre navne | Medfødt hjerteanomali, medfødt hjertesygdom |
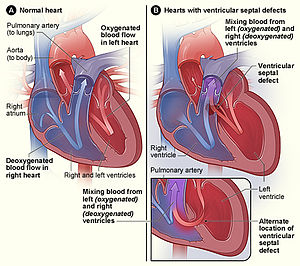 | |
| Hjertets normale struktur (til venstre) i sammenligning med to almindelige steder for en ventrikelseptumdefekt (til højre), den mest almindelige form for medfødt hjertefejl. | |
| Specialitet | Kardiologi |
| Symptomer | Hurtig vejrtrækning, blålig hud , dårlig vægtøgning, træt |
| Komplikationer | Hjertefejl |
| Typer | Cyanotiske hjertefejl , ikke-cyanotiske hjertefejl |
| Årsager | Ofte ukendt |
| Risikofaktorer | Rubella -infektion under graviditet , alkohol eller tobak , forældre er nært beslægtede, dårlig ernæringsstatus, tager antidepressiv medicin under graviditet eller fedme hos moderen |
| Behandling | Ingen, kateterbaserede procedurer , hjertekirurgi , hjertetransplantation |
| Prognose | Generelt godt (med behandling) |
| Frekvens | 48,9 millioner (2015) |
| Dødsfald: Døde | 303.300 (2015) |
En medfødt hjertefejl ( CHD ), også kendt som en medfødt hjerteanomali og medfødt hjertesygdom , er en defekt i hjertets struktur eller store kar, der er til stede ved fødslen . Tegn og symptomer afhænger af den specifikke type defekt. Symptomerne kan variere fra ingen til livstruende. Når det er til stede, kan symptomer omfatte hurtig vejrtrækning, blålig hud ( cyanose ), dårlig vægtøgning og trætthed. CHD forårsager ikke brystsmerter. De fleste medfødte hjertefejl er ikke forbundet med andre sygdomme. En komplikation af CHD er hjertesvigt .
Årsagen til en medfødt hjertefejl er ofte ukendt. Risikofaktorer omfatter visse infektioner under graviditeten, såsom røde hunde , brug af visse lægemidler eller stoffer som alkohol eller tobak , forældre, der er nært beslægtede, eller dårlig ernæringsstatus eller fedme hos moderen. At have en forælder med en medfødt hjertefejl er også en risikofaktor. En række genetiske tilstande er forbundet med hjertefejl, herunder Downs syndrom , Turners syndrom og Marfan syndrom . Medfødte hjertefejl er opdelt i to hovedgrupper: cyanotiske hjertefejl og ikke-cyanotiske hjertefejl , afhængigt af om barnet har potentiale til at blive blålig i farven. Defekterne kan involvere hjerteets indre vægge, hjerteklapperne eller de store blodkar, der fører til og fra hjertet.
Medfødte hjertefejl kan delvist forebygges gennem rubella -vaccination , tilsætning af jod til salt og tilsætning af folsyre til visse fødevarer. Nogle defekter behøver ikke behandling. Andre kan effektivt behandles med kateterbaserede procedurer eller hjertekirurgi . Nogle gange kan der være behov for en række operationer, eller en hjertetransplantation kan være påkrævet. Med passende behandling er resultaterne generelt gode, selv med komplekse problemer.
Medfødte hjertefejl er den mest almindelige fødselsdefekt . I 2015 var de til stede hos 48,9 millioner mennesker globalt. De påvirker mellem 4 og 75 pr. 1.000 levendefødte, afhængigt af hvordan de diagnosticeres. I omkring 6 til 19 pr. 1.000 forårsager de en moderat til alvorlig grad af problemer. Medfødte hjertefejl er den største årsag til fødselsdefektrelaterede dødsfald: i 2015 resulterede de i 303.300 dødsfald, ned fra 366.000 dødsfald i 1990.
tegn og symptomer
Tegn og symptomer er relateret til hjertefejlets type og sværhedsgrad. Symptomer opstår ofte tidligt i livet, men det er muligt for nogle CHD'er at blive uopdaget gennem livet. Nogle børn har ingen tegn, mens andre kan udvise åndenød, cyanose , besvimelse , hjerteklump , underudvikling af lemmer og muskler, dårlig fodring eller vækst eller luftvejsinfektioner. Medfødte hjertefejl forårsager unormal hjertestruktur, hvilket resulterer i produktion af visse lyde, der kaldes hjerteklump . Disse kan undertiden opdages ved auskultation ; dog er det ikke alle hjertemumler, der skyldes medfødte hjertefejl.
Tilhørende forhold
Medfødte hjertefejl er forbundet med en øget forekomst af syv andre specifikke medicinske tilstande, tilsammen kaldet VACTERL -foreningen :
- V - Vertebrale anomalier
- A - Anal atresia
- C - Kardiovaskulære anomalier
- T - Tracheoesophageal fistel
- E - esophageal atresi
- R - Renal (nyre) og/eller radiale anomalier
- L - Limb defekter
Ventrikelseptumdefekt (VSD), atriale septaldefekter og tetralogi af Fallot er de mest almindelige medfødte hjertefejl set i VACTERL -foreningen. Mindre almindelige defekter i foreningen er truncus arteriosus og transposition af de store arterier.
Årsager
Årsagen til medfødt hjertesygdom kan være genetisk, miljømæssig eller en kombination af begge.
Genetisk
Genetiske mutationer , ofte sporadiske, repræsenterer den største kendte årsag til medfødte hjertefejl. De er beskrevet i nedenstående tabel.
| Genetiske læsioner | Tilskrivelige procent | Eksempler | Primær gentest metode |
|---|---|---|---|
| Aneuploidier | 5-8% | Overlevende autosomale trisomier (kromosomer 13 , 18 , 21 ), kromosom X -monosomi (Turners syndrom) | Karyotyping |
| Kopier talvarianter | 10-12% | 22q11.2 sletning/duplikering (velocardiofacial/DiGeorge syndrom) , 1 q21.1 sletning/duplikering , 8p23.1 sletning/duplikering , 15q11.2 sletning (Burnside-Butlers syndrom) | Array komparativ genomisk hybridisering (også kendt som kromosomal mikroarrayanalyse) |
| Arvelig proteinkodende enkeltnukleotidvariant (SNV) eller lille indsættelse/sletning (indel) | 3-5% | Holt-Oram syndrom , Noonan syndrom , Alagille syndrom | Genpanel |
| De novo proteinkodende SNV eller indel | ~ 10% | Mutationer i gener udtrykt stærkt under hjerteudvikling | Hele exome sekventering |
Molekylære veje
Generne, der regulerer den komplekse udviklingssekvens, er kun delvist belyst. Nogle gener er forbundet med specifikke defekter. En række gener er blevet forbundet med hjerte -manifestationer. Mutationer af et hjertemuskelprotein, α-myosin tung kæde ( MYH6 ) er forbundet med atriale septaldefekter. Flere proteiner, der interagerer med MYH6, er også forbundet med hjertefejl. Transkriptionsfaktoren GATA4 danner et kompleks med TBX5, som interagerer med MYH6. En anden faktor, homeobox (udviklingsmæssigt) genet, NKX2-5 , interagerer også med MYH6. Mutationer af alle disse proteiner er forbundet med både atriale og ventrikulære septaldefekter; Derudover er NKX2-5 forbundet med defekter i hjertets elektriske ledning, og TBX5 er relateret til Holt-Oram syndrom, som omfatter elektriske ledningsfejl og abnormiteter i overekstremiteten. Den Wnt signaling cofaktorer BCL9 , BCL9L og PYGO kunne være en del af denne molekylære veje, som når deres gener er muterede, forårsager dette Fænotypers ligner den funktioner til stede i Holt-Oram-syndrom . Et andet T-box-gen, TBX1 , er involveret i velo-cardio-facial syndrom DiGeorge syndrom , den mest almindelige deletion, der har omfattende symptomer, herunder defekter i hjerteudstrømningskanalen, herunder tetralogi af Fallot .
| MYH6 | GATA4 | NKX2-5 | TBX5 | TBX1 | |
|---|---|---|---|---|---|
| Locus | 14q11.2-q13 | 8p23.1-p22 | 5q34 | 12q24.1 | 22q11.2 |
| Syndrom | Holt-Oram | DiGeorge | |||
| Atrial septal defekter | ✔ | ✔ | ✔ | ✔ | |
| Ventrikelseptumdefekter | ✔ | ✔ | ✔ | ||
| Elektriske ledningsforstyrrelser | ✔ | ✔ | |||
| Udløbskanal abnormiteter | ✔ | ||||
| Ikke-kardiale manifestationer | Afvigelser i øvre lemmer | Lille eller fraværende thymus Små eller fraværende parathyroider Facial abnormiteter |
Den hak signalvej , en reguleringsmekanisme for cellevækst og differentiering, spiller roller, i flere aspekter af hjerte- udvikling. Hakelementer er involveret i bestemmelsen af højre og venstre side af kropsplanen, så den retningsvise foldning af hjertet kan påvirkes. Hakssignalering er involveret tidligt i dannelsen af de endokardielle puder og fortsætter med at være aktiv, efterhånden som udviklingen til septa og ventiler. Det er også involveret i udviklingen af ventrikelvæggen og forbindelsen af udstrømningskanalen til de store kar. Mutationer i genet for en af de hakkede ligander, Jagged1 , identificeres i de fleste undersøgte tilfælde af arteriohepatisk dysplasi ( Alagille syndrom ), karakteriseret ved defekter i de store kar (lungearteriestenose), hjerte ( tetralogi af Fallot hos 13% tilfælde), lever, øjne, ansigt og knogler. Selvom mindre end 1% af alle tilfælde, hvor der ikke findes defekter i Jagged1 -genet, findes defekter i Notch2 -genet. I 10% af tilfældene findes ingen mutation i begge gen. For et andet medlem af genfamilien er mutationer i Notch1 -genet forbundet med bicuspid aortaklapp , en ventil med to foldere i stedet for tre. Notch1 er også forbundet med forkalkning af aortaklappen, den tredje mest almindelige årsag til hjertesygdomme hos voksne.
Mutationer af en celle -reguleringsmekanisme, Ras / MAPK -vejen er ansvarlige for en række forskellige syndromer, herunder Noonan syndrom , LEOPARD syndrom , Costello syndrom og kardiofaciokutant syndrom , hvor der er hjerteinvolvering. Selvom de angivne tilstande er kendte genetiske årsager, er der sandsynligvis mange andre gener, der er mere subtile. Det vides, at risikoen for medfødte hjertefejl er højere, når der er en nær slægtning med en.
Miljø
Kendte miljøfaktorer omfatter visse infektioner under graviditeten, såsom røde hunde , medicin ( alkohol , hydantoin , lithium og thalidomid ) og mors sygdom ( diabetes mellitus , phenylketonuri og systemisk lupus erythematosus ). Alkoholeksponering hos faderen ser også ud til at øge risikoen for medfødte hjertefejl.
At være overvægtige eller fede øger risikoen for medfødt hjertesygdom. Desuden øges risikoen for hjertefejl, efterhånden som fedme hos moderen stiger. Der er ikke identificeret en særskilt fysiologisk mekanisme til at forklare sammenhængen mellem moderens fedme og CHD, men både folatmangel før graviditet og diabetes har været impliceret i nogle undersøgelser.
Mekanisme
Der er en kompleks begivenhedssekvens, der resulterer i et velformet hjerte ved fødslen, og afbrydelse af enhver del kan resultere i en defekt. Den ordnede timing af cellevækst, cellemigration og programmeret celledød (" apoptose ") er blevet undersøgt grundigt, og de gener, der styrer processen, bliver belyst. Omkring udviklingsdag 15 findes de celler, der vil blive hjertet, i to hesteskoformede bånd i det midterste vævslag ( mesoderm ), og nogle celler vandrer fra en del af det ydre lag ( ektoderm ), det neurale kam , som er kilde til en række forskellige celler, der findes i hele kroppen. På udviklingsdag 19 dannes et par vaskulære elementer, "endokardierør". Rørene smelter sammen, når celler mellem derefter undergår programmeret død, og celler fra det første hjertefelt migrerer til røret og danner en ring af hjerteceller ( myocytter ) omkring det ved dag 21. På dag 22 begynder hjertet at slå og om dagen 24, cirkulerer blod.
På dag 22 er kredsløbssystemet bilateralt symmetrisk med parrede kar på hver side og hjertet består af et simpelt rør placeret i midten af kroppens layout. De dele, der vil blive atria og vil være placeret tættest på hovedet, er de mest fjerne fra hovedet. Fra dag 23 til og med 28 folder og vrider hjertet sig, hvor de fremtidige ventrikler bevæger sig til venstre for midten (hjertets ultimative placering) og atrierne bevæger sig mod hovedet.
På dag 28 begynder områder af væv i hjerterøret at ekspandere indad; efter cirka to uger smelter disse udvidelser, det membranøse " septum primum " og de muskulære " endokardiepuder " til at danne hjertets fire kamre. Manglende korrekt smeltning vil resultere i en defekt, der kan tillade blod at lække mellem kamre. Efter at dette er sket, begynder celler, der er migreret fra det neurale kam, at dele bulbus cordis , hovedudstrømningskanalen deles i to af væksten et spiralformet septum og bliver de store kar - det stigende segment af aorta og lungestammen. Hvis adskillelsen er ufuldstændig, er resultatet en "vedvarende truncus arteriose". Fartøjerne kan vendes (" transponering af de store fartøjer "). De to halvdele af den splittede kanal skal migrere til de korrekte positioner over de relevante ventrikler. En svigt kan resultere i, at noget blod strømmer ind i det forkerte kar ( f.eks. Tilsidesættende aorta ). Det firkammerede hjerte og de store kar har funktioner, der kræves for fostrets vækst . Lungerne er ikke ekspanderede og kan ikke rumme det fulde kredsløb. Der findes to strukturer til at shunt blodgennemstrømningen væk fra lungerne. Celler i en del af septum primum dør og skaber et hul, mens muskelceller, " septum secundum ", vokser langs den højre atrialside septum primum, bortset fra en region og efterlader et hul, hvorigennem blod kan passere fra højre artium til venstre atrium, foramen ovale . Et lille fartøj, ductus arteriosus, tillader blod fra lungearterien at passere til aorta.
Ændringer ved fødslen
Ductus arteriosus forbliver åben på grund af cirkulerende faktorer, herunder prostaglandiner . Foramen ovale forbliver åben på grund af blodstrømmen fra højre atrium til venstre atrium. Efterhånden som lungerne ekspanderer, flyder blod let gennem lungerne, og den membranøse del af foramen ovale (septum primum) flopper over den muskulære del (septum secundum). Hvis lukningen er ufuldstændig, er resultatet et patent foramen ovale . De to klapper kan smelte sammen, men mange voksne har en foramen ovale, der kun forbliver lukket på grund af trykforskellen mellem atrierne.
Teorier
Rokitansky (1875) forklarede medfødte hjertefejl som brud på hjerteudviklingen på forskellige ontogenese -stadier . Spitzer (1923) behandler dem som tilbagevenden til et af fylogenese -stadierne. Krimski (1963), der syntetiserede to tidligere synspunkter, betragtede medfødte hjertesygdomme som et stop for udvikling på et bestemt stadium af ontogenese, svarende til denne eller den anden fase af fylogenesen. Derfor kan disse teorier kun forklare feminine og neutrale typer defekter.
Diagnose
Mange medfødte hjertefejl kan diagnosticeres prenatalt ved føtal ekkokardiografi . Dette er en test, der kan udføres i anden trimester af graviditeten, når kvinden er omkring 18–24 uger gravid. Det kan være en abdominal ultralyd eller transvaginal ultralyd .
Hvis en baby er født med cyanotisk hjertesygdom, stilles diagnosen normalt kort tid efter fødslen på grund af den blå hudfarve (kaldet cyanose).
Hvis en baby er født med en septaldefekt eller en obstruktionsdefekt, er deres symptomer ofte kun mærkbare efter flere måneder eller nogle gange endda efter mange år.
Klassifikation
Der findes en række klassifikationssystemer for medfødte hjertefejl. I 2000 blev den internationale medfødte hjertekirurgiske nomenklatur udviklet til at tilvejebringe et generisk klassifikationssystem.
Hypoplasi
Hypoplasi kan påvirke hjertet, hvilket typisk resulterer i underudvikling af højre eller venstre ventrikel . Dette får kun den ene side af hjertet til at kunne pumpe blod effektivt til kroppen og lungerne . Hypoplasi i hjertet er sjælden, men er den mest alvorlige form for CHD. Det kaldes hypoplastisk venstre hjertesyndrom, når det påvirker venstre side af hjertet og hypoplastisk højre hjertesyndrom, når det påvirker højre side af hjertet. Under begge forhold er tilstedeværelsen af et patent ductus arteriosus (og, når hypoplasi påvirker den højre side af hjertet, et patent foramen ovale ) afgørende for spædbarnets evne til at overleve, indtil akut hjerteoperation kan udføres, da uden disse veje blod ikke kan cirkulere til kroppen (eller lungerne, afhængigt af hvilken side af hjertet der er defekt). Hypoplasi i hjertet er generelt en cyanotisk hjertefejl .
Obstruktive defekter
Obstruktive defekter opstår, når hjerteklapper, arterier eller vener er unormalt smalle eller blokerede . Almindelige defekter omfatter pulmonal stenose , aortastenose og koarktation af aorta , hvor andre typer, såsom bicuspid aortaklappestenose og subaortic stenose er forholdsvis sjældne. Enhver indsnævring eller blokering kan forårsage hjerteforstørrelse eller hypertension .
Septal defekter
Skillevæggen er en vævsvæg, der adskiller venstre hjerte fra højre hjerte . Defekter i det interatriale septum eller det interventrikulære septum tillader blod at strømme fra venstre side af hjertet til højre, hvilket reducerer hjertets effektivitet. Ventrikelseptumdefekter er samlet set den mest almindelige type CHD, selvom cirka 30% af voksne har en type atriefeptaldefekt kaldet probe patent foramen ovale .
Cyanotiske defekter
Cyanotiske hjertefejl kaldes sådan, fordi de resulterer i cyanose , en blågrå misfarvning af huden på grund af iltmangel i kroppen. Sådanne defekter omfatter vedvarende truncus arteriosus , total anomaløs lungevene forbindelse , tetralogi af Fallot , transponering af de store kar og tricuspid atresi .
Defekter
- Aortastenose
- Atrial septal defekt (ASD)
- Atrioventrikulær septaldefekt (AVSD)
- Bicuspid aortaklappen
- Kardiomyopati
- Komplet hjerteblok (CHB)
- Dextrocardia
- Dobbelt indløb venstre ventrikel (DILV)
- Dobbelt udløb højre ventrikel (DORV)
- Ebsteins anomali
- Hypoplastisk venstre hjerte syndrom (HLHS)
- Hypoplastisk højre hjertesyndrom (HRHS)
- Mitral stenose
- Vedvarende truncus arteriosus
- Lungeatresi
- Lungestenose
- Rhabdomyomas (Tumorer i hjertet)
- Gennemførelse af de store fartøjer
- Tricuspid atresia
- Ventrikelseptumdefekt (VSD)
- Wolff-Parkinson-White syndrom (WPW)
Nogle forhold påvirker de store kar eller andre kar i nærheden af hjertet, men ikke hjertet selv, men klassificeres ofte som medfødte hjertefejl.
- Koartation af aorta (CoA)
- Dobbelt aortabue , afvigende subklavisk arterie og andre misdannelser i de store arterier
- Afbrudt aortabue (IAA)
- Patent ductus arteriosus (PDA)
- Scimitar syndrom (SS)
Nogle konstellationer af flere defekter findes almindeligvis sammen.
- Tetralogy of Fallot (ToF)
- Pentalogi af Cantrell
- Shones syndrom / Shones kompleks / Shones anomali
Behandling
CHD kan kræve kirurgi og medicin. Medicin omfatter diuretika, som hjælper kroppen med at fjerne vand, salte og digoxin for at styrke hjertets sammentrækning. Dette bremser hjerterytmen og fjerner noget væske fra væv. Nogle defekter kræver kirurgiske procedurer for at genoprette kredsløbet tilbage til det normale, og i nogle tilfælde er det nødvendigt med flere operationer.
Interventionel kardiologi tilbyder nu patienter minimalt invasive alternativer til kirurgi for nogle patienter. Melody Transcatheter Pulmonary Valve (TPV), godkendt i Europa i 2006 og i USA i 2010 under en humanitær enhedsfritagelse (HDE), er designet til at behandle medfødte hjertesygdomspatienter med en dysfunktionel ledning i deres højre ventrikulære udstrømningskanal (RVOT) . RVOT er forbindelsen mellem hjerte og lunger; når blod når lungerne, er det beriget med ilt, før det pumpes til resten af kroppen. Transcatheter lungeventilteknologi giver et mindre invasivt middel til at forlænge levetiden for en mislykket RVOT-kanal og er designet til at give læger mulighed for at levere en ny lungeventil via et kateter gennem patientens blodkar.
Mange mennesker kræver livslang specialiseret hjertepleje, først hos en pædiatrisk kardiolog og senere hos en voksen medfødt kardiolog. Der er mere end 1,8 millioner voksne, der lever med medfødte hjertefejl.
Epidemiologi
Hjertefejl er blandt de mest almindelige fødselsdefekter , der forekommer hos 1% af levendefødte (2-3% inklusive bicuspid aortaklappen). I 2013 havde 34,3 millioner mennesker CHD. I 2010 resulterede de i 223.000 dødsfald, ned fra 278.000 dødsfald i 1990.
For medfødte hjertefejl, der opstår uden en familiehistorie ( de novo ), er tilbagefaldsrisikoen hos afkom 3-5%. Denne risiko er højere ved forhindringer i venstre ventrikel udstrømningskanal, heterotaksi og atrioventrikulære septaldefekter.
Terminologi
Medfødte hjertefejl er kendt af en række navne, herunder medfødt hjerteanomali, medfødt hjertesygdom, hjertefejl og medfødte kardiovaskulære misdannelser.
Se også
Referencer
eksterne links
| Klassifikation | |
|---|---|
| Eksterne ressourcer |
- Medfødt hjertefejl hos Curlie
- Oplysninger om medfødt hjertesygdom til forældre.