Hæmatopoiesis - Haematopoiesis
Hæmatopoiese ( / h ɪ ˌ m æ t oʊ p ɔɪ jeg s ɪ s , h jeg m ə t oʊ -, ˌ h ɛ m ə - / , fra græsk αἷμα , 'blod' og ποιεῖν 'for at gøre'; også hæmatopoiesis på amerikansk engelsk; undertiden også h (a) emopoiesis ) er dannelsen af blodcellekomponenter . Alle cellulære blodkomponenter stammer fra hæmatopoietiske stamceller . I en sund voksen person, ca. 10 11 -10 12 nye blodlegemer produceres dagligt for at opretholde steady state niveauer i det perifere kredsløb.
Behandle
Hæmatopoietiske stamceller (HSC'er)
Hæmatopoietiske stamceller (HSC'er) bor i knoglens medulla ( knoglemarv ) og har den unikke evne til at give anledning til alle de forskellige modne blodlegemer og væv. HSC'er er selvfornyende celler: når de differentierer, forbliver i det mindste nogle af deres datterceller som HSC'er, så puljen af stamceller ikke er opbrugt. Dette fænomen kaldes asymmetrisk division. De andre døtre til HSC'er ( myeloide og lymfoide stamceller) kan følge en hvilken som helst af de andre differentieringsveje, der fører til produktion af en eller flere specifikke typer blodceller, men ikke kan forny sig. Puljen af forfædre er heterogen og kan opdeles i to grupper; langsigtet selvfornyende HSC og kun forbigående selvfornyende HSC, også kaldet short-term. Dette er en af de vigtigste vitale processer i kroppen.
Celletyper
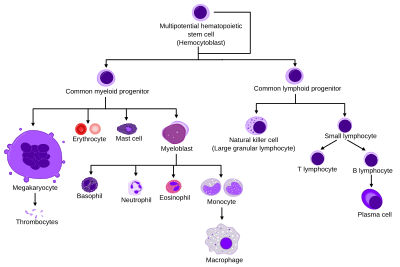
Alle blodlegemer er opdelt i tre slægter.
- Røde blodlegemer , også kaldet erytrocytter, er de iltbærende celler . Erythrocytter er funktionelle og frigives i blodet. Antallet af reticulocytter, umodne røde blodlegemer, giver et skøn over hastigheden af erythropoiesis .
- Lymfocytter er hjørnestenen i det adaptive immunsystem. De stammer fra almindelige lymfoide forfædre. Den lymfoide slægt består af T-celler , B-celler og naturlige dræberceller . Dette er lymfopoiesis .
- Celler i den myeloide slægt, der omfatter granulocytter , megakaryocytter og makrofager , er afledt af almindelige myeloide forfædre og er involveret i så forskellige roller som medfødt immunitet og blodkoagulation . Dette er myelopoiesis .
Granulopoiesis (eller granulocytopoiesis) er hæmatopoese af granulocytter undtagen for mastceller, der er granulocytter, men med en ekstramedullær modning.
Megakaryocytopoiesis er hæmatopoies af megakaryocytter.
Terminologi
Mellem 1948 og 1950 udsendte Udvalget for Afklaring af Nomenklaturen for Celler og Sygdomme i Blodet og Bloddannende Organer rapporter om blodcellernes nomenklatur. En oversigt over terminologien er vist nedenfor, fra tidligste til sidste udviklingstrin:
- [root] blast
- pro [root] cyte
- [root] cyte
- meta [root] cyte
- modent cellenavn
Roden til erytrocytkolonidannende enheder (CFU-E) er "rubri", for granulocyt-monocyt-kolonidannende enheder (CFU-GM) er "granulo" eller "myelo" og "mono", for lymfocytkolonidannende enheder (CFU-L) er "lymfo" og for megakaryocyt er kolonidannende enheder (CFU-Meg) "megakaryo". Ifølge denne terminologi ville stadierne af dannelse af røde blodlegemer være: rubriblast, prorubricyte, rubricyt, metarubricyte og erythrocyt. Følgende nomenklatur synes imidlertid på nuværende tidspunkt at være den mest udbredte:
| Udvalg | "lymfo" | "rubri" | "granulo" eller "myelo" | "mono" | "megakaryo" |
|---|---|---|---|---|---|
| Afstamning | Lymfoid | Myeloid | Myeloid | Myeloid | Myeloid |
| CFU | CFU-L | CFU-GEMM → CFU-E | CFU-GEMM → CFU-GM → CFU-G | CFU-GEMM → CFU-GM → CFU-M | CFU-GEMM → CFU-Meg |
| Behandle | lymfocytopoiesis | erythropoiesis | granulocytopoiesis | monocytopoiesis | trombocytopoiesis |
| [root] blast | Lymfoblast | Proerythroblast | Myeloblast | Monoblast | Megakaryoblast |
| pro [root] cyte | Prolymfocyt | Polykromatofil erytrocyt | Promyelocyt | Promonocyt | Promegakaryocyt |
| [root] cyte | - | Normoblast | Eosino / neutro / basofil myelocyt | Megakaryocyt | |
| meta [root] cyte | Stor lymfocyt | Retikulocyt | Eosinofil / neutrofil / basofile metamyelocyte , eosinofil / neutrofil / basofil band celle | Tidlig monocyt | - |
| modent cellenavn | Lille lymfocyt | Erythrocyt | granulocytter ( Eosino / neutro / basofil ) | Monocyt | trombocytter ( blodplader ) |
Osteoklaster stammer også fra hæmopoietiske celler i monocyt-/neutrofil-afstamningen, specifikt CFU-GM.
Beliggenhed
Ved udvikling af embryoner forekommer bloddannelse i aggregater af blodlegemer i æggeblommesækken, kaldet blodøer . Efterhånden som udviklingen skrider frem, forekommer bloddannelse i milten , leveren og lymfeknuderne . Når knoglemarv udvikler sig, påtager det sig til sidst opgaven med at danne de fleste blodlegemer for hele organismen. Modning, aktivering og en vis spredning af lymfoide celler forekommer imidlertid i milten, thymus og lymfeknuder. Hos børn forekommer hæmatopoiesis i marven på de lange knogler, såsom lårbenet og skinnebenet. Hos voksne forekommer det hovedsageligt i bækkenet, kraniet, ryghvirvlerne og brystbenet.
Ekstramedullær
I nogle tilfælde kan leveren, thymus og milten genoptage deres hæmatopoietiske funktion, hvis det er nødvendigt. Dette kaldes ekstramedullær hæmatopoiesis . Det kan få disse organer til at stige i størrelse betydeligt. Under fosterudviklingen, da knogler og dermed knoglemarven udvikler sig senere, fungerer leveren som det vigtigste hæmatopoetiske organ. Derfor forstørres leveren under udviklingen. Ekstramedullær hæmatopoiesis og myelopoiesis kan levere leukocytter i hjerte -kar -sygdomme og betændelse i voksenalderen. Spleniske makrofager og adhæsionsmolekyler kan være involveret i regulering af ekstramedullær myeloid cellegenerering ved hjerte -kar -sygdomme .
Modning
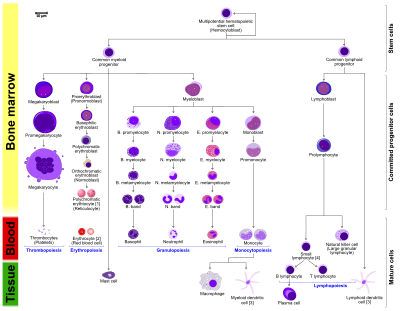
- De morfologiske egenskaber ved de hæmatopoietiske celler er vist som ses i en Wrights plet, May-Giemsa-plet eller May-Grünwald-Giemsa-plet. Alternative navne på bestemte celler er angivet mellem parenteser.
- Visse celler kan have mere end et karakteristisk udseende. I disse tilfælde er mere end én repræsentation af den samme celle blevet inkluderet.
- Tilsammen udgør monocytten og lymfocytterne agranulocytterne i modsætning til granulocytterne (basofil, neurtofil og eosinofil), der produceres under granulopoiesis.
- B., N. og E. står for henholdsvis Basofil, Neutrofil og Eosinofil - som i Basofil promyelocyt. For lymfocytter er T og B faktiske betegnelser.
- Den polykromatiske erythrocyt (reticulocyt) til højre viser sit karakteristiske udseende, når den er farvet med methylenblåt eller Azure B.
- Erytrocyt til højre er en mere præcis repræsentation af dens udseende i virkeligheden, når det ses gennem et mikroskop.
- Andre celler, der stammer fra monocytten: osteoklast, mikroglia (centralnervesystem), Langerhans -celle (epidermis), Kupffer -celle (lever).
- For klarhedens skyld er T- og B-lymfocytter delt for bedre at indikere, at plasmacellen stammer fra B-cellen. Bemærk, at der ikke er nogen forskel i udseendet af B- og T-celler, medmindre specifik farvning påføres.
Når en stamcelle modnes, gennemgår den ændringer i genekspression, der begrænser de celletyper, den kan blive, og flytter den tættere på en bestemt celletype ( celledifferentiering ). Disse ændringer kan ofte spores ved at overvåge tilstedeværelsen af proteiner på overfladen af cellen. Hver successive ændring flytter cellen tættere på den endelige celletype og begrænser yderligere dens potentiale til at blive en anden celletype.
Bestemmelse af celleskæbne
To modeller for hæmatopoiesis er blevet foreslået: determinisme og stokastisk teori. For stamcellerne og andre udifferentierede blodlegemer i knoglemarven forklares bestemmelsen generelt med determinisme teorien om hæmatopoiesis og siger, at kolonistimulerende faktorer og andre faktorer i det hæmatopoietiske mikromiljø bestemmer cellerne for at følge en bestemt celledifferentieringsvej. Dette er den klassiske måde at beskrive hæmatopoiesis. I stokastisk teori differentierer udifferentierede blodlegemer til bestemte celletyper ved tilfældighed. Denne teori er blevet understøttet af eksperimenter, der viser, at inden for en population af musens hæmatopoietiske stamceller, underliggende stokastisk variabilitet i fordelingen af Sca-1 , en stamcellefaktor , opdeler befolkningen i grupper, der udviser variable hastigheder for cellulær differentiering . For eksempel under påvirkning af erythropoietin (en erythrocyt-differentieringsfaktor) differentierede en subpopulation af celler (som defineret af niveauerne af Sca-1) til erytrocytter med en syvdoblet højere hastighed end resten af befolkningen. Desuden blev det vist, at hvis den fik lov til at vokse, genetablerede denne subpopulation den oprindelige subpopulation af celler, hvilket understøttede teorien om, at dette er en stokastisk, reversibel proces. Et andet niveau, hvor stokasticitet kan være vigtigt, er i færd med apoptose og selvfornyelse. I dette tilfælde hersker det hæmatopoietiske mikromiljø hos nogle af cellerne for at overleve, og nogle på den anden side for at udføre apoptose og dø. Ved at regulere denne balance mellem forskellige celletyper kan knoglemarven ændre mængden af forskellige celler til i sidste ende at blive produceret.
Vækstfaktorer

Røde og hvide blodlegemers produktion reguleres med stor præcision hos raske mennesker, og produktionen af leukocytter øges hurtigt under infektion. Spredning og selvfornyelse af disse celler afhænger af vækstfaktorer. En af nøglespillerne i selvfornyelse og udvikling af hæmatopoietiske celler er stamcellefaktor (SCF), som binder sig til c-kit-receptoren på HSC. Fravær af SCF er dødelig. Der er andre vigtige glycoproteinvækstfaktorer , der regulerer proliferation og modning, såsom interleukiner IL-2 , IL-3 , IL-6 , IL-7 . Andre faktorer, kaldet kolonistimulerende faktorer (CSF'er), stimulerer specifikt produktionen af engagerede celler. Tre CSF'er er granulocyt-makrofag CSF (GM-CSF), granulocyt CSF (G-CSF) og makrofag CSF (M-CSF). Disse stimulerer granulocytdannelse og er aktive på enten stamceller eller slutproduktceller.
Erythropoietin er påkrævet for at en myeloid stamcelle skal blive en erytrocyt. På den anden side får thrombopoietin myeloide stamceller til at differentiere sig til megakaryocytter ( trombocytdannende celler). Diagrammet til højre giver eksempler på cytokiner og de differentierede blodlegemer, de giver anledning til.
Transkriptionsfaktorer
Vækstfaktorer initierer signaltransduktionsveje , hvilket fører til aktivering af transkriptionsfaktorer . Vækstfaktorer fremkalder forskellige resultater afhængigt af kombinationen af faktorer og cellens differentieringsstadium. For eksempel resulterer langtidsekspression af PU.1 i myeloide engagement, og kortsigtet induktion af PU.1-aktivitet fører til dannelse af umodne eosinofiler. For nylig blev det rapporteret, at transkriptionsfaktorer, såsom NF-KB, kan reguleres af mikroRNA'er (f.eks. MiR-125b) ved hæmatopoiesis.
Den første nøglespiller for differentiering fra HSC til en multipotent progenitor (MPP) er transkriptionsfaktor CCAAT-enhancer-bindende protein α ( C/EBP α). Mutationer i C/EBPα er forbundet med akut myeloid leukæmi . Fra dette tidspunkt kan celler enten differentiere langs Erythroid-megakaryocyt-afstamningen eller lymfoide og myeloid-slægt, der har fælles stamceller, kaldet lymfoide-primet multipotent stamfader. Der er to hovedtranskriptionsfaktorer. PU.1 for Erythroid-megakaryocyt-afstamning og GATA-1 , hvilket fører til en lymfoide-primet multipotent progenitor.
Andre transkriptionsfaktorer omfatter Ikaros ( B -celleudvikling ) og Gfi1 (fremmer Th2 -udvikling og hæmmer Th1) eller IRF8 ( basofiler og mastceller ). Betydeligt fremkalder visse faktorer forskellige reaktioner på forskellige stadier i hæmatopoiesen. For eksempel CEBPα i neutrofil udvikling eller PU.1 i monocytter og dendritisk celleudvikling. Det er vigtigt at bemærke, at processer ikke er ensrettede: differentierede celler kan genvinde egenskaber for stamceller.
Et eksempel er PAX5 -faktor, som er vigtig i B -celleudvikling og forbundet med lymfomer. Overraskende tillod pax5 betingede knock-out-mus, at perifere modne B-celler kunne differentieres til tidlige knoglemarvsforfædre. Disse fund viser, at transkriptionsfaktorer fungerer som plejere af differentieringsniveau og ikke kun som initiativtagere.
Mutationer i transkriptionsfaktorer er tæt forbundet med blodkræft som akut myeloid leukæmi (AML) eller akut lymfoblastisk leukæmi (ALL). For eksempel er Ikaros kendt for at være regulator for mange biologiske begivenheder. Mus uden Ikaros mangler B -celler , Natural killer og T -celler . Ikaros har seks zinkfingre- domæner, fire er bevaret DNA-bindende domæne og to er til dimerisering . Meget vigtigt fund er, at forskellige zinkfingre er involveret i binding til forskellige steder i DNA, og dette er årsagen til pleiotropisk effekt af Ikaros og forskellig involvering i kræft, men hovedsageligt er mutationer forbundet med BCR-Abl- patienter, og det er en dårlig prognostisk markør .
Andre dyr
Hos nogle hvirveldyr kan hæmatopoies forekomme, hvor der er et løst stroma af bindevæv og langsom blodtilførsel, såsom tarmen , milten eller nyrerne .
Se også
- Klonal hæmatopoiesis
- Erythropoiesis-stimulerende midler
- Haematon
- Hæmatopoietiske stimulanser:
- Leukocyt ekstravasation
Referencer
Yderligere læsning
- Godin, Isabelle; Cumano, Ana, red. (2006). Hæmatopoietisk stamcelleudvikling . Springer. ISBN 978-0-306-47872-7.
eksterne links
| Scholia har et emne profil for hæmatopoiese . |