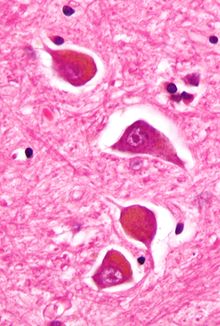
Hepatisk encefalopati - Hepatic encephalopathy
| Hepatisk encefalopati | |
|---|---|
| Andre navne | Portosystemisk encefalopati, hepatisk koma, koma hepaticum |
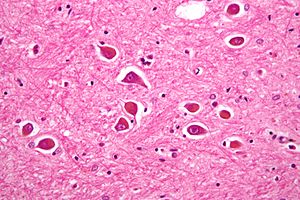 | |
| Mikrograf af Alzheimer type II astrocytter , som det kan ses ved hepatisk encefalopati. | |
| Specialitet | Gastroenterologi |
| Symptomer | Ændret bevidsthedsniveau , humørsvingninger, personlighedsændringer, bevægelsesproblemer |
| Typer | Akut, tilbagevendende, vedholdende |
| Årsager | Leversvigt |
| Risikofaktorer | Infektioner , gastrointestinal blødning , forstoppelse , elektrolytproblemer , visse lægemidler |
| Diagnostisk metode | Baseret på symptomer efter at have udelukket andre mulige årsager |
| Differential diagnose | Wernicke – Korsakoffs syndrom , delirium tremens , hypoglykæmi , subduralt hæmatom , hyponatræmi |
| Behandling | Støttende pleje , behandling af triggere, lactulose , levertransplantation |
| Prognose | Gennemsnitlig levealder mindre end et år hos dem med alvorlig sygdom |
| Frekvens | Påvirker> 40% med skrumpelever |
Hepatisk encefalopati ( HE ) er et ændret bevidsthedsniveau som følge af leversvigt . Dens begyndelse kan være gradvis eller pludselig. Andre symptomer kan omfatte bevægelsesproblemer, ændringer i humør eller ændringer i personlighed . I de avancerede stadier kan det resultere i koma .
Hepatisk encefalopati kan forekomme hos personer med akut eller kronisk leversygdom. Episoder kan udløses af infektioner , GI -blødning , forstoppelse , elektrolytproblemer eller visse lægemidler. Den underliggende mekanisme menes at involvere ophobning af ammoniak i blodet, et stof, der normalt fjernes af leveren . Diagnosen er typisk baseret på symptomer efter at have udelukket andre potentielle årsager. Det kan understøttes af ammoniakniveauer i blodet, et elektroencefalogram eller en CT -scanning af hjernen.
Hepatisk encefalopati er muligvis reversibel med behandling. Dette indebærer typisk understøttende pleje og adressering af begivenhedens udløsere. Lactulose bruges ofte til at reducere ammoniakniveauer. Visse antibiotika (såsom rifaximin ) og probiotika er andre potentielle muligheder. En levertransplantation kan forbedre resultaterne hos dem med alvorlig sygdom.
Mere end 40% af mennesker med cirrose udvikler hepatisk encefalopati. Mere end halvdelen af dem med cirrose og signifikant HE lever mindre end et år. Hos dem, der er i stand til at få en levertransplantation, er risikoen for død mindre end 30% i løbet af de efterfølgende fem år. Tilstanden er blevet beskrevet siden mindst 1860.
tegn og symptomer
Den mildeste form for hepatisk encefalopati er vanskelig at opdage klinisk, men kan påvises ved neuropsykologisk testning . Det opleves som glemsomhed, mild forvirring og irritabilitet. Den første fase af hepatisk encefalopati er karakteriseret ved et omvendt søvn-vågne mønster (sover om dagen, er vågen om natten). Den anden fase er præget af sløvhed og personlighedsændringer. Den tredje fase er præget af forværret forvirring. Det fjerde trin er præget af en progression til koma.
Mere alvorlige former for hepatisk encefalopati fører til et forværret bevidsthedsniveau, fra sløvhed til søvnighed og til sidst koma. I de mellemliggende faser observeres en karakteristisk rykbevægelse af lemmerne ( asterixis , " leverflap " på grund af dens flappende karakter); dette forsvinder, når døsigheden forværres. Der er desorientering og hukommelsestab, og uhæmmet adfærd kan forekomme. I tredje fase kan neurologisk undersøgelse afsløre clonus og positivt Babinski -tegn . Koma og anfald repræsenterer det mest avancerede stadie; cerebralt ødem (hævelse af hjernevævet) fører til døden.
Encefalopati forekommer ofte sammen med andre symptomer og tegn på leversvigt. Disse kan omfatte gulsot (gul misfarvning af huden og det hvide i øjnene), ascites (væskeansamling i bughulen) og perifert ødem (hævelse af benene på grund af væskeophobning i huden). De senereflekser kan være overdrevet, og babinskirefleks kan være unormal, nemlig forløbende frem bøjning (Babinskis tegn) i alvorlig encephalopati. En særlig lugt på en berørt persons ånde ( foetor hepaticus ) kan detekteres.
Årsager
I en lille del af tilfældene skyldes encephalopati direkte af leversvigt; dette er mere sandsynligt ved akut leversvigt. Mere almindeligt, især ved kronisk leversygdom, udløses hepatisk encefalopati af en yderligere årsag, og det kan være vigtigt at identificere disse udløsere for at behandle episoden effektivt.
| Type | Årsager |
|---|---|
| Overdreven kvælstofbelastning |
Forbrug af store mængder protein , gastrointestinal blødning f.eks. Fra esophageal varices (blod er højt i protein, som reabsorberes fra tarmen), nyresvigt (manglende evne til at udskille nitrogenholdige affaldsstoffer såsom urinstof ), forstoppelse |
|
Elektrolyt eller metabolisk forstyrrelse |
Hyponatriæmi (lavt natriumniveau i blodet) og hypokaliæmi (lave kaliumniveauer ) - disse er begge almindelige hos dem, der tager diuretika , der ofte bruges til behandling af ascites; desuden alkalose (nedsat syreniveau), hypoxi (utilstrækkelige iltniveauer), dehydrering |
| Narkotika og medicin |
Beroligende midler såsom benzodiazepiner (ofte brugt til at undertrykke alkoholudtagning eller angstlidelse ), narkotika (brugt som smertestillende eller misbrugsmidler), antipsykotika , alkoholforgiftning |
| Infektion | Lungebetændelse , urinvejsinfektion , spontan bakteriel peritonitis , andre infektioner |
| Andre | Kirurgi , progression af leversygdommen, yderligere årsag til leverskade (f.eks. Alkoholisk hepatitis , hepatitis A ) |
| Ukendt | I 20-30% af tilfældene kan der ikke findes nogen klar årsag til et angreb |
Hepatisk encefalopati kan også forekomme efter oprettelsen af en transjugulær intrahepatisk portosystemisk shunt (TIPS). Dette bruges til behandling af ildfaste ascites , blødninger fra esophageal varices og hepatorenalt syndrom . TIPS-relateret encefalopati forekommer i cirka 30% af tilfældene, idet risikoen er højere hos dem med tidligere episoder af encefalopati, højere alder, kvindelig køn og leversygdom på grund af andre årsager end alkohol.
Patogenese

Der er forskellige forklaringer på, hvorfor leverdysfunktion eller portosystemisk shunting kan føre til encefalopati. Hos raske personer transporteres nitrogenholdige forbindelser fra tarmen , genereret af tarmbakterier fra mad, via portvenen til leveren, hvor 80–90% metaboliseres gennem urinstofcyklussen og/eller udskilles med det samme. Denne proces er nedsat i alle undertyper af hepatisk encefalopati, enten fordi hepatocytterne (levercellerne) ikke er i stand til at metabolisere affaldsprodukterne, eller fordi portalvenøst blod omgår leveren gennem sikkerhedscirkulation eller en medicinsk konstrueret shunt. Nitrogenaffaldsprodukter akkumuleres i den systemiske cirkulation (heraf det ældre udtryk "portosystemisk encefalopati"). Det vigtigste affaldsprodukt er ammoniak (NH 3 ). Dette lille molekyle krydser blod -hjerne -barrieren og absorberes og metaboliseres af astrocytterne , en population af celler i hjernen, der udgør 30% af hjernebarken . Astrocytter bruger ammoniak ved syntetisering af glutamin fra glutamat . De øgede niveauer af glutamin fører til en stigning i osmotisk tryk i astrocytterne, som bliver hævede. Der er øget aktivitet af det hæmmende y-aminosmørsyre (GABA) system, og energiforsyningen til andre hjerneceller reduceres. Dette kan betragtes som et eksempel på hjerneødem af typen "cytotoksisk".
På trods af adskillige undersøgelser, der viser ammoniaks centrale rolle, korrelerer ammoniakniveauerne ikke altid med sværhedsgraden af encefalopati; det er mistanke om, at dette betyder, at der allerede er blevet absorberet mere ammoniak i hjernen hos dem med alvorlige symptomer, hvis serumniveauer er relativt lave. Andre affaldsprodukter impliceret i hepatisk encefalopati omfatter mercaptaner (stoffer, der indeholder en thiolgruppe), kortkædede fedtsyrer og phenol .
Adskillige andre abnormiteter er blevet beskrevet ved hepatisk encefalopati, selv om deres relative bidrag til sygdomstilstanden er usikkert. Tab af glutamattransportørgenekspression (især EAAT 2) er blevet tilskrevet akut leversvigt. Benzodiazepinlignende forbindelser er blevet påvist ved forøgede niveauer såvel som abnormiteter i GABA -neurotransmissionssystemet . En ubalance mellem aromatiske aminosyrer (phenylalanin, tryptophan og tyrosin) og forgrenede aminosyrer (leucin, isoleucin og valin) er blevet beskrevet; dette ville føre til dannelse af falske neurotransmittere (f.eks. octopamin og 2-hydroxyphenethylamin ). Dysregulering af serotoninsystemet er også blevet rapporteret. Udtømning af zink og ophobning af mangan kan spille en rolle. Betændelse andre steder i kroppen kan udfælde encephalopati gennem virkningen af cytokiner og bakteriel lipopolysaccharid på astrocytter.
Diagnose
Undersøgelser
Diagnosen hepatisk encefalopati kan kun stilles i nærvær af bekræftet leversygdom (type A og C) eller en portosystemisk shunt (type B), da dens symptomer ligner dem, der opstår i andre encefalopatier . For at skelne mellem dette kræves unormale leverfunktionstest og/eller ultralyd, der tyder på leversygdom, og ideelt set en leverbiopsi . Symptomerne på hepatisk encefalopati kan også opstå fra andre tilstande, såsom blødning i hjernen og anfald (som begge er mere almindelige ved kronisk leversygdom). En CT -scanning af hjernen kan være påkrævet for at udelukke blødning i hjernen, og hvis der er mistanke om anfaldsaktivitet, kan der udføres en elektroencefalograf (EEG) undersøgelse. Sjældnere efterligninger af encefalopati er meningitis , encephalitis , Wernickes encephalopati og Wilsons sygdom ; disse kan mistænkes af kliniske årsager og bekræftes med undersøgelser.
Diagnosen hepatisk encefalopati er klinisk, når andre årsager til forvirring eller koma er udelukket; ingen test fuldstændigt diagnosticerer eller udelukker det. Serumammoniakniveauet er forhøjet hos 90% af mennesker, men ikke alle hyperammonæmi (høje ammoniakniveauer i blodet) er forbundet med encefalopati. En CT -scanning af hjernen viser normalt ingen abnormitet undtagen i fase IV encephalopati, når hjernens hævelse (cerebralt ødem) kan være synlig. Andre neuroimaging -metoder, såsom magnetisk resonansbilleddannelse (MRI), betragtes i øjeblikket ikke som nyttige, selvom de kan vise abnormiteter. Elektroencefalografi viser ingen klare abnormiteter i trin 0, selvom minimal HE er til stede; i trin I, II og III er der trifasiske bølger over frontallapperne, der svinger ved 5 Hz, og i fase IV er der langsom delta -bølgeaktivitet . Ændringerne i EEG er imidlertid ikke typiske nok til at være nyttige til at skelne hepatisk encefalopati fra andre tilstande.
Når diagnosen encephalopati er stillet, bestræber man sig på at udelukke underliggende årsager (f.eks. Anført ovenfor under " årsager "). Dette kræver blodprøver (urinstof og elektrolytter, fuldt blodtal, leverfunktionstest), normalt et røntgenbillede af brystet og urinalyse . Hvis der er ascites, kan en diagnostisk paracentese (fjernelse af en væskeprøve med en nål) være påkrævet for at identificere spontan bakteriel peritonitis (SBP).
Klassifikation
West Haven kriterier
Alvorligheden af hepatisk encefalopati er klassificeret med West Haven Criteria; dette er baseret på niveauet af nedsat autonomi, ændringer i bevidsthed, intellektuel funktion, adfærd og afhængighed af terapi.
- Grad 0 - Ingen tydelige ændringer udover et potentielt let fald i intellektuel evne og koordination
- Grade 1 - Trivial mangel på bevidsthed; eufori eller angst; forkortet opmærksomhed span; nedsat ydelse af addition eller subtraktion
- Grad 2 - Sløvhed eller apati ; minimal desorientering for tid eller sted; subtil personlighedsændring; upassende adfærd
- Grad 3 - Somnolens over for semi stupor , men lydhør over for verbale stimuli; forvirring; grov desorientering
- Grad 4 - koma
Typer
En klassificering af hepatisk encefalopati blev indført på World Congress of Gastroenterology 1998 i Wien. Ifølge denne klassifikation er hepatisk encefalopati opdelt i type A, B og C afhængigt af den underliggende årsag.
- Type A (= akut) beskriver hepatisk encefalopati forbundet med akut leversvigt , typisk forbundet med cerebralt ødem
- Type B (= bypass ) er forårsaget af portal-systemisk shunting uden tilknyttet iboende leversygdom
- Type C (= skrumpelever ) forekommer hos mennesker med skrumpelever - denne type er opdelt i episodisk , vedvarende og minimal encefalopati
Udtrykket minimal encefalopati (MHE) er defineret som encefalopati, der ikke fører til klinisk åben kognitiv dysfunktion, men kan påvises med neuropsykologiske undersøgelser. Dette er stadig et vigtigt fund, da minimal encefalopati har vist sig at forringe livskvaliteten og øge risikoen for involvering i færdselsuheld .
Minimal HE
Diagnosen minimal hepatisk encefalopati kræver neuropsykologisk test pr. Definition. Ældre tests omfatter "tal, der forbinder test" A og B (måler den hastighed, hvormed man kunne forbinde tilfældigt spredte tal 1–20), "blokdesigntesten" og "cifret-symboltesten". I 2009 konkluderede et ekspertpanel, at neuropsykologiske testbatterier rettet mod måling af flere kognitive funktionsområder generelt er mere pålidelige end enkelt test, og har en tendens til at være stærkere korreleret med funktionel status. Både det gentagelige batteri til vurdering af neuropsykologisk status (RBANS) og PSE-syndromtest kan bruges til dette formål. PSE-Syndrom-testen, der er udviklet i Tyskland og valideret i flere andre europæiske lande, indeholder ældre vurderingsværktøjer, f.eks. Nummerforbindelsestesten.
Behandling
Personer med alvorlig encefalopati (trin 3 og 4) risikerer at blokere deres luftveje på grund af nedsatte beskyttelsesreflekser, såsom gagrefleksen . Dette kan føre til åndedrætsstop . Det er påkrævet at overføre personen til et højere sygepleje, f.eks. En intensiv afdeling , og intubation af luftvejen er ofte nødvendig for at forhindre livstruende komplikationer (f.eks. Aspiration eller respirationssvigt). Placering af et nasogastrisk rør tillader sikker administration af næringsstoffer og medicin.
Behandlingen af hepatisk encefalopati afhænger af den formodede underliggende årsag (type A, B eller C) og tilstedeværelsen eller fraværet af underliggende årsager. Hvis encefalopati udvikler sig ved akut leversvigt (type A), selv i en mild form (grad 1-2), indikerer det, at en levertransplantation kan være påkrævet, og det anbefales at overføre til et specialistcenter. Hepatisk encefalopati type B kan opstå hos dem, der har gennemgået en TIPS -procedure; i de fleste tilfælde løser dette sig spontant eller med de medicinske behandlinger, der diskuteres nedenfor, men i en lille andel på ca. 5%er okklusion af shunten påkrævet for at løse symptomerne.
Ved hepatisk encefalopati type C er identifikation og behandling af alternative eller underliggende årsager central for den første behandling. I betragtning af infektionshyppigheden som den underliggende årsag administreres antibiotika ofte empirisk (uden kendskab til den nøjagtige kilde og art af infektionen). Når en episode af encefalopati er blevet effektivt behandlet, kan det være nødvendigt at tage en beslutning om, hvorvidt man skal forberede sig på en levertransplantation.
Kost
Tidligere troede man, at forbrug af proteiner selv ved normale niveauer øgede risikoen for hepatisk encefalopati. Dette har vist sig at være forkert. Desuden er mange mennesker med kronisk leversygdom underernærede og har brug for tilstrækkeligt protein til at opretholde en stabil kropsvægt. En kost med tilstrækkelig protein og energi anbefales derfor.
Kosttilskud med forgrenede aminosyrer har vist forbedring af encefalopati og andre komplikationer af cirrose. Nogle undersøgelser har vist fordel ved administration af probiotika ("sunde bakterier").
Lactulose/lactitol
Lactulose og lactitol er disaccharider , der ikke optages fra fordøjelseskanalen. De menes at reducere dannelsen af ammoniak af bakterier, gøre ammoniakken uoptagelig ved at omdanne den til ammonium (NH 4 + ) ioner og øge transit af tarmindhold gennem tarmen. Doser på 15-30 ml administreres typisk tre gange om dagen; resultatet sigter mod at være 3-5 bløde afføring om dagen eller (i nogle indstillinger) en afføring pH på <6,0. Lactulose kan også gives som lavement , især hvis encefalopati er alvorlig. Mere almindeligt, phosphat anvendes lavement. Dette kan lindre forstoppelse, en af årsagerne til encefalopati og øge tarmtransit.
Lactulose og lactitol er gavnlige til behandling af hepatisk encefalopati, og er den anbefalede førstelinjebehandling. Lactulose ser ikke ud til at være mere effektiv end lactitol til behandling af mennesker med hepatisk encefalopati. Bivirkninger af lactulose og lactitol omfatter muligheden for diarré , oppustethed i maven , gassiness og kvalme . Ved akut leversvigt er det uklart, om lactulose er gavnligt. Den mulige bivirkning af oppustethed kan forstyrre en levertransplantationsprocedure, hvis det er nødvendigt.
Antibiotika
Antibiotika rifaximin kan anbefales ud over lactulose til patienter med tilbagevendende sygdom. Det er et ikke -absorberbart antibiotikum fra rifamycinklassen . Dette menes at virke på samme måde som andre antibiotika, men uden de komplikationer, der er knyttet til neomycin eller metronidazol . På grund af den lange historie og lavere omkostninger ved brug af lactulose bruges rifaximin generelt kun som anden behandling, hvis lactulose tolereres dårligt eller ikke er effektivt. Når rifaximin sættes til lactulose, kan kombinationen af de to være mere effektiv end hver komponent separat. Rifaximin er dyrere end lactulose, men omkostningerne kan opvejes af færre hospitalsindlæggelser for encefalopati.
Antibiotika neomycin og metronidazol er andre antibiotika, der bruges til behandling af hepatisk encefalopati. Begrundelsen for deres anvendelse var, at ammoniak og andre affaldsprodukter genereres og omdannes af tarmbakterier, og at dræbe disse bakterier ville reducere dannelsen af disse affaldsprodukter. Neomycin blev valgt på grund af dets lave tarmabsorption , da neomycin og lignende aminoglycosidantibiotika kan forårsage høretab og nyresvigt, hvis det bruges ved injektion . Senere undersøgelser viste, at neomycin faktisk blev absorberet ved indtagelse gennem munden , med deraf følgende komplikationer. Metronidazol bruges på samme måde mindre almindeligt, fordi langvarig brug kan forårsage nerveskader ud over gastrointestinale bivirkninger.
L -ornithin og L -aspartat
Kombinationen af L -ornithin og L -aspartat (LOLA) sænker niveauet af ammoniak i en persons blod. Meget svagt bevis fra kliniske forsøg tyder på, at LOLA -behandling kan være til gavn for mennesker med hepatisk encefalopati. LOLA sænker ammoniakniveauerne ved at øge dannelsen af urinstof gennem urinstofcyklussen , en metabolisk vej, der fjerner ammoniak ved at gøre det til det neutrale stof urinstof . LOLA kan kombineres med lactulose og/eller rifaximin, hvis disse alene er ineffektive til at kontrollere symptomer.
Epidemiologi og prognose
Hos personer med cirrose er risikoen for at udvikle hepatisk encefalopati 20% om året, og til enhver tid viser omkring 30-45% af mennesker med cirrose tegn på åben encephalopati. Forekomsten af minimal hepatisk encefalopati, der kan påvises ved formel neuropsykologisk testning, er 60–80%; dette øger sandsynligheden for at udvikle åben encefalopati i fremtiden. Når hepatisk encefalopati er udviklet, bestemmes prognosen stort set af andre markører for leversvigt, såsom niveauerne af albumin (et protein produceret af leveren), protrombintiden (en koagulationstest , som er afhængig af proteiner produceret i leveren ), tilstedeværelsen af ascites og niveauet af bilirubin (et nedbrydningsprodukt af hæmoglobin, som konjugeres og udskilles af leveren). Sammen med sværhedsgraden af encefalopati er disse markører blevet inkorporeret i Child-Pugh-scoren ; denne score bestemmer overlevelse på et og to år og kan hjælpe med en beslutning om at tilbyde levertransplantation.
Ved akut leversvigt forudsiger udviklingen af alvorlig encefalopati stærkt kortvarig dødelighed og er næsten lige så vigtig som arten af den underliggende årsag til leversvigt ved bestemmelse af prognosen. Historisk set har meget udbredte kriterier for at tilbyde levertransplantation, såsom King's College Criteria , begrænset brug, og nylige retningslinjer afskrækker overdreven afhængighed af disse kriterier. Forekomsten af hepatisk encefalopati hos mennesker med Wilsons sygdom (arvelig kobberakkumulering) og svampeforgiftning indikerer et akut behov for en levertransplantation.
Historie
Forekomsten af forstyrret adfærd hos mennesker med gulsot kan have været beskrevet i antikken af Hippokrates of Cos (ca. 460–370 fvt). Celsus og Galen (henholdsvis første og tredje århundrede) genkendte begge tilstanden. Mange moderne beskrivelser af sammenhængen mellem leversygdom og neuropsykiatriske symptomer blev lavet i det attende og det nittende århundrede; for eksempel rapporterede Giovanni Battista Morgagni (1682–1771) i 1761, at det var en progressiv tilstand.
I 1950'erne opregnede flere rapporter de mange abnormiteter, der tidligere blev rapporteret, og bekræftede den tidligere udtalte teori om, at metabolisk svækkelse og portosystemisk shunting er de underliggende mekanismer bag hepatisk encefalopati, og at de nitrogenrige forbindelser stammer fra tarmen. Professor Dame Sheila Sherlock (1918–2001) udførte mange af disse undersøgelser på Royal Postgraduate Medical School i London og efterfølgende på Royal Free Hospital . Den samme gruppe undersøgte proteinrestriktion og neomycin.
Det West Haven klassifikation blev formuleret af professor Harold Conn (1925-2011) og hans kolleger på Yale University under behandlingen af den terapeutiske effekt af lactulose.
Referencer
eksterne links
| Klassifikation | |
|---|---|
| Eksterne ressourcer |