Fremkaldte stamceller - Induced stem cells
Inducerede stamceller ( iSC ) er stamceller afledt af somatiske , reproduktive , pluripotente eller andre celletyper ved bevidst epigenetisk omprogrammering. De klassificeres som enten totipotent (iTC), pluripotent (iPSC) eller progenitor (multipotent - iMSC, også kaldet en induceret multipotent progenitorcelle - iMPC) eller unipotent - (iUSC) i henhold til deres udviklingspotentiale og grad af dedifferentiering . Progenitorer opnås ved såkaldt direkte omprogrammering eller rettet differentiering og kaldes også inducerede somatiske stamceller .
Tre teknikker er almindeligt anerkendt:
- Transplantation af kerner taget fra somatiske celler til en oocyt (ægcelle), der mangler sin egen kerne (fjernet i laboratoriet)
- Fusion af somatiske celler med pluripotente stamceller og
- Transformation af somatiske celler til stamceller ved anvendelse af det genetiske materiale, der koder for omprogrammering af proteinfaktorer , rekombinante proteiner; microRNA, et syntetisk, selvreplikerende polycistronisk RNA og biologisk aktive stoffer med lav molekylvægt.
Naturlige processer
I 1895 fjernede Thomas Morgan en af en frøs to blastomerer og fandt ud af, at padder er i stand til at danne hele embryoner fra den resterende del. Dette betød, at cellerne kan ændre deres differentieringsvej. I 1924 demonstrerede Spemann og Mangold nøglebetydningen af celle -celleinduktioner under udvikling af dyr. Den reversible transformation af celler af en differentieret celletype til en anden kaldes metaplasi . Denne overgang kan være en del af den normale modningsproces eller forårsaget af en stimulering.
Et eksempel er transformation af irisceller til linseceller i processen med modning og transformation af retinale pigmentepitelceller til den neurale nethinde under regenerering i voksne newt øjne. Denne proces gør det muligt for kroppen at erstatte celler, der ikke er egnede til nye forhold, med mere egnede nye celler. I Drosophila imaginale diske skal celler vælge mellem et begrænset antal standard diskrete differentieringstilstande. Det faktum, at transdetermination (ændring af differentieringsvejen) ofte forekommer for en gruppe af celler frem for enkeltceller, viser, at den fremkaldes snarere end en del af modning.
Forskerne var i stand til at identificere de minimale forhold og faktorer, der ville være tilstrækkelige til at starte kaskaden af molekylære og cellulære processer til at instruere pluripotente celler til at organisere embryoet . De viste, at modstående gradienter af knoglemorfogenetisk protein (BMP) og Nodal , to transformerende vækstfaktor familiemedlemmer, der virker som morfogener , er tilstrækkelige til at fremkalde molekylære og cellulære mekanismer der kræves for at organisere, in vivo eller in vitro , uudnyttede celler i zebrafisk blastula dyrestang til et veludviklet embryo .
Nogle typer modne, specialiserede voksne celler kan naturligt vende tilbage til stamceller. For eksempel udtrykker "chef" -celler stamcellemarkøren Troy. Selvom de normalt producerer fordøjelsesvæsker til maven, kan de vende tilbage til stamceller for at foretage midlertidige reparationer af mavesår, såsom et snit eller beskadigelse som følge af infektion. Desuden kan de foretage denne overgang selv i fravær af mærkbare skader og er i stand til at genopbygge hele maveenheder, som i det væsentlige fungerer som hvilende "reserve" stamceller. Differentierede luftvejsepitelceller kan vende tilbage til stabile og funktionelle stamceller in vivo . Efter skade adskiller modne terminalt differentierede nyreceller sig til mere oprindelige versioner af sig selv og differentierer derefter til celletyperne, der har brug for udskiftning i det beskadigede væv. Makrofager kan selvfornyes ved lokal spredning af modne differentierede celler. I newts regenereres muskelvæv fra specialiserede muskelceller, der dedifferentierer og glemmer den celletype, de havde været. Denne evne til at regenerere falder ikke med alderen og kan være forbundet med deres evne til at fremstille nye stamceller fra muskelceller efter behov.
En række ikke -tumorigene stamceller viser evnen til at generere flere celletyper. For eksempel er multilineage-differentierende stress-varige (Muse) celler stress-tolerante voksne menneskelige stamceller, der kan forny sig selv. De danner karakteristiske celleklynger i suspensionskultur, der udtrykker et sæt gener forbundet med pluripotens og kan differentiere sig til endodermale , ektodermale og mesodermale celler både in vitro og in vivo.
Andre veldokumenterede eksempler på transdifferentiering og deres betydning for udvikling og regenerering blev beskrevet detaljeret.

Inducerede totipotente celler
SCNT-medieret
Inducerede totipotente celler kan opnås ved omprogrammering af somatiske celler med somatisk-cellekerneoverførsel (SCNT). Processen involverer at suge kernen i en somatisk (krops) celle og injicere den i en oocyt, der har fået fjernet sin kerne
Ved hjælp af en tilgang baseret på protokollen skitseret af Tachibana et al., Kan hESC'er genereres af SCNT ved hjælp af dermale fibroblastkerner fra både en midaldrende 35-årig mand og en ældre, 75-årig mand, hvilket tyder på den alder -associerede ændringer er ikke nødvendigvis en hindring for SCNT-baseret nuklear omprogrammering af humane celler. Sådan omprogrammering af somatiske celler til en pluripotent tilstand rummer enorme potentialer for regenerativ medicin . Desværre er de celler, der genereres af denne teknologi, potentielt ikke fuldstændigt beskyttet mod patientens immunsystem (donor af kerner), fordi de har det samme mitokondrielle DNA som en donor af oocytter, i stedet for patientens mitokondrielle DNA. Dette reducerer deres værdi som kilde til autolog stamcelletransplantationsterapi ; hvad angår nærværende, er det ikke klart, om det kan fremkalde en immunreaktion hos patienten ved behandling.
Inducerede androgenetiske haploide embryonale stamceller kan bruges i stedet for sæd til kloning. Disse celler, synkroniseret i M -fase og injiceret i oocytten, kan producere levedygtige afkom.
Denne udvikling, sammen med data om muligheden for ubegrænsede oocytter fra mitotisk aktive reproduktive stamceller, giver mulighed for industriel produktion af transgene husdyr. Gentagen rekloning af levedygtige mus gennem en SCNT -metode, der inkluderer en histondeacetylasehæmmer , trichostatin, tilføjet til cellekulturmediet, viser, at det kan være muligt at reclone dyr på ubestemt tid uden synlig akkumulering af omprogrammering eller genomiske fejl. Forskning i teknologier til udvikle sæd- og ægceller fra stamceller rejser bioetiske spørgsmål.
Sådanne teknologier kan også have vidtrækkende kliniske anvendelser til at overvinde cytoplasmiske defekter i humane oocytter. For eksempel kan teknologien forhindre, at arvelig mitokondriel sygdom overgår til fremtidige generationer. Mitokondrielt genetisk materiale overføres fra mor til barn. Mutationer kan forårsage diabetes, døvhed, øjensygdomme, gastrointestinale lidelser, hjertesygdomme, demens og andre neurologiske sygdomme. Kernen fra et menneskeligt æg er blevet overført til et andet, inklusive dets mitokondrier, hvilket skaber en celle, der kan betragtes som at have to mødre. Æggene blev derefter befrugtet, og de resulterende embryonale stamceller bar det ombyttede mitokondrielle DNA. Som bevis på, at teknikken er sikker, peger forfatteren af denne metode på eksistensen af de raske aber, der nu er mere end fire år gamle - og er et produkt af mitokondrielle transplantationer på tværs af forskellige genetiske baggrunde.
I sen generation telomerase- defekte (Terc-/-) mus reducerer SCNT-medieret omprogrammering telomerdysfunktion og mitokondrielle defekter i større omfang end iPSC-baseret omprogrammering.
Andre kloning og totipotente transformationspræstationer er blevet beskrevet.
Opnået uden SCNT
For nylig lykkedes det nogle forskere at få totipotente celler uden hjælp fra SCNT. Totipotente celler blev opnået ved anvendelse af epigenetiske faktorer, såsom oocyt germinal isoform af histon. Omprogrammering in vivo, ved forbigående induktion af de fire faktorer Oct4, Sox2, Klf4 og c-Myc i mus, giver totipotensfunktioner. Intraperitoneal injektion af sådanne in vivo iPS-celler genererer embryolignende strukturer, der udtrykker embryonale og ekstraembryonale ( trophectodermale ) markører. Udviklingspotentialet for musens pluripotente stamceller til at give både embryonale og ekstra-embryonale slægter kan også udvides med microRNA miR-34a- mangel, hvilket fører til stærk induktion af endogene retrovira MuERV-L (MERVL).
Foryngelse til iPSC'er

iPSc blev først opnået i form af transplanterbart teratocarcinom induceret af transplantater taget fra musembryoner . Teratocarcinom dannet af somatiske celler. Genetisk mosaikmus blev opnået fra maligne teratocarcinomceller, hvilket bekræfter cellernes pluripotens. Det viste sig, at teratocarcinomceller er i stand til at opretholde en kultur af pluripotente embryonale stamceller i en udifferentieret tilstand ved at forsyne kulturmediet med forskellige faktorer. I 1980'erne blev det klart, at transplantation af pluripotente/embryonale stamceller i kroppen hos voksne pattedyr normalt fører til dannelse af teratomer , som derefter kan blive til et ondartet tumorteratocarcinom. Men ved at sætte teratocarcinomceller i embryoet på blastocyststadiet fik de til at blive inkorporeret i den indre cellemasse og frembragte ofte et normalt kimært dyr (dvs. sammensat af celler fra forskellige organismer). Dette indikerede, at årsagen til teratom er en dissonans - gensidig fejlkommunikation mellem unge donorceller og omgivende voksne celler (modtagerens såkaldte " niche ").
I august 2006 omgåede japanske forskere behovet for en oocyt, som i SCNT. Ved at omprogrammere musens embryonale fibroblaster til pluripotente stamceller via ektopisk ekspression af fire transkriptionsfaktorer , nemlig Oct4 , Sox2 , Klf4 og c-Myc , beviste de, at overekspression af et lille antal faktorer kan skubbe cellen til overgang til en ny stabil tilstand, der er forbundet med ændringer i aktiviteten af tusinder af gener.

Omprogrammeringsmekanismer er således forbundet snarere end uafhængige og er centreret om et lille antal gener. IPSC -egenskaber ligner meget ESC'er. iPSC'er har vist sig at understøtte udviklingen af alle iPSC-mus ved hjælp af et tetraploid (4n) embryo, det strengeste assay for udviklingspotentiale. Nogle genetisk normale iPSC'er undlod imidlertid at producere alle-iPSC-mus på grund af afvigende epigenetisk dæmpning af den påtrykte Dlk1-Dio3- genklynge. Et team ledet af Hans Schöler (der opdagede Oct4-genet tilbage i 1989) viste, at overekspression af Oct4 driver massiv genaktivering uden for mål under omprogrammering, forringet kvaliteten af iPSC'er. Sammenlignet med OSKM (4. oktober, Sox2, Klf4 og c-Myc), der viser unormale prægnings- og differentieringsmønstre, genererer SKM (Sox2, Klf4 og c-Myc) omprogrammering iPSC'er med stort udviklingspotentiale (næsten 20 gange højere end OSKM) svarende til embryonale stamceller , som bestemt af deres evne til at generere alle-iPSC-mus gennem tetraploide embryokomplementering.
En vigtig fordel ved iPSC frem for ESC er, at de kan stamme fra voksne celler i stedet for fra embryoner. Derfor bliver det muligt at få iPSC fra voksne og endda ældre patienter.
Omprogrammering af somatiske celler til iPSC'er fører til foryngelse. Det blev fundet, at omprogrammering fører til forlængelse af telomer og efterfølgende afkortning efter deres differentiering tilbage til fibroblastlignende derivater. Således fører omprogrammering til genoprettelse af embryonisk telomerlængde og øger dermed det potentielle antal celledelinger, der ellers er begrænset af Hayflick -grænsen .
På grund af dissonansen mellem foryngede celler og den omgivende niche i modtagerens ældre celler fører indsprøjtningen af hans egen iPSC normalt til et immunrespons , som kan bruges til medicinske formål eller dannelse af tumorer, såsom teratom. En hypotetiseret årsag er, at nogle celler differentieret fra ESC'er og iPSC'er in vivo fortsætter med at syntetisere embryonale proteinisoformer . Så immunsystemet kan opdage og angribe celler, der ikke samarbejder korrekt.
Et lille molekyle kaldet MitoBloCK-6 kan tvinge de pluripotente stamceller til at dø ved at udløse apoptose (via cytokrom c frigivelse over den mitokondriale ydre membran) i humane pluripotente stamceller, men ikke i differentierede celler. Kort efter differentiering blev datterceller resistente over for døden. Da MitoBloCK-6 blev introduceret til differentierede cellelinjer, forblev cellerne raske. Nøglen til deres overlevelse blev antaget at skyldes de ændringer, der gennemgik af pluripotente stamcellemitokondrier i celledifferentieringsprocessen. Denne evne for MitoBloCK-6 til at adskille de pluripotente og differentierede cellelinjer har potentiale til at reducere risikoen for teratomer og andre problemer inden for regenerativ medicin.
I 2012 blev andre små molekyler (selektive cytotoksiske hæmmere af humane pluripotente stamceller - hPSC'er) identificeret, der forhindrede humane pluripotente stamceller i at danne teratomer hos mus. Den mest potente og selektive forbindelse af dem (PluriSIn #1) hæmmer stearoyl-coA-desaturase (nøgleenzymet i oliesyrebiosyntese ), hvilket endelig resulterer i apoptose. Ved hjælp af dette molekyle kan de udifferentierede celler selektivt fjernes fra kultur. En effektiv strategi til selektivt at eliminere pluripotente celler med teratompotentiale er målretning mod pluripotente stamcellespecifikke antiapoptotiske faktorer (dvs. survivin eller Bcl10). En enkelt behandling med kemiske survivin hæmmere (f.eks quercetin eller YM155) kan inducere selektiv og fuldstændig celledød af udifferentierede hPSCs og hævdes at være tilstrækkelig til at forhindre teratom dannelse efter transplantation. Det er imidlertid usandsynligt, at nogen form for foreløbig godkendelse er i stand til at sikre genplantning af iPSC'er eller ESC'er. Efter den selektive fjernelse af pluripotente celler dukker de hurtigt op igen ved at omdanne differentierede celler til stamceller, hvilket fører til tumorer. Dette kan skyldes forstyrrelsen i let-7 regulering af dets mål Nr6a1 (også kendt som kimcelle nuklear faktor -GCNF), en embryonisk transkriptionel repressor af pluripotensgener, der regulerer genekspression i voksne fibroblaster efter tab af mikro-RNA miRNA.
Teratomdannelse af pluripotente stamceller kan være forårsaget af lav aktivitet af PTEN-enzym , rapporteret at fremme overlevelse af en lille population (0,1–5% af den samlede befolkning) af stærkt tumorigene, aggressive, teratom-initierende embryonlignende carcinomceller under differentiering . Overlevelsen af disse teratom-initierende celler er forbundet med mislykket undertrykkelse af Nanog samt en tilbøjelighed til øget glukose- og kolesterolmetabolisme. Disse teratom-initierende celler udtrykte også et lavere forhold på p53/p21 sammenlignet med ikke-tumorigene celler. I forbindelse med ovenstående sikkerhedsproblemer er brugen af iPSC'er til celleterapi stadig begrænset. De kan dog bruges til en række andre formål, herunder modellering af sygdom, screening (selektiv selektion) af lægemidler og test af toksicitet af forskellige lægemidler.
Vævet vokset fra iPSC'er, placeret i de "kimære" embryoner i de tidlige stadier af musens udvikling, forårsager praktisk talt ikke et immunrespons (efter at embryoerne er vokset til voksne mus) og er egnede til autolog transplantation Samtidig er fuld omprogrammering af voksne celler in vivo i væv ved forbigående induktion af de fire faktorer Oct4, Sox2, Klf4 og c-Myc i mus resulterer i, at der kommer teratomer fra flere organer. Endvidere viser delvis omprogrammering af celler mod pluripotens in vivo hos mus, at ufuldstændig omprogrammering medfører epigenetiske ændringer (mislykket undertrykkelse af Polycomb -mål og ændret DNA -methylering ) i celler, der driver kræftudvikling. Imidlertid formåede en række forskere senere at udføre cyklisk delvis omprogrammering in vivo ved udtryk for Yamanaka -faktorerne i en kort periode uden efterfølgende kræftfremkaldelse og dermed delvis forynge og forlænge levetiden i progeroidmus. Med in vitro -metode, der anvender lidt længere perioder med omprogrammering (til væsentligt foryngelse) mister celler midlertidigt deres celleidentitet, men "genvinder deres oprindelige somatiske skæbne, når omprogrammeringsfaktorerne trækkes tilbage".
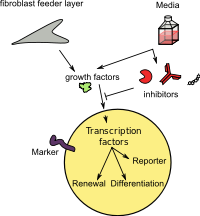
Kemisk fremkaldelse
Ved hjælp af udelukkende små molekyler demonstrerede Deng Hongkui og kolleger, at endogene "mestergener" er nok til omprogrammering af cellernes skæbne. De inducerede en pluripotent tilstand i voksne celler fra mus ved hjælp af syv småmolekyleforbindelser. Metodens effektivitet er ret høj: den var i stand til at konvertere 0,02% af de voksne vævsceller til iPSC'er, hvilket kan sammenlignes med genindsættelsesomdannelsesfrekvensen. Forfatterne bemærker, at musene genereret fra CiPSC'er var "100% levedygtige og tilsyneladende sunde i op til 6 måneder". Så denne kemiske omprogrammeringsstrategi har potentiel anvendelse til at generere funktionelle ønskelige celletyper til kliniske anvendelser.
I 2015 blev der etableret et robust kemisk omprogrammeringssystem med et udbytte op til 1.000 gange større end i den tidligere rapporterede protokol. Så kemisk omprogrammering blev en lovende tilgang til at manipulere celleskæbner.
Differentiering fra induceret teratom
Den kendsgerning, at menneskelige iPSC'er er i stand til at danne teratomer ikke kun hos mennesker, men også i nogle dyr, især mus eller svin, tillod forskere at udvikle en metode til differentiering af iPSC'er in vivo. Til dette formål injiceres iPSC'er med et middel til at inducere differentiering i målceller til en genetisk modificeret gris eller mus, der har undertrykt immunsystemaktivering på humane celler. Det dannede teratom skæres ud og bruges til isolering af de nødvendige differentierede humane celler ved hjælp af monoklonalt antistof mod vævsspecifikke markører på overfladen af disse celler. Denne metode er med succes blevet brugt til produktion af funktionelle myeloid-, erythroid- og lymfoide humane celler, der er egnede til transplantation (endnu kun til mus). Mus indgraveret med humane iPSC-teratom-afledte hæmatopoietiske celler producerede humane B- og T-celler, der var i stand til funktionelle immunresponser. Disse resultater giver håb om, at in vivo -generering af patienttilpassede celler er mulig, hvilket giver materialer, der kan være nyttige til transplantation, human antistofdannelse og applikationer til screening af lægemidler. Ved hjælp af MitoBloCK-6 og/eller PluriSIn # 1 kan de differentierede stamceller renses yderligere fra teratomdannende pluripotente celler. Det faktum, at differentieringen finder sted, selv i teratomnichen, giver håb om, at de resulterende celler er tilstrækkeligt stabile til at stimuli kan forårsage deres overgang tilbage til den dedifferentierede (pluripotente) tilstand og derfor sikre. Et lignende in vivo-differentieringssystem, der giver engraftable hæmatopoietiske stamceller fra mus og humane iPSC'er i teratombærende dyr i kombination med en manøvre for at lette hæmatopoiesis, blev beskrevet af Suzuki et al. De bemærkede, at hverken leukæmi eller tumorer blev observeret hos modtagere efter intravenøs injektion af iPSC-afledte hæmatopoietiske stamceller i bestrålede modtagere. Desuden resulterede denne injektion i multilineage og langsigtet rekonstituering af det hæmatolymfopoietiske system ved serielle overførsler. Et sådant system tilvejebringer et nyttigt værktøj til praktisk anvendelse af iPSC'er til behandling af hæmatologiske og immunologiske sygdomme.
For yderligere udvikling af denne metode skal dyr (såsom mus), hvor det humane celletransplantat dyrkes, have modificeret genom, så alle dets celler udtrykker og har menneskelige SIRPa på overfladen . For at forhindre afstødning efter transplantation til patienten af det allogene organ eller væv, der er vokset fra de pluripotente stamceller in vivo i dyret, bør disse celler udtrykke to molekyler: CTLA4-Ig , som forstyrrer T-celles costimulatoriske veje og PD-L1 , som aktiverer T -cellehæmmende vej.
Se også: US 20130058900 patent.
Differentierede celletyper
Retinale celler
I den nærmeste fremtid vil kliniske forsøg, der er designet til at demonstrere sikkerheden ved brug af iPSC'er til celleterapi af mennesker med aldersrelateret makuladegeneration, en sygdom, der forårsager blindhed gennem skader på nethinden, begynde. Der er flere artikler, der beskriver metoder til fremstilling af nethindeceller fra iPSC'er, og hvordan de bruges til celleterapi. Rapporter om iPSC-afledt retinalpigmenteret epiteltransplantation viste forbedret visuelt styret adfærd hos forsøgsdyr i 6 uger efter transplantation. Imidlertid har kliniske forsøg været en succes: ti patienter, der lider af retinitis pigmentosa, har fået synet genoprettet, herunder en kvinde, der kun havde 17 procent af sit syn tilbage.
Lunge- og luftvejsepitelceller
Kroniske lungesygdomme, såsom idiopatisk lungefibrose og cystisk fibrose eller kronisk obstruktiv lungesygdom og astma , er førende årsager til sygelighed og dødelighed på verdensplan med en betydelig menneskelig, samfundsmæssig og økonomisk byrde. Derfor er der et presserende behov for effektiv celleterapi og lunge vævsmanipulering . Flere protokoller er blevet udviklet til generering af de fleste celletyper i luftvejene , hvilket kan være nyttigt til at udlede patientspecifikke terapeutiske celler.
Reproduktive celler
Nogle linjer af iPSC'er har potentiale til at differentiere sig til mandlige kønsceller og oocytlignende celler i en passende niche (ved dyrkning i retinsyre og porcint follikulært væskedifferentieringsmedium eller seminiferous tubulatransplantation). Desuden bidrager iPSC -transplantation til at reparere testiklerne hos ufrugtbare mus, hvilket demonstrerer potentialet for gametafledning fra iPSC'er in vivo og in vitro.
Fremkaldte stamceller fra stamceller
Direkte transdifferentiering
Risikoen for kræft og tumorer skaber behov for at udvikle metoder til sikrere cellelinjer, der er egnede til klinisk brug. En alternativ tilgang er såkaldt "direkte omprogrammering"-transdifferentiering af celler uden at passere gennem pluripotent tilstand. Grundlaget for denne fremgangsmåde var, at 5-azacytidin -et DNA-demethyleringsreagens-kan forårsage dannelse af myogene , chondrogene og adipogeni-kloner i en udødelig cellelinie af mus embryonale fibroblaster, og at aktiveringen af et enkelt gen, senere kaldet MyoD1, er tilstrækkelig til en sådan omprogrammering. Sammenlignet med iPSC'er, hvis omprogrammering kræver mindst to uger, sker dannelsen af inducerede stamceller undertiden inden for få dage, og effektiviteten af omprogrammering er normalt mange gange højere. Denne omprogrammering kræver ikke altid celledeling. Cellerne som følge af en sådan omprogrammering er mere egnede til celleterapi, fordi de ikke danner teratomer. F.eks. Beskriver Chandrakanthan et al., & Pimanda dannelsen af vævsregenerative multipotente stamceller (iMS-celler) ved at behandle modne knogle- og fedtceller forbigående med en vækstfaktor ( trombocyt-afledt vækstfaktor -AB (PDGF-AB)) og 5-Azacytidin. Disse forfattere udtaler, at "I modsætning til primære mesenkymale stamceller, der bruges med få objektive beviser i klinisk praksis til at fremme vævsreparation, bidrager iMS-celler direkte til in vivo vævsregenerering på en kontekstafhængig måde uden at danne tumorer" og dermed "har signifikant anvendelsesområde for vævsregenerering ".
Enkelt transkriptionsfaktortransdifferentiering
Oprindeligt kunne kun tidlige embryonale celler lokkes til at ændre deres identitet. Modne celler er modstandsdygtige over for at ændre deres identitet, når de har forpligtet sig til en bestemt slags. Imidlertid kan kort udtryk for en enkelt transkriptionsfaktor, ELT-7 GATA-faktoren, konvertere identiteten af fuldt differentierede, specialiserede ikke-endodermale celler i svælget til fuldt differentierede tarmceller i intakte larver og voksne rundorm Caenorhabditis elegans uden krav om en dedifferentieret mellemprodukt.
Transdifferentiering med CRISPR-medieret aktivator
Celleskæbnen kan effektivt manipuleres ved epigenomredigering , især via direkte aktivering af specifik endogen genekspression med CRISPR -medieret aktivator. Når dCas9 (som er blevet modificeret, så det ikke længere skærer DNA, men stadig kan ledes til specifikke sekvenser og bindes til dem) kombineres med transkriptionsaktivatorer, kan det præcist manipulere endogent genekspression. Ved hjælp af denne metode forbedrede Wei et al. Ekspressionen af endogene Cdx2- og Gata6- gener ved hjælp af CRISPR-medierede aktivatorer, hvilket direkte konverterede musens embryonale stamceller til to ekstraembryoniske slægter, dvs. typiske trofoblast-stamceller og ekstraembryoniske endodermceller. En analog fremgangsmåde blev anvendt til at inducere aktivering af de endogene Brn2-, Ascl1- og Myt1l -gener til at omdanne embryonale fibroblaster fra mus til inducerede neuronale celler. Således er transkriptionel aktivering og epigenetisk ombygning af endogene master -transkriptionsfaktorer tilstrækkelige til konvertering mellem celletyper. Den hurtige og vedvarende aktivering af endogene gener i deres native kromatinkontekst ved denne fremgangsmåde kan lette omprogrammering med forbigående metoder, der undgår genomisk integration og giver en ny strategi til at overvinde epigenetiske barrierer for celleskæbnespecifikation.
Stadig procesmodellerende regenerering
En anden måde at omprogrammere er simulering af processer, der opstår under regenerering af amfibier . I urodele padder er et tidligt trin i regenerering af lemmer skeletmuskelfiberdedifferentiering til et cellulat, der formerer sig til lemvæv. Imidlertid sekventiel lille molekyle behandling af musklen fiber med myoseverin, reversine (den aurora B kinase inhibitor), og nogle andre kemikalier (BIO (glycogensyntase-3-kinase inhibitor), lysophosphatidsyre (pleiotropisk aktivator af G-protein-koblede receptorer) , SB203580 ( p38 MAP kinasehæmmer ) eller SQ22536 (adenylylcyclasehæmmer)) forårsager dannelse af nye muskelcelletyper såvel som andre celletyper, såsom forstadier til fedt-, knogle- og nervesystemceller.
Antistofbaseret transdifferentiering
Forskerne opdagede, at GCSF -efterlignende antistof kan aktivere en vækststimulerende receptor på marvceller på en måde, der inducerer marvstamceller, der normalt udvikler sig til hvide blodlegemer, til at blive neurale stamceller. Teknikken gør det muligt for forskere at søge i store biblioteker med antistoffer og hurtigt vælge dem med en ønsket biologisk effekt.
Omprogrammering af bakterier
Menneskets mave -tarmkanal er koloniseret af et stort fællesskab af symbionter og kommensaler. Forskerne demonstrerer fænomenet somatisk omprogrammering af bakterier og dannelse af multipotentiale celler fra voksne humane dermale fibroblastceller ved at inkorporere mælkesyrebakterier Denne cellulære transdifferentiering skyldes ribosomer og "kan forekomme via donorbakterier, der sluges og fordøjes af værtsceller, som kan fremkalde ribosomal stress og stimulere cellulær udviklingsmæssig plasticitet ".
Betinget omprogrammerede celler
Schlegel og Liu demonstrerede, at kombinationen af føderceller og en Rho kinasehæmmer (Y-27632) inducerer normale og tumorepitelceller fra mange væv til at formeres på ubestemt tid in vitro. Denne proces sker uden behov for transduktion af eksogene virale eller cellulære gener. Disse celler er blevet betegnet "betinget omprogrammerede celler (CRC)". Induktionen af CRC'er er hurtig og skyldes omprogrammering af hele cellepopulationen. CRC'er udtrykker ikke høje niveauer af proteiner, der er karakteristiske for iPSC'er eller embryonale stamceller (ESC'er) (f.eks. Sox2, Oct4, Nanog eller Klf4). Denne induktion af CRC'er er reversibel, og fjernelse af Y-27632 og feeders gør det muligt for cellerne at differentiere normalt. CRC teknologi kan generere 2 x 10 6 celler i 5 til 6 dage fra nålebiopsier og kan generere kulturer fra kryopræserveret væv og fra færre end fire levedygtige celler. CRC'er bevarer en normal karyotype og forbliver ikke -tumorigene. Denne teknik etablerer også effektivt cellekulturer fra humane tumorer og gnavere.
Evnen til hurtigt at generere mange tumorceller fra små biopsiprøver og frosset væv giver betydelige muligheder for cellebaseret diagnostik og terapi (herunder kemosensitivitetstest) og udvider i høj grad værdien af biobank. Ved hjælp af CRC -teknologi kunne forskere identificere en effektiv terapi til en patient med en sjælden type lungetumor. Engleman's gruppe beskriver en farmakogenomisk platform, der letter hurtig opdagelse af lægemiddelkombinationer, der kan overvinde resistens ved hjælp af CRC -system. Derudover tillader CRC -metoden den genetiske manipulation af epitelceller ex vivo og deres efterfølgende evaluering in vivo i den samme vært. Mens indledende undersøgelser afslørede, at co-dyrkning af epitelceller med schweiziske 3T3-celler J2 var afgørende for CRC-induktion, med transwellkulturplader, er fysisk kontakt mellem foderautomater og epitelceller ikke påkrævet for at inducere CRC'er og endnu vigtigere, bestråling af fødercellerne er påkrævet for denne induktion. I overensstemmelse med transwellforsøgene inducerer og vedligeholder konditioneret medium CRC'er, som ledsages af en samtidig stigning i cellulær telomeraseaktivitet. Aktiviteten af det konditionerede medium korrelerer direkte med strålingsinduceret fødercelle-apoptose. Således medieres betinget omprogrammering af epitelceller af en kombination af Y-27632 og en eller flere opløselige faktorer frigivet af apoptotiske føderceller.
Riegel et al. demonstrere, at mus-ME-celler, isoleret fra normale brystkirtler eller fra mus-brysttumorvirus (MMTV) -Neu-inducerede brysttumorer, kan dyrkes på ubestemt tid som betinget omprogrammerede celler (CRC'er). Celleoverfladeforfaderassocierede markører induceres hurtigt i normale mus-ME-CRC'er i forhold til ME-celler. Imidlertid falder ekspressionen af visse mælkeforfader -subpopulationer, såsom CD49f+ ESA+ CD44+, betydeligt i senere passager. Ikke desto mindre gav ME-CRC'er fra mus, der blev dyrket i en tredimensionel ekstracellulær matrix, anledning til mammære acinarstrukturer. ME-CRC'er isoleret fra MMTV-Neu transgene musebrysttumorer udtrykker høje niveauer af HER2/neu samt tumorinitierende cellemarkører, såsom CD44+, CD49f+og ESA+(EpCam). Disse udtryksmønstre opretholdes i senere CRC -passager. Tidlig og sen passage ME-CRC'er fra MMTV-Neu-tumorer, der blev implanteret i mælkefedtpuderne hos syngene eller nøgne mus, udviklede vaskulære tumorer, der metastaserede inden for 6 uger efter transplantation. Det er vigtigt, at histopatologien for disse tumorer ikke kunne skelnes fra forældretumoren, der udvikler sig i MMTV-Neu-musene. Anvendelse af CRC -systemet på muse -brystepitelceller giver et attraktivt modelsystem til at studere genetik og fænotype af normalt og transformeret musepitel i et defineret kulturmiljø og i in vivo -transplantationsundersøgelser.
En anden tilgang til CRC er at hæmme CD47 -et membranprotein, der er thrombospondin-1- receptoren. Tab af CD47 tillader vedvarende spredning af primære murine endotelceller, øger asymmetrisk division og gør det muligt for disse celler at spontant omprogrammere til dannelse af multipotente embryoide kropslignende klynger. CD47-knockdown øger akut mRNA- niveauer af c-Myc og andre stamcelletranskriptionsfaktorer i celler in vitro og in vivo. Thrombospondin-1 er et vigtigt miljømæssigt signal, der hæmmer stamcellens selvfornyelse via CD47. Således muliggør CD47-antagonister cellens selvfornyelse og omprogrammering ved at overvinde negativ regulering af c-Myc og andre stamcelletranskriptionsfaktorer. In vivo-blokade af CD47 ved hjælp af en antisense morpholino øger overlevelsen af mus udsat for dødelig total kropsbestråling på grund af øget proliferationskapacitet af knoglemarvsafledte celler og radiobeskyttelse af radiosensitive gastrointestinale væv.
Slægtsspecifikke forstærkere
Differentierede makrofager kan selvfornyes i væv og ekspandere langsigtet i kultur. Under visse betingelser kan makrofager dele sig uden at miste funktioner, de har erhvervet, mens de specialiserer sig i immunceller - hvilket normalt ikke er muligt med differentierede celler . Makrofagerne opnår dette ved at aktivere et gennetværk, der ligner et, der findes i embryonale stamceller. Enkeltcelleanalyse afslørede, at in vivo , prolifererende makrofager kan deprimere et makrofag-specifikt forstærkerrepertoire forbundet med et gennetværk, der styrer selvfornyelse. Dette skete, da koncentrationer af to transkriptionsfaktorer ved navn MafB og c-Maf var naturligt lave eller blev hæmmet i kort tid. Genetiske manipulationer, der slukkede MafB og c-Maf i makrofagerne, fik cellerne til at starte et selvfornyelsesprogram. Det lignende netværk styrer også embryonale stamcelles selvfornyelse, men er forbundet med forskellige embryonale stamcellespecifikke forstærkere.
Derfor deler makrofager isoleret fra MafB- og c-Maf-dobbelt-mangelfulde mus sig på ubestemt tid; selvfornyelsen afhænger af c-Myc og Klf4 .
Indirekte slægtskonvertering
Indirekte slægtskonvertering er en omprogrammeringsmetode, hvor somatiske celler overgår gennem en plastisk mellemliggende tilstand af delvist omprogrammerede celler (præ-iPSC), induceret af kort eksponering for omprogrammeringsfaktorer efterfulgt af differentiering i et specielt udviklet kemisk miljø (kunstig niche).
Denne metode kunne være både mere effektiv og sikrere, da den ikke synes at producere tumorer eller andre uønskede genetiske ændringer og resulterer i meget større udbytte end andre metoder. Imidlertid er sikkerheden ved disse celler fortsat tvivlsom. Da slægtskonvertering fra pre-iPSC er afhængig af brugen af iPSC-omprogrammeringsbetingelser, kunne en brøkdel af cellerne erhverve pluripotente egenskaber, hvis de ikke stopper de-differentieringsprocessen in vitro eller på grund af yderligere de-differentiering in vivo.
Ydermembran glycoprotein
Et fælles træk ved pluripotente stamceller er den særlige karakter af protein glycosylering af deres ydre membran. Det adskiller dem fra de fleste ikke -pluripotente celler, men ikke fra hvide blodlegemer . De glycaner ved for- celleoverfladen reagere hurtigt på ændringer i cellulær tilstand og signalering og er derfor velegnede til at identificere selv mindre ændringer i cellepopulationer. Mange stamcellemarkører er baseret på glycanepitoper på celleoverfladen, herunder de meget udbredte markører SSEA-3 , SSEA-4, Tra 1-60 og Tra 1-81. Suila Heli et al. spekulere i, at i humane stamceller spiller ekstracellulær O-GlcNAc og ekstracellulær O-LacNAc en afgørende rolle i finjusteringen af Notch-signalvejen -et stærkt konserveret cellesignalsystem, der regulerer celleskæbnespecifikation, differentiering, venstre-højre asymmetri, apoptose, somitogenese og angiogenese og spiller en central rolle i stamcelleproliferation (gennemgået af Perdigoto og Bardin og Jafar-Nejad et al.)
Ændringer i ydre membranprotein -glykosylering er markører for celletilstande, der på en eller anden måde er forbundet med pluripotens og differentiering. Glykosyleringsændringen er tilsyneladende ikke kun resultatet af initialiseringen af genekspression, men fungerer også som en vigtig genregulator, der er involveret i erhvervelse og vedligeholdelse af den udifferentierede tilstand.
For eksempel inducerer aktivering af glycoprotein ACA, der forbinder glycosylphosphatidylinositol på overfladen af stamcellerne i humant perifert blod, øget ekspression af gener Wnt , Notch-1 , BMI1 og HOXB4 gennem en signalkaskade PI3K / Akt / mTor / PTEN og fremmer dannelsen af en selvfornyende population af hæmatopoietiske stamceller.
Desuden fører dedifferentiering af stamceller induceret af ACA-afhængig signalvej til ACA-inducerede pluripotente stamceller, der er i stand til at differentiere in vitro til celler i alle tre kimlag . Undersøgelsen af lectins evne til at opretholde en kultur af pluripotente humane stamceller har ført til opdagelsen af lectin Erythrina crista-galli (ECA), som kan tjene som en enkel og yderst effektiv matrix til dyrkning af humane pluripotente stamceller.
Omprogrammering med en proteoglycan
En alternativ strategi til at konvertere somatiske celler til pluripotente tilstande kan være kontinuerlig stimulering af fibroblaster med et enkelt ECM proteoglycan , fibromodulin . Sådanne celler udviser evne til skeletmuskulaturgenerering med markant lavere tumorigent risiko sammenlignet med iPSC'er. Den nedsatte tumorigenicitet af sådanne celler er relateret til CDKN2B -opregulering under den rekombinante humane fibromodulin -omprogrammeringsproces
Omprogrammering gennem en fysisk tilgang
Celleadhæsionsprotein E-cadherin er uundværligt for en robust pluripotent fænotype . Under omprogrammering til iPS-cellegenerering kan N-cadherin erstatte funktionen af E-cadherin. Disse funktioner af cadheriner er ikke direkte relateret til vedhæftning, fordi kuglemorfologi hjælper med at opretholde stamcellernes "stilhed". Desuden inducerer kugledannelse på grund af tvungen vækst af celler på en lav vedhæftningsflade undertiden omprogrammering. For eksempel kan neurale stamceller genereres fra fibroblaster direkte gennem en fysisk tilgang uden at indføre eksogene omprogrammeringsfaktorer.
Fysiske signaler, i form af parallelle mikrospor på overfladen af celleadhæsive substrater, kan erstatte virkningerne af småmolekylære epigenetiske modifikatorer og forbedre omprogrammeringseffektiviteten betydeligt. Mekanismen bygger på mekanomodulation af cellernes epigenetiske tilstand. Specifikt fører "nedsat histondeacetylaseaktivitet og opregulering af ekspressionen af WD repeat -domæne 5 (WDR5) - en underenhed af H3 -methyltranferase - af mikro -rillede overflader til øget histon -H3 -acetylering og methylering". Nanofibre stilladser med justeret fiberorientering frembringer effekter, der ligner dem, der produceres af mikrospor, hvilket tyder på, at ændringer i cellemorfologi kan være ansvarlig for modulering af den epigenetiske tilstand.

Substratstivhed er en vigtig biofysisk cue, der påvirker neural induktion og subtype -specifikation. For eksempel bløde substrater fremme neuroepitel omdannelse mens inhibering neuralkam differentiering af hESCs i en BMP4 -afhængig måde. Mekanistiske undersøgelser afslørede en multimålrettet mekanotransduktiv proces, der involverer mekanosensitiv Smad- phosphorylering og nukleocytoplasmatisk shuttling, reguleret af stivhedsafhængige Hippo / YAP- aktiviteter og actomyosin- cytoskelet- integritet og kontraktilitet .
Musens embryonale stamceller (mESC'er) undergår selvfornyelse i nærvær af den cytokin leukæmi hæmmende faktor (LIF). Efter LIF tilbagetrækning, mESCs differentiere, ledsaget af en stigning i celle-substrat adhæsion og cellespredning. Begrænset cellespredning i fravær af LIF ved enten at dyrke mESC'er på kemisk definerede, svagt klæbende biosubstrater eller ved at manipulere cytoskelet , tillod cellerne at forblive i en udifferentieret og pluripotent tilstand. Effekten af begrænset cellespredning på mESC-selvfornyelse medieres ikke af øget intercellulær adhæsion, da hæmning af mESC-adhæsion ved hjælp af en funktion, der blokerer anti-E-cadherin-antistof eller siRNA , ikke fremmer differentiering. Mulige mekanismer for stamcelles skæbne forudbestemmelse ved fysiske interaktioner med den ekstracellulære matrix er blevet beskrevet.
En ny metode er blevet udviklet, der gør celler til stamceller hurtigere og mere effektivt ved at 'klemme' dem ved hjælp af 3D -mikromiljøstivhed og densitet af den omgivende gel. Teknikken kan anvendes på et stort antal celler til fremstilling af stamceller til medicinske formål i industriel skala.
Celler involveret i omprogrammeringsprocessen ændres morfologisk, efterhånden som processen skrider frem. Dette resulterer i fysiske forskelle i klæbekræfter mellem celler. Væsentlige forskelle i 'klæbende signatur' mellem pluripotente stamceller, delvist omprogrammerede celler, differentierede afkom og somatiske celler muliggjorde udviklingen af separationsproces til isolering af pluripotente stamceller i mikrofluidiske enheder , som er:
- hurtig (adskillelse tager mindre end 10 minutter);
- effektiv (adskillelse resulterer i en mere end 95 procent ren iPS -cellekultur);
- uskadelig (celleoverlevelsesrate er større end 80 procent, og de resulterende celler bevarer normale transkriptionelle profiler, differentieringspotentiale og karyotype).
Stamceller besidder mekanisk hukommelse (de husker tidligere fysiske signaler) -med Hippo-signalvejen faktorer: Ja-associeret protein (YAP) og transkriptionel koaktivator med PDZ-bindende domæne (TAZ), der fungerer som en intracellulær mekanisk reostat-der gemmer information fra fortiden fysiske miljøer og påvirker cellernes skæbne.
Neurale stamceller
Hjerteslag og mange neurodegenerative lidelser, såsom Parkinsons sygdom, Alzheimers sygdom og amyotrofisk lateral sklerose, har brug for celleerstatningsterapier. Den vellykkede brug af konverterede neurale celler (cN'er) i transplantationer åbner en ny vej til behandling af sådanne sygdomme. Ikke desto mindre er inducerede neuroner (iN'er) direkte konverteret fra fibroblaster terminalt engagerede og udviser meget begrænset proliferationsevne, der muligvis ikke giver nok autologe donorceller til transplantation. Selvfornyende inducerede neurale stamceller (iNSC'er) giver yderligere fordele i forhold til iN'er til både grundforskning og kliniske anvendelser.
For eksempel under særlige vækstbetingelser kan musfibroblaster omprogrammeres med en enkelt faktor, Sox2, for at danne iNSC'er, der fornyer sig selv i kultur og efter transplantation og kan overleve og integrere uden at danne tumorer i musens hjerner. INSC'er kan stammer fra voksne humane fibroblaster ved ikke-virale teknikker og tilbyder således en sikker metode til autolog transplantation eller til udvikling af cellebaserede sygdomsmodeller.
Neurale kemisk inducerede progenitorceller (ciNPC'er) kan genereres fra mushale fibroblaster og humane urinære celler uden at indføre eksogene faktorer, men - ved en kemisk cocktail, nemlig VCR (V, VPA , en hæmmer af HDAC'er ; C, CHIR99021, en hæmmer af GSK-3 kinaser og R, RepSox , en hæmmer af TGF beta-signalveje ), under en fysiologisk hypoksisk tilstand . Alternative cocktails med hæmmere af histondeacetylering, glycogensyntasekinase og TGF-β-veje (hvor: natriumbutyrat (NaB) eller Trichostatin A (TSA) kan erstatte VPA, Lithiumchlorid (LiCl) eller lithiumcarbonat (Li2CO3) kan erstatte CHIR99021 eller Repsox kan udskiftes med SB-431542 eller Tranilast ) viser lignende virkninger for ciNPC-induktion. Zhang, et al., Rapporterer også om meget effektiv omprogrammering af musefibroblaster til inducerede neurale stamcellelignende celler (ciNSLC'er) ved hjælp af en cocktail af ni komponenter.
Flere metoder til direkte transformation af somatiske celler til inducerede neurale stamceller er blevet beskrevet.
Principeksperimenter viser, at det er muligt at konvertere transplanterede humane fibroblaster og menneskelige astrocytter direkte i hjernen, der er konstrueret til at udtrykke inducerbare former for neurale omprogrammeringsgener, til neuroner, når omprogrammeringsgener ( Ascl1 , Brn2a og Myt1l ) aktiveres efter transplantation brug af et lægemiddel.
Astrocytter - de mest almindelige neurogliale hjerneceller, som bidrager til ardannelse som reaktion på skade - kan omprogrammeres direkte in vivo for at blive funktionelle neuroner, der danner netværk i mus uden behov for celletransplantation. Forskerne fulgte musene i næsten et år for at lede efter tegn på tumordannelse og rapporterede at finde ingen. De samme forskere har forvandlet ardannende astrocytter til stamceller, kaldet neuroblaster, der regenererede til neuroner i den skadede voksne rygmarv.
Oligodendrocyt -precursorceller
Uden myelin til at isolere neuroner mister nervesignaler hurtigt strøm. Sygdomme, der angriber myelin, såsom multipel sklerose, resulterer i nervesignaler, der ikke kan forplante sig til nerveender og som følge heraf føre til kognitive, motoriske og sensoriske problemer. Transplantation af oligodendrocyt -precursorceller (OPC'er), som med succes kan skabe myelinskeder omkring nerveceller, er en lovende potentiel terapeutisk reaktion. Direkte slægtskonvertering af mus- og rottefibroblaster til oligodendroglialceller giver en potentiel kilde til OPC'er. Omdannelse ved tvungen ekspression af både otte eller af de tre transkriptionsfaktorer Sox10, Olig2 og Zfp536 kan give sådanne celler.
Kardiomyocytter
Cellebaserede in vivo-terapier kan tilvejebringe en transformativ tilgang til at øge vaskulær og muskelvækst og forhindre ikke-kontraktil ardannelse ved at levere transkriptionsfaktorer eller mikroRNA'er til hjertet. Hjertefibroblaster, der repræsenterer 50% af cellerne i pattedyrets hjerte, kan omprogrammeres til kardiomyocytlignende celler in vivo ved lokal levering af hjertekerntranskriptionsfaktorer (GATA4, MEF2C, TBX5 og til forbedret omprogrammering plus ESRRG, MESP1, Myocardin og ZFPM2) efter koronar ligering . Disse resultater indebar terapier, der direkte kan remuscularisere hjertet uden celletransplantation. Effektiviteten af en sådan omprogrammering viste sig imidlertid at være meget lav, og fænotypen af modtagne kardiomyocytlignende celler ligner ikke en moden normal kardiomyocyt. Endvidere resulterede transplantation af hjertetranskriptionsfaktorer i skadede murine hjerter i dårlig celleoverlevelse og minimal ekspression af hjertegener.
I mellemtiden skete der fremskridt inden for metoderne til opnåelse af myocytter in vitro. Effektiv hjertedifferentiering af humane iPS -celler gav anledning til forfædre, der blev tilbageholdt i infarktede rottehjerter og reduceret ombygning af hjertet efter iskæmisk skade.
Forskerteamet, ledet af Sheng Ding, brugte en cocktail af ni kemikalier (9C) til transdifferentiering af menneskelige hudceller til bankende hjerteceller. Med denne metode begyndte mere end 97% af cellerne at slå, en egenskab ved fuldt udviklede, raske hjerteceller. De kemisk inducerede kardiomyocytlignende celler (ciCM'er) kontraherede ensartet og lignede humane kardiomyocytter i deres transkriptome, epigenetiske og elektrofysiologiske egenskaber. Når de blev transplanteret i infarktede musehjerter, blev 9C-behandlede fibroblaster effektivt konverteret til ciCM'er og udviklet til sunde hjertemuskelceller i organet. Denne kemiske omprogrammeringsmetode, efter yderligere optimering, kan tilbyde en let måde at give de tegn, der får hjertemusklen til at regenerere lokalt.
I en anden undersøgelse blev iskæmisk kardiomyopati i murineinfarktmodellen målrettet af iPS -celletransplantation. Det synkroniserede svigtende ventrikler og tilbyder en regenerativ strategi for at opnå resynkronisering og beskyttelse mod dekompensation ved hjælp af forbedret ledning og kontraktilitet i venstre ventrikel, reduceret ardannelse og vending af strukturel ombygning. En protokol genererede populationer på op til 98% kardiomyocytter fra hPSC'er blot ved at modulere den kanoniske Wnt -signalvej på bestemte tidspunkter under differentiering ved hjælp af let tilgængelige små molekylforbindelser.
Opdagelse af de mekanismer, der styrer dannelsen af kardiomyocytter, førte til udviklingen af lægemidlet ITD-1, som effektivt rydder celleoverfladen fra TGF-β- receptor type II og selektivt hæmmer intracellulær TGF-β-signalering. Det forbedrer således selektivt differentieringen af uforpligtende mesoderm til kardiomyocytter, men ikke til vaskulære glatte muskler og endotelceller.
Et projekt podede decellulariserede musehjerter med humane iPSC-afledte multipotentielle kardiovaskulære stamceller. De introducerede celler migrerede, formerede og differentierede in situ til cardiomyocytter, glatte muskelceller og endotelceller for at rekonstruere hjerterne. Desuden signalerede hjertets ekstracellulære matrix (hjertestillets substrat) de menneskelige celler til at blive de specialiserede celler, der er nødvendige for korrekt hjertefunktion. Efter 20 dages perfusion med vækstfaktorer begyndte de konstruerede hjertevæv at slå igen og reagerede på lægemidler.
Omprogrammering af hjertefibroblaster til inducerede kardiomyocytlignende celler (iCM'er) in situ repræsenterer en lovende strategi for hjerteregenerering. Mus udsat in vivo for tre hjerte-transkriptionsfaktorer GMT (Gata4, Mef2c, Tbx5) og de små molekyler: SB-431542 (den transformerende vækstfaktor (TGF) -β-hæmmer) og XAV939 (WNT-hæmmeren) i 2 uger efter myokardieinfarkt viste signifikant forbedret omprogrammering (omprogrammeringseffektivitet øget otte gange) og hjertefunktion sammenlignet med dem, der kun blev udsat for GMT.
Se også: anmeldelse
Foryngelse af muskelstamcellen
De ældre lider ofte af progressiv muskelsvaghed og regenerativ svigt, dels på grund af forhøjet aktivitet af p38α- og p38β-mitogenaktiverede kinasestien i senescerende skeletmuskelstamceller. Underkastelse af sådanne stamceller til forbigående inhibering af p38α og p38β i forbindelse med kultur på bløde hydrogel -substrater ekspanderer og forynger dem hurtigt, hvilket resulterer i tilbagevenden af deres styrke.
Hos geriatriske mus mister hvilende satellitceller reversibel hviletid ved at skifte til en irreversibel tilstand før ældning, forårsaget af derepression af p16 INK4a (også kaldet Cdkn2a). Ved skade undlader disse celler at aktivere og ekspandere, selv i et ungdommeligt miljø. p16INK4a -dæmpning i geriatriske satellitceller genopretter ro og muskelregenerative funktioner.
Myogene forfædre til potentiel anvendelse i sygdomsmodellering eller cellebaserede terapier målrettet mod skeletmuskulatur kan også genereres direkte fra inducerede pluripotente stamceller ved hjælp af frit svævende sfærisk kultur (EZ-kugler) i et kulturmedium suppleret med høje koncentrationer (100 ng/ml) af fibroblastvækstfaktor-2 ( FGF-2 ) og epidermal vækstfaktor .
Hepatocytter
I modsætning til nuværende protokoller til afledning af hepatocytter fra humane fibroblaster, genererede Saiyong Zhu et al., (2014) ikke iPSC'er, men afkortede ved hjælp af små molekyler kort omprogrammering til pluripotens for at generere en induceret multipotent stamcelle (iMPC) tilstand, hvorfra endoderm stamceller og efterfølgende blev hepatocytter (iMPC-Heps) effektivt differentieret. Efter transplantation i en immundefekt musemodel for humant leversvigt prolifererede iMPC-Heps i vid udstrækning og erhvervede niveauer af hepatocytfunktion svarende til niveauet for humane primære voksne hepatocytter. iMPC-Heps dannede ikke tumorer, sandsynligvis fordi de aldrig kom i en pluripotent tilstand.
Disse resultater fastslår gennemførligheden af betydelig leverfopbygning af mus med humane hepatocytter genereret in vitro, hvilket fjerner en langvarig vejspærring på vejen til autolog levercelleterapi.
En cocktail af små molekyler, Y-27632 , A-83-01 (en TGFβ kinase/activin receptor som kinase ( ALK5 ) hæmmer) og CHIR99021 (potent hæmmer af GSK-3 ), kan omdanne rotte og mus modne hepatocytter in vitro ind i proliferative bipotente celler - CLiP'er (kemisk inducerede leverprogenitorer). CLiP'er kan differentiere sig til både modne hepatocytter og galdeepitelceller, der kan danne funktionelle duktale strukturer. I langtidskultur mistede CLiP'er ikke deres spredningskapacitet og deres leverdifferentieringsevne og kan genbefolke kronisk skadet levervæv.
Insulinproducerende celler
Komplikationer af diabetes mellitus, såsom hjerte -kar -sygdomme , retinopati , neuropati , nefropati og perifere kredsløbssygdomme afhænger af sukkerdysregulering på grund af mangel på insulin fra pancreas -beta -celler og kan være dødelige, hvis de ikke behandles. En af de lovende tilgange til at forstå og helbrede diabetes er at bruge pluripotente stamceller (PSC'er), herunder embryonale stamceller (ESC'er) og inducerede PCS'er (iPSC'er). Desværre ligner humane PSC-afledte insulin-udtrykkende celler humane føtale β-celler frem for voksne β-celler. I modsætning til voksne β-celler virker føtale β-celler funktionelt umodne, som det fremgår af øget basal glukosesekretion og mangel på glukosestimulering og bekræftet af RNA-seq, hvis transkripter .
En alternativ strategi er omdannelse af fibroblaster til distinkte endodermale stamcellepopulationer og ved hjælp af cocktails af signalfaktorer vellykket differentiering af disse endodermale stamceller til funktionelle beta-lignende celler både in vitro og in vivo.
Overudtryk af de tre transkriptionsfaktorer , kombinationen PDX1 (påkrævet til pancreatisk knopudvækst og betacellemodning), NGN3 (påkrævet for dannelse af endokrine precursorceller) og MAFA (til beta-cellemodning) kombination (kaldet PNM) kan føre til transformation af nogle celletyper i en betacelle-lignende tilstand. En tilgængelig og rigelig kilde til funktionelle insulinproducerende celler er tarm . PMN-ekspression i humane intestinale " organoider " stimulerer omdannelsen af tarmepitelceller til β-lignende celler, der muligvis er acceptable til transplantation .
Nephron Progenitors
Voksne proksimale tubulære celler blev direkte transkriptionelt omprogrammeret til nefronforfædre i den embryonale nyre ved hjælp af en pool af seks gener af instruktive transkriptionsfaktorer (SIX1, SIX2, OSR1, Eyes absent homolog 1 (EYA1), Homeobox A11 (HOXA11) og Snail homolog 2 (SNAI2)), der aktiverede gener i overensstemmelse med en cap mesenchym /nefron stamfænotype i den voksne proksimale tubulære cellelinje. Genereringen af sådanne celler kan føre til cellulære terapier mod voksen nyresygdom . Embryoniske nyreorganoider placeret i voksne rottenyrer kan undergå videre udvikling og vaskulær udvikling.
Blodkarceller
Efterhånden som blodkarrene ældes, bliver de ofte unormale i struktur og funktion og bidrager derved til talrige aldersrelaterede sygdomme, herunder myokardieinfarkt, iskæmisk slagtilfælde og åreforkalkning af arterier, der forsyner hjertet, hjernen og underekstremiteterne. Så et vigtigt mål er at stimulere vaskulær vækst for sikkerhedscirkulationen for at forhindre forværring af disse sygdomme. Inducerede vaskulære stamceller (iVPC'er) er nyttige til cellebaseret terapi designet til at stimulere koronar kollateral vækst. De blev genereret ved delvist omprogrammering af endotelceller. Den vaskulære forpligtelse for iVPC'er er relateret til den epigenetiske hukommelse af endotelceller, som skaber dem som cellulære komponenter i voksende blodkar. Det var derfor, da iVPC'er blev implanteret i myokardiet , de indpodet i blodkar og øget koronar kollateral strømning bedre end iPSC'er, mesenkymale stamceller eller native endotelceller.
Ex vivo genetisk modifikation kan være en effektiv strategi til forbedring af stamcellens funktion. For eksempel cellulær terapi, der anvender genetisk modifikation med Pim-1 kinase (en nedstrøms effektor af Akt , som positivt regulerer neovasculogenese) af knoglemarvsafledte celler eller humane hjerteprogenitorceller, isoleret fra svigtende myokard, resulterer i reparationsholdbarhed sammen med forbedring af funktionelle parametre for myokardial hæmodynamisk ydeevne.
Stamceller ekstraheret fra fedtvæv efter fedtsugning kan lokkes til at blive stamceller til glatte muskelceller (iPVSMC'er), der findes i arterier og vener.
2D-kultursystemet for humane iPS-celler i forbindelse med triple markerselektion ( CD34 (et overfladeglycophosphoprotein udtrykt på udviklingsmæssigt tidlige embryonale fibroblaster), NP1 (receptor-neuropilin 1) og KDR (kinase insert-domæneholdig receptor)) til isolering af vaskulogene precursorceller fra humane iPSC, genererede endotelceller, der efter transplantation dannede stabile, funktionelle museblodkar in vivo og varede i 280 dage.
For at behandle infarkt er det vigtigt at forhindre dannelse af fibrotisk arvæv. Dette kan opnås in vivo ved forbigående anvendelse af parakrinfaktorer , der omdirigerer stamcellebidrag fra native stamceller fra arvæv til kardiovaskulært væv. For eksempel i en mus myokardieinfarkt-model resulterer en enkelt intramyokardial injektion af human vaskulær endotelvækstfaktor A mRNA (VEGF-A modRNA), modificeret for at undslippe kroppens normale forsvarssystem, på lang sigt forbedring af hjertefunktionen på grund af mobilisering og omdirigering af epikardielle stamceller mod kardiovaskulære celletyper.
Blodstamceller
røde blodlegemer
RBC -transfusion er nødvendig for mange patienter. Til dato er udbuddet af RBC'er imidlertid stadig labilt. Derudover risikerer transfusion overførsel af infektionssygdomme. Et stort udbud af sikre RBC'er genereret in vitro ville hjælpe med at løse dette problem. Ex vivo erythroid -cellegenerering kan levere alternative transfusionsprodukter til at opfylde nuværende og fremtidige kliniske krav. Røde blodlegemer (RBC) genereret in vitro fra mobiliserede CD34 positive celler har normal overlevelse, når de transfunderes til en autolog modtager. RBC produceret in vitro indeholdt udelukkende føtal hæmoglobin (HbF), som redder funktionaliteten af disse RBC'er. In vivo blev skiftet mellem føtal og voksen hæmoglobin observeret efter infusion af nukleare erythroid -forstadier afledt af iPSC'er. Selvom RBC'er ikke har kerner og derfor ikke kan danne en tumor, har deres umiddelbare erythroblaster -forstadier kerner. Den endelige modning af erythroblaster til funktionelle RBC'er kræver en kompleks ombygningsproces, der ender med ekstrudering af kernen og dannelsen af en enukleret RBC. Celleprogrammering forstyrrer ofte enukleation. Transfusion af in vitro-genererede RBC'er eller erythroblaster beskytter ikke tilstrækkeligt mod tumordannelse.
Den aryl hydrocarbon receptor (AhR) pathway (som er blevet vist at være involveret i fremme af cancer celleudvikling) spiller en vigtig rolle i normal blodcelleudvikling. AhR-aktivering i humane hæmatopoietiske stamceller (HP'er) driver en hidtil uset udvidelse af HP'er, megakaryocyt- og erythroid-slægtceller. Se også Kortfattet gennemgang: SH2B3- genet koder for en negativ regulator af cytokinsignalering og naturligt forekommende funktionstabsvarianter i dette gen øger RBC-tællinger in vivo. Målrettet undertrykkelse af SH2B3 i primære humane hæmatopoietiske stam- og stamceller forbedrede modningen og det samlede udbytte af in vitro-afledte RBC'er. Desuden inaktivering af SH2B3 af CRISPR / Cas9 genomet redigering i humane pluripotente stamceller tilladt forøget erythroid celleekspansion med konserverede differentiering. (Se også oversigt.)
Trombocytter
Blodplader hjælper med at forhindre blødning hos trombocytopeniske patienter og patienter med trombocytæmi . Et væsentligt problem for multitransfunderede patienter er brydning over for trombocytransfusioner. Således ville evnen til at generere trombocytprodukter ex vivo og trombocytprodukter, der mangler HLA-antigener i serumfrie medier, have klinisk værdi. En RNA-interferensbaseret mekanisme anvendte en lentiviral vektor til at udtrykke RNAi med kort hårnål målrettet β2-mikroglobulin-transkripter i CD34-positive celler. Genererede blodplader viste en 85% reduktion i klasse I HLA -antigener. Disse blodplader syntes at have normal funktion in vitro
En klinisk anvendelig strategi for afledning af funktionelle blodplader fra human iPSC involverer etablering af stabile udødeliggjorte megakaryocyt-stamcellelinjer (imMKCL'er) gennem doxycyclin- afhængig overekspression af BMI1 og BCL-XL . De resulterende imMKCL'er kan udvides i kultur over længere perioder (4-5 måneder), selv efter kryokonservering . Stop af overekspressionen (ved fjernelse af doxycyclin fra mediet) af c-MYC, BMI1 og BCL-XL i voksende imMKCL'er førte til produktion af CD42b + blodplader med funktionalitet, der kan sammenlignes med den for native blodplader på basis af en række analyser in vitro og in vivo. Thomas et al., Beskriver en fremadrettet programmeringsstrategi, der er afhængig af den samtidige eksogene ekspression af 3 transkriptionsfaktorer: GATA1 , FLI1 og TAL1 . De fremprogrammerede megakaryocytter formerer sig og differentierer i kultur i flere måneder med megakaryocytrenhed over 90% og når op til 2x10 5 modne megakaryocytter pr. Input hPSC. Funktionelle blodplader genereres i hele kulturen, hvilket muliggør den potentielle indsamling af flere transfusionsenheder fra så få som en million startende hPSC'er. Se også oversigt
Immunceller
En specialiseret type hvide blodlegemer , kendt som cytotoksiske T -lymfocytter (CTL'er), produceres af immunsystemet og er i stand til at genkende specifikke markører på overfladen af forskellige infektiøse eller tumorceller, hvilket får dem til at starte et angreb for at dræbe de skadelige celler. Immunterapi med funktionelle antigenspecifikke T-celler har derfor potentiale som en terapeutisk strategi til bekæmpelse af mange kræftformer og virusinfektioner. Cellekilder er imidlertid begrænsede, fordi de produceres i små mængder naturligt og har en kort levetid.
En potentielt effektiv tilgang til generering af antigenspecifikke CTL'er er at omdanne modne immun-T-celler til iPSC'er, som besidder ubestemt proliferationskapacitet in vitro og efter deres multiplikation til at lokke dem til at redifferentiere tilbage til T-celler.
En anden metode kombinerer iPSC og kimær antigenreceptor (CAR) teknologier til at generere humane T -celler målrettet mod CD19 , et antigen udtrykt af ondartede B -celler , i vævskultur. Denne tilgang til generering af terapeutiske humane T -celler kan være nyttig til kræftimmunterapi og andre medicinske anvendelser.
Invariant natural killer T (iNKT) celler har et stort klinisk potentiale som adjuvanser til kræftimmunterapi . iNKT -celler fungerer som medfødte T -lymfocytter og fungerer som en bro mellem det medfødte og erhvervede immunsystem . De øger antitumorresponser ved at producere interferon-gamma (IFN-γ). Tilgangen til indsamling, omprogrammering/dedifferentiering, re-differentiering og injektion er blevet foreslået til relateret tumorbehandling.
Dendritiske celler (DC) er specialiseret til at kontrollere T-cellers respons. DC med passende genetiske modifikationer kan overleve længe nok til at stimulere antigenspecifik CTL og derefter elimineres fuldstændigt. DC-lignende antigenpræsenterende celler opnået fra humane inducerede pluripotente stamceller kan tjene som kilde til vaccinationsterapi .
CCAAT/enhancer-bindende protein-α (C/EBPα) inducerer transdifferentiering af B-celler til makrofager ved høj effektivitet og forbedrer omprogrammering til iPS-celler, når det co-udtrykkes med transkriptionsfaktorer Oct4, Sox2, Klf4 og Myc. med en 100-fold stigning i iPS-celles omprogrammeringseffektivitet, der involverer 95% af befolkningen. Endvidere kan C/EBPa konvertere udvalgte humane B-cellelymfom- og leukæmicellelinjer til makrofaglignende celler ved høj effektivitet, hvilket forringer cellernes tumordannende kapacitet.
Thymiske epitelceller foryngelse
Den brissel er den første orgel at forværres som folk alder. Denne krympning er en af hovedårsagerne til, at immunsystemet bliver mindre effektivt med alderen. Formindsket ekspression af thymisk epitelcellelinie transkriptionsfaktor FOXN1 er blevet impliceret som en komponent af mekanismen regulerende aldersrelateret involution.
Clare Blackburn og kolleger viser, at etableret aldersrelateret thymisk involution kan vendes ved tvungen opregulering af kun en transkriptionsfaktor-FOXN1 i de tymiske epitelceller for at fremme foryngelse , spredning og differentiering af disse celler til fuldt funktionelt thymisk epitel. Denne foryngelse og øget spredning blev ledsaget af opregulering af gener, der fremmer cellecyklusprogression ( cyclin D1 , ΔN p63 , FgfR2IIIb ), og som er nødvendige i de tymiske epitelceller for at fremme specifikke aspekter af T -celleudvikling ( Dll4 , Kitl , Ccl25 , Cxcl12 , Cd40 , Cd80 , Ctsl , Pax1 ). I fremtiden kan denne metode blive meget udbredt til at forbedre immunfunktionen og bekæmpe betændelse hos patienter ved at forynge thymus in situ .
Mesenkymale stamceller
Induktion
Mesenkymale stamme/stromaceller (MSC'er) er under undersøgelse for anvendelser inden for hjerte-, nyre-, neurale-, led- og knoglereparation samt ved inflammatoriske tilstande og hæmopoietisk cotransplantation. Dette er på grund af deres immunsuppressive egenskaber og evne til at differentiere sig til en bred vifte af mesenkymale slægtsvæv. MSC høstes typisk fra voksen knoglemarv eller fedt, men disse kræver smertefulde invasive procedurer og er lavfrekvente kilder, der kun udgør 0,001-0,01% af knoglemarvsceller og 0,05% i fedtsugningsaspirater. Af bekymring for autolog brug, især hos ældre, der har mest brug for vævsreparation, falder MSC'er i mængde og kvalitet med alderen.
IPSC'er kunne opnås ved cellernes foryngelse af selv hundredeårige. Fordi iPSC'er kan høstes fri for etiske begrænsninger og kultur kan udvides på ubestemt tid, er de en fordelagtig kilde til MSC'er. IPSC-behandling med SB-431542 fører til hurtig og ensartet MSC-generering fra humane iPSC'er. (SB-431542 er en hæmmer af activin/TGF-veje ved at blokere fosforylering af ALK4- , ALK5- og ALK7- receptorer.) Disse iPS-MSC'er kan mangle teratomdannende evne, vise en normal stabil karyotype i kultur og udvise vækst- og differentieringsegenskaber, der ligner de primære MSC'ers. Det har potentiale for in vitro-opskalering, hvilket muliggør MSC-baserede terapier. MSC afledt af iPSC har kapacitet til at hjælpe periodontal regenerering og er en lovende kilde til let tilgængelige stamceller til brug i den kliniske behandling af periodontitis.
Lai et al., & Lu rapporterer den kemiske metode til at generere MSC-lignende celler (iMSC'er) fra humane primære dermale fibroblaster ved hjælp af seks kemiske hæmmere (SP600125, SB202190, Go6983, Y-27632, PD0325901 og CHIR99021) med eller uden 3 vækstfaktorer (transformerende vækstfaktor-β (TGF-β), grundlæggende fibroblastvækstfaktor (bFGF) og leukæmihæmmende faktor (LIF)). Den kemiske cocktail omdanner direkte humane fibroblaster til iMSC'er med en monolagskultur på 6 dage, og konverteringsfrekvensen var ca. 38%.
Udover celleterapi in vivo kan kulturen af humane mesenkymale stamceller bruges in vitro til masseproduktion af exosomer , som er ideelle midler til levering af lægemidler.
Dedifferentierede adipocytter
Fedtvæv , på grund af dets overflod og relativt mindre invasive høstmetoder, repræsenterer en kilde til mesenkymale stamceller (MSC'er). Desværre er fedtsugningsaspirater kun 0,05% MSC'er. Imidlertid kan en stor mængde modne adipocytter, som generelt har mistet deres proliferative evner og derfor er typisk kasseres, let isoleres fra adipøst cellesuspensionen og dedifferentierede i lipide -fri fibroblastlignende celler, opkaldt dedifferentierede fedt (DFAT) celler . DFAT-celler genetablerer aktiv spredningsevne og udtrykker multipotente kapaciteter. Sammenlignet med voksne stamceller viser DFAT -celler unikke fordele i overflod, isolation og homogenitet. Under korrekt induktionskultur in vitro eller korrekt miljø in vivo kunne DFAT -celler demonstrere adipogene, osteogene, chondrogene og myogene potentialer. De kunne også udvise perivaskulære egenskaber og fremkalde neovaskularisering.
Chondrogene celler
Brusk er bindevævet, der er ansvarlig for friktionsfri ledbevægelse. Dens degeneration resulterer i sidste ende i fuldstændigt tab af ledfunktion i de sene stadier af slidgigt . Som et avaskulært og hypocellulært væv har brusk en begrænset kapacitet til selvreparation. Chondrocytter er den eneste celletype i brusk, hvor de er omgivet af den ekstracellulære matrix, som de udskiller og samler.
En metode til fremstilling af brusk er at inducere det fra iPS -celler. Alternativt er det muligt at konvertere fibroblaster direkte til inducerede chondrogene celler (iChon) uden et mellemliggende iPS-celletrin ved at indsætte tre omprogrammeringsfaktorer (c-MYC, KLF4 og SOX9). Humane iChon -celler udtrykte markørgener for chondrocytter (type II -kollagen), men ikke fibroblaster.
Implanteret i defekter skabt i ledbrusk hos rotter overlevede humane iChon -celler til dannelse af bruskvæv i mindst fire uger uden tumorer. Metoden gør brug af c-MYC, som menes at have en stor rolle i tumorigenese og anvender et retrovirus til at indføre omprogrammeringsfaktorer, udelukkende fra umodificeret brug i human terapi.
Kilder til celler til omprogrammering
De hyppigst anvendte kilder til omprogrammering er blodlegemer og fibroblaster, der opnås ved biopsi af huden, men at tage celler fra urinen er mindre invasiv. Sidstnævnte metode kræver ikke en biopsi eller blodprøveudtagning. Fra 2013 var urin-afledte stamceller blevet differentieret til endotel, osteogen, chondrogen, adipogen, skeletal myogen og neurogen slægt uden at danne teratomer. Derfor er deres epigenetiske hukommelse velegnet til omprogrammering til iPS -celler. Imidlertid forekommer få celler i urinen, kun lave konverteringseffektiviteter var opnået, og risikoen for bakteriel kontaminering er relativt høj.
En anden lovende kilde til celler til omprogrammering er mesenkymale stamceller, der stammer fra menneskelige hårsække.
Oprindelsen af somatiske celler, der bruges til omprogrammering, kan påvirke effektiviteten af omprogrammering, de resulterende inducerede stamcellers funktionelle egenskaber og evnen til at danne tumorer.
IPSC'er bevarer en epigenetisk hukommelse om deres oprindelsesvæv, hvilket påvirker deres differentieringspotentiale. Denne epigenetiske hukommelse manifesterer sig ikke nødvendigvis på pluripotensstadiet - iPSC'er afledt af forskellige væv udviser korrekt morfologi, udtrykker pluripotensmarkører og er i stand til at differentiere sig til de tre embryonale lag in vitro og in vivo. Denne epigenetiske hukommelse kan imidlertid manifestere sig under re-differentiering til specifikke celletyper, der kræver det specifikke sted, der bærer resterende epigenetiske mærker.
Se også
- Transdifferentiering
- Eksempler på in vitro-transdifferentiering ved slægt-instruktiv tilgang
- Eksempler på in vitro transdifferentiering ved indledende epigenetisk aktiveringsfasemetode
- Eksempler på in vivo transdifferentiering ved slægt-instruktiv tilgang
- Skade fremkaldt stamcelle nicher
- Transkriptionsfaktorer
- Vækstfaktorer
- Pionerfaktorer
- Cellular differentiering
- CAF-1
Referencer
Yderligere læsning
- Scudellari M (juni 2016). "Sådan ændrede iPS -celler verden" . Natur . 534 (7607): 310–2. Bibcode : 2016Natur.534..310S . doi : 10.1038/534310a . PMID 27306170 .
- Turksen K, Nagy A (2016). Inducerede pluripotente stamceller (iPS) . Metoder i molekylærbiologi. 1357 . doi : 10.1007/978-1-4939-3055-5 . ISBN 978-1-4939-3054-8. S2CID 46010857 .
- Li M, Izpisua Belmonte JC (september 2016). "Ser på fremtiden efter 10 års inducerede pluripotente stamcelleteknologier" . Naturprotokoller . 11 (9): 1579–85. doi : 10.1016/j.cell.2016.08.055 . PMID 27490631 .
- Srivastava D, DeWitt N (september 2016). "In Vivo cellulær omprogrammering: den næste generation" . Celle . 166 (6): 1386–1396. doi : 10.1016/j.cell.2016.08.055 . PMC 6234007 . PMID 27610565 .
- Tabar V, Studer L (februar 2014). "Pluripotente stamceller i regenerativ medicin: udfordringer og nylige fremskridt" . Naturanmeldelser. Genetik . 15 (2): 82–92. doi : 10.1038/nrg3563 . PMC 4539940 . PMID 24434846 .
- Tan Y, Ooi S, Wang L (januar 2014). "Immunogenicitet og tumorigenicitet af pluripotente stamceller og deres derivater: genetiske og epigenetiske perspektiver" . Nuværende stamcelleforskning og terapi . 9 (1): 63–72. doi : 10.2174/1574888x113086660068 . PMC 3873036 . PMID 24160683 .
- Yamanaka S (juni 2012). "Inducerede pluripotente stamceller: fortid, nutid og fremtid" . Celle stamcelle . 10 (6): 678–684. doi : 10.1016/j.stem.2012.05.005 . PMID 22704507 .
- Takahashi K, Yamanaka S (juni 2013). "Inducerede pluripotente stamceller inden for medicin og biologi" . Udvikling . 140 (12): 2457–61. doi : 10.1242/dev.092551 . PMID 23715538 .
- Asuelime GE, Shi Y (august 2012). "Et tilfælde af cellulær alkymi: omprogrammering af slægter og dets potentiale inden for regenerativ medicin" . Journal of Molecular Cell Biology . 4 (4): 190–6. doi : 10.1093/jmcb/mjs005 . PMC 3408064 . PMID 22371436 .
- Lensch MW, Mummery CL (juni 2013). "Fra at stjæle ild til mobilprogrammering: en videnskabelig historie, der førte til Nobelprisen i 2012" . Stamcellerapporter . 1 (1): 5–17. doi : 10.1016/j.stemcr.2013.05.001 . PMC 3757737 . PMID 24052937 .
- Zhou Q (oktober 2013). "Inducerede pluripotente stamceller: nuværende fremskridt og fremtidsperspektiver. Forord" . Genomics, Proteomics & Bioinformatics . 11 (5): 257–8. doi : 10.1016/j.gpb.2013.10.001 . PMC 4357784 . PMID 24121127 .
- Lin J, Li MR, Ti DD, Chen MX, Hao HJ, Zhao YL, et al. (Januar 2013). "Mikromiljø-fremkaldt cellelinieomdannelse: Flytning af fokus fra intern omprogrammering til ekstern tvang". Aldersforskningsanmeldelser . 12 (1): 29–38. doi : 10.1016/j.arr.2012.04.002 . PMID 22561469 . S2CID 40367513 .
- Takahashi K (februar 2014). "Mobil omprogrammering" . Cold Spring Harbor -perspektiver i biologi . 6 (2): a018606. doi : 10.1101/cshperspect.a018606 . PMC 3941237 . PMID 24492711 .
- Nobelprisen i fysiologi eller medicin 2012 Tildelt for opdagelse af, at modne celler kan omprogrammeres til at blive pluripotente
- Hussein SM, Nagy AA (oktober 2012). "Fremskridt i omprogrammeringsområdet: nye faktorer, nye strategier og et nyt syn". Nuværende udtalelse i genetik og udvikling . 22 (5): 435–43. doi : 10.1016/j.gde.2012.08.007 . PMID 22959308 .
- Zhang Y, Yao L, Yu X, Ou J, Hui N, Liu S (december 2012). "En dårlig efterligning af en naturlig proces: en opfordring til at genoverveje iPSC -teknikteknikken" . Cellecyklus . 11 (24): 4536–44. doi : 10.4161/cc.22575 . PMC 3562298 . PMID 23114619 .
- Luni C, Giulitti S, Serena E, Ferrari L, Zambon A, Gagliano O, et al. (Maj 2016). "Højeffektiv cellulær omprogrammering med mikrofluidika". Naturmetoder . 13 (5): 446–52. doi : 10,1038/nmeth.3832 . PMID 27088312 . S2CID 5462386 . en 50 gange stigning i effektivitet; små mængder; differentiering til ønskede celler i den samme platform
- Mochiduki Y, Okita K (juni 2012). "Metoder til iPS -cellegenerering til grundforskning og kliniske applikationer". Bioteknologisk Journal . 7 (6): 789–97. doi : 10.1002/biot.201100356 . PMID 22378737 . S2CID 22317543 .
- Madonna R (oktober 2012). "Menneskeinducerede pluripotente stamceller: på jagt efter kliniske anvendelser". Molekylær bioteknologi . 52 (2): 193–203. doi : 10.1007/s12033-012-9504-0 . PMID 22302314 . S2CID 9920142 .
- Lorenzo IM, Fleischer A, Bachiller D (august 2013). "Generering af mus og mennesker inducerede pluripotente stamceller (iPSC) fra primære somatiske celler". Stamcelleanmeldelser og rapporter . 9 (4): 435–50. doi : 10.1007/s12015-012-9412-5 . HDL : 10261/98876 . PMID 23104133 . S2CID 2225015 .
-
"Stamcelleprogrammeringsværktøjer" . Invitrogen .
Detaljerede protokoller til omprogrammering og til analyse af iPSC'er
- Buganim Y, Faddah DA, Jaenisch R (juni 2013). "Mekanismer og modeller for somatisk celleprogrammering" . Naturanmeldelser. Genetik . 14 (6): 427–39. doi : 10.1038/nrg3473 . PMC 4060150 . PMID 23681063 .



