Methylmalonsyreæmi - Methylmalonic acidemia
| Methylmalonsyreæmi | |
|---|---|
| Andre navne | MMA |
 | |
| Methylmalonsyre | |
| Specialitet |
Endokrinologi |
Methylmalonsyreæmi , også kaldet methylmalonsyreuri , er en autosomal recessiv metabolisk lidelse, der forstyrrer normal aminosyremetabolisme. Det er en klassisk type organisk acidæmi . Resultatet af denne tilstand er manglende evne til korrekt at fordøje specifikke fedtstoffer og proteiner, hvilket igen fører til en ophobning af et giftigt niveau af methylmalonsyre i blodet.
Methylmalonsyreæmi stammer fra flere genotyper , alle former for lidelsen diagnosticeres normalt i den tidlige neonatale periode, der viser progressiv encefalopati og sekundær hyperammonæmi . Lidelsen kan resultere i døden, hvis den ikke er diagnosticeret eller efterlades ubehandlet. Det anslås, at denne lidelse har en hyppighed på 1 ud af 48.000 fødsler, selvom den høje dødelighed i diagnosticerede tilfælde vanskeliggør nøjagtig bestemmelse. Methylmalonsyre findes i samme frekvens på tværs af etniske grænser.
Symptomer og tegn
Afhængigt af det / de berørte gen (er) kan denne lidelse vise symptomer, der spænder fra mild til livstruende.
- Slag
- Progressiv encefalopati
- Anfald
- Nyresvigt
- Opkastning
- Dehydrering
- Manglende trives og forsinkelser i udviklingen
- Sløvhed
- Gentagne gærinfektioner
- Acidose
- Hepatomegali
- Hypotoni
- Pankreatitis
- Åndedrætsbesvær
årsag
Genetisk

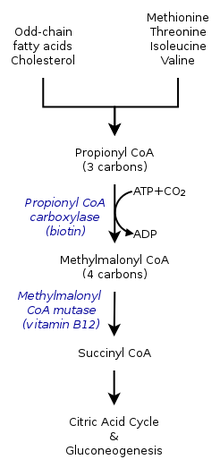
De arvelige former for methylmalonsyreæmi forårsager defekter i den metaboliske vej, hvor methylmalonyl-coenzym A (CoA) omdannes til succinyl-CoA af enzymet methylmalonyl-CoA-mutase.
Vitamin B 12 er også nødvendig for omdannelsen af methylmalonyl-CoA til succinyl-CoA. Mutationer, der fører til defekter i vitamin B 12 -metabolisme eller i dets transport, resulterer ofte i udviklingen af methylmalonsyreæmi.
Denne lidelse har et autosomalt recessivt arvsmønster, hvilket betyder, at det defekte gen er placeret på et autosom , og to kopier af genet - en fra hver forælder - skal arves for at blive påvirket af lidelsen. Forældrene til et barn med en autosomal recessiv lidelse er bærere af en kopi af det defekte gen, men er normalt ikke påvirket af lidelsen.
Ernæringsmæssig
Selvom det ikke altid er grupperet sammen med de nedarvede versioner, kan en alvorlig ernæringsmæssig mangel på vitamin B 12 også resultere i syndrom med identiske symptomer og behandlinger som de genetiske methylmalonsyre. Methylmalonyl-CoA kræver vitamin B 12 for at danne succinyl-CoA. Når mængden af B 12 er utilstrækkelig til omdannelse af cofaktor methylmalonyl-CoA i succinyl-CoA, opbygning af ubrugte methylmalonyl-CoA sidste ende fører til methylmalonsyre acidemia. Denne diagnose bruges ofte som en indikator på vitamin B 12 -mangel i serum .
Mekanisme
Patofysiologi
Ved methylmalonsyreæmi er kroppen ikke i stand til at nedbryde aminosyrerne methionin , threonin , isoleucin og valin ; som et resultat ophobes methylmalonsyre i blodet og vævene. Dem, der er ramt af denne lidelse, mangler enten funktionelle kopier eller tilstrækkelige niveauer af et eller flere af følgende enzymer: methylmalonyl-CoA-mutase , methylmalonyl-CoA-epimerase eller dem, der er involveret i adenosylcobalaminsyntese .
Methylmalonyl-CoA mutase
Det anslås, at så mange som 60% af tilfældene er resultatet af et muteret MUT- gen, der koder for proteinet methylmalonyl-CoA-mutase. Dette enzym er ansvarligt for fordøjelsen af potentielt toksiske derivater af nedbrydningen af de ovennævnte aminosyrer og fedtstoffer, primært kolesterol , især dette enzym omdanner methylmalonyl-CoA til succinyl-CoA. Uden dette enzym har kroppen ingen midler til at neutralisere eller fjerne methylmalonsyre og beslægtede forbindelser. Virkningen af dette enzym kan også være lammet af mutationer i MMAA- , MMAB- og MMADHC- generne, som hver koder for et protein, der er nødvendigt for normal funktion af methylmalonyl-CoA-mutase.
Methylmalonyl-CoA epimerase
Mutationer i MCEE- genet, som koder for methylmalonyl-CoA-epimerase-proteinet, også omtalt som methylmalonyl-racemase, vil forårsage en meget mere mild form for lidelsen end den relaterede methylmalonyl-CoA-mutase-variant. Ligesom mutasen fungerer epimerasen også ved at nedbryde de samme stoffer, men i betydeligt mindre omfang end mutasen gør. De fænotypiske forskelle forårsaget af mangel på epimerasen i modsætning til mutasen er så milde, at der inden for det medicinske samfund er debat om, hvorvidt denne genetiske mangel kan betragtes som en lidelse eller et klinisk syndrom.
Adenosylcobalamin
Også kendt som vitamin B 12, er denne form for cobalamin en påkrævet cofaktor af methylmalonyl-CoA-mutase. Selv med en funktionel version af enzymet ved fysiologisk normale niveauer, hvis B 12 ikke kan omdannes til denne aktive form, vil mutase være ude af stand til at fungere.
Progression
Selvom der ikke er forskellige stadier af sygdommen, er methylmalonsyreæmi en progressiv tilstand; symptomerne på denne lidelse forværres, når koncentrationen af methylmalonsyre stiger. Hvis de udløsende proteiner og fedtstoffer ikke fjernes fra kosten, kan denne opbygning føre til uoprettelig nyre- eller leverskade og til sidst død.
Diagnose
En af, hvis ikke den mest almindelige form for organisk acidæmi, methylmalonsyreæmi er ikke synlig ved fødslen, da symptomer normalt ikke viser sig, før proteiner tilføjes til spædbarnets kost. På grund af dette manifesterer symptomer sig typisk når som helst inden for det første leveår. På grund af sværhedsgraden og hurtigheden, hvor denne lidelse kan forårsage komplikationer, når den ikke udføres, er screening for methylmalonsyreæmi ofte inkluderet i den nyfødte screeningundersøgelse.
På grund af manglende evne til korrekt at nedbryde aminosyrer fuldstændigt findes biproduktet af proteinfordøjelse, forbindelsen methylmalonsyre, i en uforholdsmæssig koncentration i blod og urin hos de ramte. Disse unormale niveauer bruges som de vigtigste diagnostiske kriterier til diagnosticering af lidelsen. Denne lidelse bestemmes typisk ved brug af en urinanalyse eller blodpanel . Tilstedeværelsen af methylmalonsyreæmi kan også mistænkes ved brug af en CT- eller MR -scanning eller ammoniak -test, men disse tests er på ingen måde specifikke og kræver klinisk og metabolisk/korrelation. Forhøjede niveauer af ammoniak , glycin og ketonlegemer kan også være til stede i blodet og urinen.
Typer
Methylmalonsyreæmi har varierende diagnoser, behandlingskrav og prognoser, som bestemmes af den specifikke genetiske mutation, der forårsager den arvelige form for lidelsen. Følgende er de kendte genotyper, der er ansvarlige for methylmalonsyreæmi:
| OMIM | Navn | Gene |
|---|---|---|
| 251100 | cblA -type | MMAA |
| 251110 | cblB type | MMAB |
| 277400 | cblC -type | MMACHC |
| 277410 | cblD -type | MMADHC |
| 277380 | cblF type | LMBRD1 |
| 251000 | mut type | MUT |
Mut-typen kan yderligere opdeles i mut0 og mut-undertyper, hvor mut0 er karakteriseret ved en fuldstændig mangel på methylmalonyl-CoA-mutase og mere alvorlige symptomer og mut-karakteriseret ved en reduceret mængde mutaseaktivitet.
Mut-, cblB og cblA-versioner af methylmalonsyreæmi har vist sig at være cobalamin-responsive. Mut0 er en ikke -reagerende variant.
Behandling
Kost
Behandling af alle former for denne tilstand er primært afhængig af en proteinfattig kost, og afhængigt af hvilken variant af lidelsen den enkelte lider af, forskellige kosttilskud. Alle varianter reagerer på levo -isomeren af carnitin, da forkert nedbrydning af de berørte stoffer resulterer i, at patienter udvikler en carnitinmangel. Carnitinen hjælper også med at fjerne acyl-CoA, hvis ophobning er almindelig i lavprotein-diæter ved at omdanne det til acyl-carnitin, som kan udskilles i urinen. Selvom ikke alle former for methylmalonyl acidæmi reagerer på cobalamin, bruges cyanocobalamintilskud ofte i første linie behandling af denne lidelse. Hvis den enkelte viser sig reagerer på både cobalamin og carnitin kosttilskud, så det kan være muligt for dem at indtage stoffer, der indeholder små mængder af den problematiske aminosyrer isoleucin, threonin, methionin og valin uden at forårsage et angreb.
Kirurgisk
En mere ekstrem behandling omfatter nyre- eller levertransplantation fra en donor uden tilstanden. De fremmede organer vil producere en funktionel version af de defekte enzymer og fordøje methylmalonsyren, men alle ulemperne ved organtransplantation er naturligvis anvendelige i denne situation. Der er tegn på, at centralnervesystemet kan metabolisere methylmalonyl-CoA i et system isoleret fra resten af kroppen. Hvis dette er tilfældet, må transplantation ikke vende de neurologiske virkninger af methylmalonsyre før transplantationen eller forhindre yderligere skade på hjernen ved fortsat opbygning.
Prognose
Prognosen vil variere afhængigt af sværhedsgraden af tilstanden og den enkeltes reaktion på behandlingen. Prognose er typisk bedre for dem med cobalamin-responsive varianter og ikke lovende hos dem, der lider af noncobalamin-responsive varianter. Mildere varianter har en højere hyppighed i befolkningen end de mere alvorlige. Selv med kostændringer og fortsat lægehjælp er det muligvis ikke muligt at forhindre neurologisk skade hos personer med en ikke -reagerende acidæmi. Uden ordentlig behandling eller diagnose er det ikke ualmindeligt, at det første syriske angreb er dødeligt.
På trods af disse udfordringer har behandlingen og forståelsen af tilstanden siden den første gang blev identificeret i 1967 forbedret til det punkt, hvor det ikke er uhørt, at selv dem med ikke -reagerende former for methylmalonsyreæmi kan nå voksenalderen og endda bære og føde børn sikkert.
Forskning
Nosologisk historie
MMA blev først karakteriseret af Oberholzer et al. i 1967.
Neurologiske virkninger
At MMA kan have katastrofale virkninger på nervesystemet er længe blevet rapporteret; den mekanisme, hvormed dette sker, er imidlertid aldrig blevet bestemt. Udgivet den 15. juni 2015 udførte forskning om virkningerne af methylmalonsyre på neuroner isoleret fra fosterrotter i en in vitro -indstilling ved hjælp af en kontrolgruppe af neuroner behandlet med en alternativ syre med lignende pH . Disse tests har antydet, at methylmalonsyre forårsager fald i cellestørrelse og stigning i frekvensen af cellulær apoptose på en koncentrationsafhængig måde, idet mere ekstreme effekter ses ved højere koncentrationer. Endvidere har mikro -array -analyse af disse behandlede neuroner også antydet, at på en epigenetisk -niveau methylmalonsyre ændrer transkriptionshastigheden for 564 gener, især herunder dem, der er involveret i apoptose-, p53- og MAPK -signalveje.
Mitokondriel dysfunktion
Da omdannelsen af methylmalonyl-CoA til succinyl-CoA finder sted inde i mitokondrierne , har mitokondriel dysfunktion som følge af nedsat elektrontransportkædefunktion længe været mistænkt som en funktion i MMA. Nyere forskning har fundet ud af, at mitokondrier hos rotter, der er ramt af lidelsen, vokser til usædvanlig størrelse i rottemodeller, kaldet megamitochondrier. Disse megamitokondrier ser også ud til at have deformerede indre strukturer og et tab i elektronrigdom i deres indre matrix . Disse megamitokondrier viste også tegn på nedsat respiratorisk kædefunktion, især i respiratorisk kompleks IV, som kun fungerede med ca. 50% effektivitet. Lignende ændringer blev identificeret i mitokondrier i en leverprøve, der blev fjernet under transplantation fra en 5-årig dreng, der led af MMA.
Godartet mut fænotype
Nylige casestudier med flere patienter, der præsenterer nonresponsive mut0 MMA med en specifik mutation betegnet p.P86L, har antydet muligheden for yderligere underinddeling i mut type MMA muligvis. Selvom det i øjeblikket er uklart, om dette skyldes den specifikke mutation eller tidlig opsporing og behandling, trods fuldstændig manglende reaktion på cobalamintilskud, så disse personer ud til at udvikle en stort set godartet og næsten fuldstændig asymptomatisk version af MMA. På trods af at de konstant viste forhøjet methylmalonsyre i blodet og urinen, så disse individer for en stor del udviklingsmæssigt normale ud.
Bemærkelsesværdige sager
- Ryan Stallings, et spædbarn i St. Louis, blev fejlagtigt diagnosticeret med ethylenglycolforgiftning i stedet for MMA i 1989, hvilket førte til en uretmæssig morddom og livstidsdom for hans mor, Patricia Stallings .
Se også
Noter
Referencer
Yderligere læsning
- GeneReviews artikel om methylmalonsyre
- GeneReviews artikel om lidelser i intracellulær kobalaminmetabolisme
eksterne links
| Klassifikation | |
|---|---|
| Eksterne ressourcer |