Nepafenac - Nepafenac
 | |
| Kliniske data | |
|---|---|
| Handelsnavne | Nevanac, Ilevro, Amnac, andre |
| AHFS / Drugs.com | Monografi |
| MedlinePlus | a606007 |
| Licensdata | |
| Graviditet kategori |
|
| Ruter for administration |
Aktuelle øjendråber |
| ATC-kode | |
| Lovlig status | |
| Lovlig status | |
| Identifikatorer | |
| |
| CAS-nummer | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| CHEMBL | |
| CompTox Dashboard ( EPA ) | |
| ECHA InfoCard |
100.207.414 |
| Kemiske og fysiske data | |
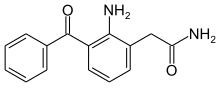
| Formel | C 15 H 14 N 2 O 2 |
| Molar masse | 254.289 g · mol −1 |
| 3D-model ( JSmol ) | |
| |
| |
|
| |
Nepafenac , der sælges under varemærket Nevanac blandt andre, er et NSAID (NSAID), sælges normalt som en recept øjendråber 0,1% opløsning (Nevanac) eller 0,3% opløsning (Ilevro). Det bruges til at behandle smerte og betændelse forbundet med grå stær kirurgi. Nepafenac er et prodrug af amfenac , en hæmmer af COX-1 og COX-2- aktivitet.
Medicinske anvendelser
Nepafenac er indiceret til brug til behandling af smerte og betændelse efter grå stæroperation.
I EU er nepafenac også indiceret til reduktion af risikoen for postoperativ makulaødem forbundet med kataraktkirurgi hos mennesker med diabetes.
Farmakologi
Handlingsmekanisme
Nepafenac er et NSAID, menes at være et prolægemiddel af amfenac efter omdannelse af okulære vævshydrolaser efter penetration via hornhinden . Amfenac menes ligesom andre NSAID'er at hæmme cyclooxygenase- virkningen.
Bivirkninger
Bivirkninger inkluderer hovedpine; løbende næse; smerter eller pres i ansigtet kvalme; opkastning og tørre, kløende, klæbrige øjne. Alvorlige bivirkninger inkluderer røde eller blodig øjne; fremmedlegemer i øjet; følsomhed over for lys nedsat synsstyrke ; at se pletter eller pletter tårende øjne; eller øjenudslip eller skorpedannelse.
Regulerende
Nevanac
Den 25. februar 2005 indgav Alcon en ny lægemiddelansøgning (NDA) til den amerikanske fødevare- og lægemiddeladministration (FDA) for Nevanac 0,1%. Resultater fra de to forsøg, der er henvist til i NDA (fase 2/3 undersøgelse C-02-53; fase 3 undersøgelse C-03-32) er ikke blevet offentliggjort. Undersøgelse C-02-53 bestod af 228 patienter på tværs af 10 centre i USA. Undersøgelse C-03-32 bestod af 522 patienter på tværs af 22 centre i USA. De præsenterede effektresultater blev bekræftet i en undersøgelse offentliggjort i 2007.
Nevanac blev godkendt af FDA den 19. august 2005 med ansøgningsnummer 021–862.
Ilevro
En NDA for Ilevro blev indgivet den 15. december 2011. I en en-måneders undersøgelse opstod der ingen nye toksiciteter i den nye formulering af nepafenac. Oplysninger om sikkerhed og virkning blev afledt af den tidligere Nevanac-applikation. I juni 2010 startede en bekræftende undersøgelse (Studie C09055) bestående af over 2000 patienter fra 49 amerikanske lokaliteter og 37 europæiske lokaliteter. Et andet fase 3-forsøg (undersøgelse C11003) blev udført i en befolkning på 1.342 patienter på 37 steder i USA, som ikke viste overlegenhed over Nevanac i et ændret doseringsregime.
Ilevro blev godkendt af FDA den 16. oktober 2012 med ansøgningsnummer 203–491.
Kommercialisering
Både Nevanac og Ilevro produceres og sælges af Alcon , Inc. Alcon er i øjeblikket en division af Novartis International AG, der primært er baseret i Schweiz. Alcon, Inc. har også placeringer i både Schweiz og USA. Virksomheden har gennemgået flere navneændringer, fra Alcon Laboratories, Inc. til Alcon Universal, Ltd., til Alcon, Inc.
Nevanac kom ind på markedet i 2005 som et produkt af Alcon, på det tidspunkt et datterselskab af Nestlé. Den 6. april 2008 indvilligede Novartis i at købe cirka 74 millioner aktier i Alcon fra Nestlé til $ 143,18 pr. Aktie. Den 4. januar 2010 indvilligede Novartis i at købe alle resterende aktier i Alcon fra Nestlé, i alt 156 millioner aktier eller 77% af aktierne i selskabet. På købstidspunktet blev Alcon bestyrelse fremsat et forslag om en fusion i henhold til schweizisk fusionsret. Fusionen blev aftalt den 15. december 2010, hvilket gjorde Alcon til "den næststørste division inden for Novartis." Fusionen blev afsluttet den 8. april 2011.
Ilevro blev lanceret af Alcon den 21. januar 2013. I 2014 og 2015 voksede Alcons nettosalg, hvilket blandt andet bidrog til den øgede omsætning af Ilevro. Det regnskabsår rapporterede Novartis $ 18 milliarder i samlet finansiel gæld. Denne figur er vokset støt siden. I 2016 rapporterede Novartis en samlet gæld på 23,8 mia. $, Op fra de 21,9 mia. $, Der blev rapporteret i 2015, og de 20,4 mia. $, Der blev rapporteret i 2014. Fra maj 2017 anslås Novartis til at være 193,2 mia.
Den 27. januar 2016 blev Alcon flyttet til at blive en afdeling af Innovative Medicines Division i Novartis. Tidligt i 2016 indgik Alcon aftaler med både TrueVision og PowerVision og erhvervede Transcend Medical. Fra januar 2017 afvejer Novartis muligheder for Alcon i forretningsstrukturen.
Kommercielle risici
Alcon stod over for faldende vækst i 2016 efter at have stået over for udfordringer inden for udvikling og markedsføring af nye produkter.
Marketing
Novartis opretholder en detaljeringsenhed rettet mod sundhedspersonale bestående af over 3.000 ansatte i USA og yderligere 21.000 over hele verden. Novartis søger også at udvide direkte-til-forbruger-reklame og adgang til specialprodukter. Novartis bemærker også indflydelsen af position og præference på amerikanske centre for Medicare & Medicaid-formularer i udvidelsen af deres markedsværdi.
Nepafenac, Nevanac og Ilevro er alle fraværende i årsrapporten for 2016 fra Novartis.
Intellektuel ejendom
Der er i øjeblikket syv amerikanske patenter, der er direkte forbundet med de moderniserede formuleringer af nepafenac, som alle stammer fra Novartis. Der er tre patenter forbundet med Nevanac, der stadig er aktive, og fire er forbundet med Ilevro. Det tidligste patent relateret til de moderne formuleringer af nepafenac blev godkendt den 11. juni 2002 efter indgivelse i 1999 af Bahram Asgharian. Et patent blev indgivet af Warren Wong, tilknyttet Alcon, Inc. med base i Fort Worth, Texas , den 2. december 2005 for vandige suspensioner af nepafenac. Et andet patent på et nepafenac-baseret lægemiddel blev indgivet den 8. maj 2006 af Geoffrey Owen, Amy Brooks og Gustav Graff. Et patent blev indgivet af Masood A. Chowhan og Huagang Chen den 9. februar 2007 og godkendt den 24. maj 2011, fulgt tæt af et patent indgivet af Warren Wong den 23. september 2010 og godkendt den 6. december 2011. Masood A. Chowhan, Malay Ghosh, Bahram Asgharian og Wesley Wehsin Han indgav endnu et patent den 1. december 2010 og blev godkendt den 30. december 2014. Det seneste patent blev indgivet af Masood A. Chowhan, Malay Ghosh, Bahram Asgharian og Wesley Weshin Han den 12. november 2014 og godkendt den 30. maj 2017. Disse patenter er gældende indtil datoer fra 17. juli 2018 til 31. marts 2032.
Novartis opretholder også patenter på nepafenac i 26 lande uden for USA.
Udfordringer
En sag blev anlagt af Alcon den 4. marts 2016 mod Watson Laboratories i Delaware for fremstilling af en generisk version af 0,3% nepafenac-formuleringen, Ilevro. Klagen blev ændret den 14. juni 2017.
Referencer
eksterne links
- "Nepafenac" . Lægemiddeloplysningsportal . US National Library of Medicine.
