Rifampicin - Rifampicin
 | |
 | |
| Kliniske data | |
|---|---|
| Udtale | / R ɪ f æ m p ə s ɪ n / |
| Handelsnavne | Rifadin, andre |
| Andre navne | Rifampin ( USAN USA ) |
| AHFS / Drugs.com | Monografi |
| MedlinePlus | a682403 |
| Licensdata | |
| Graviditet kategori |
|
| Ruter for administration |
Ved mund , IV |
| ATC -kode | |
| Lovlig status | |
| Lovlig status | |
| Farmakokinetiske data | |
| Biotilgængelighed | 90 til 95% (gennem munden) |
| Proteinbinding | 80% |
| Metabolisme | Lever og tarmvæg |
| Eliminering halveringstid | 3-4 timer |
| Udskillelse | Urin (~ 30%), afføring (60-65%) |
| Identifikatorer | |
| |
| CAS -nummer | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| CHEMBL | |
| NIAID ChemDB | |
| PDB -ligand | |
| CompTox Dashboard ( EPA ) | |
| ECHA InfoCard |
100.032.997 |
| Kemiske og fysiske data | |
| Formel | C 43 H 58 N 4 O 12 |
| Molar masse | 822,953 g · mol −1 |
| 3D -model ( JSmol ) | |
| Smeltepunkt | 183 til 188 ° C (361 til 370 ° F) |
| Kogepunkt | 937 ° C (1.719 ° F) |
| |
| |
|
| |
Rifampicin , også kendt som rifampin , er et antibiotikum, der bruges til at behandle flere typer bakterielle infektioner , herunder tuberkulose (TB), Mycobacterium avium -kompleks , spedalskhed og legionærsygdom . Det bruges næsten altid sammen med andre antibiotika med to bemærkelsesværdige undtagelser: når det gives som en "foretrukken behandling, der stærkt anbefales" til latent TB -infektion; og når det bruges som profylakse efter eksponering for at forhindre Haemophilus influenzae type b og meningokoksygdom hos mennesker, der har været udsat for disse bakterier. Inden behandling af en person i en længere periode anbefales målinger af leverenzymer og blodtællinger. Rifampicin kan gives enten gennem munden eller intravenøst.
Almindelige bivirkninger omfatter kvalme, opkastning, diarré og tab af appetit. Det får ofte urin, sved og tårer til at blive en rød eller orange farve. Leverproblemer eller allergiske reaktioner kan forekomme. Det er en del af den anbefalede behandling af aktiv tuberkulose under graviditeten, selvom dens sikkerhed under graviditeten ikke er kendt. Rifampicin er af gruppen rifamycin af antibiotika. Det virker ved at reducere produktionen af RNA af bakterier.
Rifampicin blev opdaget i 1965, markedsført i Italien i 1968 og godkendt i USA i 1971. Det er på Verdenssundhedsorganisationens liste over essentielle lægemidler . Verdenssundhedsorganisationen klassificerer rifampicin som kritisk vigtigt for humanmedicin. Det fås som en generisk medicin . Rifampicin fremstilles af jordbakterien Amycolatopsis rifamycinica .
Medicinske anvendelser
Mycobakterier
Rifampicin bruges til behandling af tuberkulose i kombination med andre antibiotika, såsom pyrazinamid , isoniazid og ethambutol . Til behandling af tuberkulose administreres det dagligt i mindst seks måneder. Kombinationsterapi bruges til at forhindre udvikling af resistens og for at forkorte behandlingens længde. Resistens af Mycobacterium tuberculosis mod rifampicin udvikler sig hurtigt, når det bruges uden et andet antibiotikum, med laboratorieestimater af resistenshastigheder fra 10 −7 til 10 −10 pr. Tuberkulosebakterie pr. Generation.
Rifampicin kan bruges alene til patienter med latente tuberkuloseinfektioner for at forhindre eller forlænge udviklingen af aktiv sygdom, fordi der kun er et lille antal bakterier til stede. En Cochrane-gennemgang fandt ingen forskel i effekt mellem en 3- til 4-måneders behandling med rifampicin og en 6-måneders behandling med isoniazid til forebyggelse af aktiv tuberkulose hos patienter, der ikke var inficeret med HIV, og patienter, der modtog rifampicin, havde en lavere hepatotoksicitet . Imidlertid blev kvaliteten af beviserne vurderet til at være lav. Et kortere 2-måneders forløb af rifampicin og pyrazinamid var tidligere blevet anbefalet, men det anbefales ikke længere på grund af høje hepatotoksiciteter.
Rifampicin skal tages på tom mave med et glas vand. Det tages generelt enten mindst en time før måltider eller 2 timer efter måltider.
Rifampicin bruges også til behandling af ikke -tuberkuløse mykobakterielle infektioner, herunder spedalskhed (Hansens sygdom) og Mycobacterium kansasii .
Med multidrug terapi anvendt som standardbehandling af Hansens sygdom, rifampicin altid i kombination med dapson og clofazimin ikke fremkalder lægemiddelresistens.
Det bruges også til behandling af Mycobacterium ulcerans infektioner i forbindelse med Buruli ulcer , normalt i kombination med clarithromycin eller andre antibiotika.
Andre bakterier og protozoer
I 2008 viste foreløbige beviser, at rifampicin kan være nyttigt til behandling af methicillinresistente Staphylococcus aureus ( MRSA ) i kombination med andre antibiotika, herunder i vanskeligt behandlede infektioner såsom osteomyelitis og proteseleddinfektioner. Fra 2012 var rifampicin -kombinationsbehandling nyttig ved pyogen vertebral osteomyelitis uklar. En metaanalyse konkluderede, at tilføjelse af supplerende rifampicin til et β-lactam eller vancomycin kan forbedre resultaterne ved stafylococcus aureus-bakteriæmi. Et nyere forsøg fandt imidlertid ingen fordel ved hjælp af supplerende rifampicin.
Det bruges også som forebyggende behandling mod Neisseria meningitidis ( meningokok ) infektioner. Rifampicin anbefales også som en alternativ behandling for infektioner med de flåtbårne patogener Borrelia burgdorferi og Anaplasma phagocytophilum, når behandling med doxycyclin er kontraindiceret, f.eks. Hos gravide kvinder eller hos patienter med en historie med allergi over for tetracyklinantibiotika.
Det bruges også nogle gange til at behandle infektioner af Listeria -arter, Neisseria gonorrhoeae , Haemophilus influenzae og Legionella pneumophila . For disse ikke -standardiserede indikationer bør antimikrobiel modtagelighedstest udføres (hvis det er muligt), før rifampicinbehandling påbegyndes.
Den Enterobacteriaceae , Acinetobacter -arter, og Pseudomonas arter er uløseligt resistente over for rifampicin.
Det er blevet brugt sammen med amphotericin B i stort set mislykkede forsøg på at behandle primær amøbisk meningoencephalitis forårsaget af Naegleria fowleri .
Rifampicin kan bruges som monoterapi i et par dage som profylakse mod meningitis, men resistens udvikler sig hurtigt under langvarig behandling af aktive infektioner, så stoffet bruges altid mod aktive infektioner i kombination med andre antibiotika.
Rifampicin er relativt ineffektivt mod spirocheter , hvilket har ført til dets anvendelse som et selektivt middel, der er i stand til at isolere dem i materialer, der dyrkes i laboratorier.
Vira
Rifampicin har en vis effektivitet mod vacciniavirus .
Følsomhed for patogener
De mindste hæmmende koncentrationer af rifampicin for flere medicinsk signifikante patogener er:
- Mycobacterium tuberculosis - 0,002 - 64 µg/ml
- Mycobacterium bovis - 0,125 µg/ml
- Staphylococcus aureus (methicillinresistent) - ≤ 0,006–256 µg/ml
- Chlamydia pneumoniae - 0,005 µg/ml
Primær galde cholangitis
Rifampicin bruges til at behandle kløe forårsaget af primær biliær cholangitis . De behandlingsrelaterede bivirkninger omfatter hepatotoksicitet , nefrotoksicitet , hæmolyse og interaktioner med andre lægemidler. Af disse årsager samt nogle etiske bekymringer vedrørende off-label brug af antibiotika anses rifampin som et meget effektivt forebyggende antibiotikum mod meningitis ikke at være egnet til kløe.
Hidradenitis suppurativa
Rifampicin med clindamycin er blevet brugt til behandling af hudsygdommen hidradenitis suppurativa .
Bivirkninger
Den alvorligste bivirkning er hepatotoksicitet, og folk, der modtager det, gennemgår ofte baseline og hyppige leverfunktionstests for at opdage tidlig leverskade.
De mere almindelige bivirkninger omfatter feber, gastrointestinale forstyrrelser, udslæt og immunologiske reaktioner. Indtagelse af rifampicin forårsager normalt, at visse kropsvæsker, såsom urin, sved og tårer, bliver orange-røde i farven, en godartet bivirkning, der ikke desto mindre kan være skræmmende, hvis det ikke forventes. Dette kan også bruges til at overvåge effektiv absorption af lægemidlet (hvis lægemidlets farve ikke ses i urinen, kan patienten ønske at flytte lægemiddeldosis længere i tid fra mad eller mælkeindtag). Misfarvningen af sved og tårer er ikke direkte mærkbar, men sved kan plette lys tøj orange, og tårer kan permanent plette bløde kontaktlinser. Da rifampicin kan udskilles i modermælk, bør amning undgås, mens det tages.
Andre negative virkninger omfatter:
- Levertoksicitet - hepatitis , leversvigt i alvorlige tilfælde
- Åndedrætsorganer - åndenød
- Kutan - rødme, kløe, udslæt, hyperpigmentering, rødme og vanding af øjnene
- Abdominal - kvalme , opkastning, mavekramper, diarré
- Influenzalignende symptomer- kuldegysninger, feber, hovedpine, artralgi og utilpashed . Rifampicin har god indtrængning i hjernen, og det kan direkte forklare en vis utilpashed og dysfori hos et mindretal af brugerne.
- Allergisk reaktion - udslæt, kløe, hævelse af tungen eller halsen, alvorlig svimmelhed og vejrtrækningsbesvær
Kemisk struktur
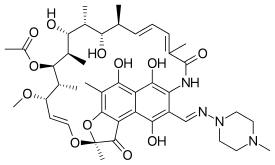
Rifampicin er et polyketid, der tilhører den kemiske klasse af forbindelser kaldet ansamyciner , så navngivet på grund af deres heterocykliske struktur, der indeholder en naphthoquinon -kerne, der er dækket af en alifatisk ansa -kæde. Den naphthoquinoniske chromofor giver rifampicin sin karakteristiske rødorange krystallinske farve.
De kritiske funktionelle grupper af rifampicin i dets hæmmende binding af bakteriel RNA -polymerase er de fire kritiske hydroxylgrupper i ansa -broen og naphtholringen, som danner hydrogenbindinger med aminosyrerester på proteinet.
Rifampicin er 3- (4-methyl-1-piperazinyl) -iminomethylderivatet af rifamycin SV .
Interaktioner
Rifampicin er den mest kraftfulde kendte inducer af det hepatiske cytochrom P450 -enzymsystem, herunder isoenzymer CYP2B6 , CYP2C8 , CYP2C9 , CYP2C19 , CYP3A4 , CYP3A5 og CYP3A7 . Det øger metabolismen af mange lægemidler og kan som en konsekvens gøre dem mindre effektive eller endda ineffektive ved at reducere deres niveauer. For eksempel skal patienter, der gennemgår langvarig antikoagulationsbehandling med warfarin, øge deres dosering af warfarin og få deres koagulationstid kontrolleret ofte, fordi undladelse af at gøre det kan føre til utilstrækkelig antikoagulation, hvilket kan resultere i alvorlige konsekvenser af tromboemboli.
Rifampicin kan reducere effekten af p -piller eller anden hormonel prævention ved sin induktion af cytokrom P450 -systemet, i det omfang utilsigtede graviditeter er forekommet hos kvinder, der bruger orale præventionsmidler og tog rifampicin selv ved meget korte forløb (f.eks. Som profylakse) mod eksponering for bakteriel meningitis).
Andre interaktioner omfatter nedsatte niveauer og mindre effektivitet af antiretrovirale midler , everolimus , atorvastatin , rosiglitazon , pioglitazon , celecoxib , clarithromycin , caspofungin , voriconazol og lorazepam .
Rifampicin er antagonistisk over for de mikrobiologiske virkninger af antibiotika gentamicin og amikacin. Aktiviteten af rifampicin mod nogle arter af mykobakterier kan forstærkes af isoniazid (gennem hæmning af mykolsyntese) og ambroxol (gennem værtstyrede effekter i autofagi og farmakokinetik).
Farmakologi
Handlingsmekanisme
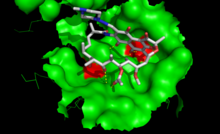
Rifampicin hæmmer bakteriel DNA-afhængig RNA-syntese ved at hæmme bakteriel DNA-afhængig RNA-polymerase .
Krystalstrukturdata og biokemiske data tyder på, at rifampicin binder til lommen af RNA -polymerase β -underenheden inden for DNA/RNA -kanalen, men væk fra det aktive sted. Inhibitoren forhindrer RNA -syntese ved fysisk at blokere forlængelse og dermed forhindre syntese af værtsbakterielle proteiner. Ved denne "sterisk okklusions" -mekanisme blokerer rifampicin syntesen af den anden eller tredje phosphodiesterbinding mellem nukleotiderne i RNA-rygraden og forhindrer forlængelse af 5'-enden af RNA-transkriptet forbi mere end 2 eller 3 nukleotider.
I en nylig undersøgelse blev Rifampicin vist at binde sig til cytochrom P450 reduktase og ændre dets konformation samt aktivitet i retning af at understøtte metabolisme af progesteron via CYP21A2 .
Modstandsmekanisme
Resistens over for rifampicin stammer fra mutationer, der ændrer rester af rifampicinbindingsstedet på RNA -polymerase, hvilket resulterer i nedsat affinitet for rifampicin. Resistensmutationer tilknyttes rpoB -genet, der koder for beta -underenheden af RNA -polymerase. Størstedelen af resistensmutationer i E. coli er i 3 klynger på rpoB . Klynge I er aminosyrer 509 til 533, klynge II er aminosyrer 563 til 572, og klynge III er aminosyre 687.
Når man beskriver mutationer i rpoB i andre arter, bruges det tilsvarende aminosyretal i E. coli normalt. I Mycobacterium tuberculosis er størstedelen af mutationer, der fører til rifampicinresistens, i klynge I i et 81bp hotspot -kerneområde kaldet RRDR for "rifampcin resistens bestemmende region". En ændring i aminosyre 531 fra serin til leucin som følge af en ændring i DNA -sekvensen af TCG til TTG er den mest almindelige mutation. Tuberkuloseresistens er også forekommet på grund af mutationer i den N-terminale region af rpoB og klynge III.
En alternativ resistensmekanisme er gennem Arr-katalyseret ADP-ribosylering af rifampicin. Med bistand af enzymet Arr produceret af patogenet Mycobacterium smegmatis , tilsættes ADP-ribose til rifampicin ved en af dens ansa kæde hydroxygrupper, derved inaktivere lægemidlet.
Modstand mod tuberkulose
Mykobakteriel resistens over for rifampicin kan forekomme alene eller sammen med resistens over for andre første linje antituberkulære lægemidler. Tidlig påvisning af en sådan multilægemiddel eller i vid udstrækning lægemiddelresistent tuberkulose er afgørende for at forbedre patientresultaterne ved at indføre passende andenlinjebehandlinger og reducere overførslen af lægemiddelresistent TB. Traditionelle metoder til påvisning af resistens involverer mykobakteriel kultur og test af modtagelighed for lægemidler, hvis resultater kan tage op til 6 uger. Xpert MTB/RIF assay er en automatiseret test, der kan påvise rifampicinresistens og også diagnosticere tuberkulose. En Cochrane -anmeldelse, der blev opdateret i 2014, konkluderede, at for rifampicin -resistensdetektion var Xpert MTB/RIF nøjagtig, det vil sige (95%) følsomt og (98%) specifikt.
Farmakokinetik
Oralt administreret rifampicin resulterer i maksimale plasmakoncentrationer på cirka 2-4 timer. 4-Aminosalicylsyre (et andet antituberkulosemedicin) reducerer absorptionen af rifampicin markant, og spidskoncentrationerne kan være lavere. Hvis disse to lægemidler skal bruges samtidigt, skal de gives separat, med et interval på 8 til 12 timer mellem administrationerne.
Rifampicin absorberes let fra mave -tarmkanalen (GI); dets esterfunktionelle gruppe hydrolyseres hurtigt i galde , og den katalyseres af en høj pH og substratspecifikke esteraser . Efter ca. 6 timer deacetyleres næsten alt lægemiddel. Selv i denne deacetylerede form er rifampicin stadig et potent antibiotikum; den kan imidlertid ikke længere reabsorberes af tarmene og elimineres fra kroppen. Kun ca. 7% af det administrerede lægemiddel udskilles uændret i urinen, selvom eliminering af urin kun tegner sig for ca. 30% af lægemiddeludskillelsen. Ca. 60% til 65% udskilles via afføring.
Den halveringstid af rifampicin i området fra 1,5 til 5,0 h, skønt nedsat leverfunktion øger den. Fødeforbrug hæmmer dets absorption fra mave -tarmkanalen, og stoffet elimineres hurtigere. Når rifampicin tages sammen med et måltid, falder dets maksimale blodkoncentration med 36%. Antacida påvirker ikke dets absorption. Faldet i rifampicinabsorption med mad er undertiden nok til at påvirke urinfarven mærkbart, hvilket kan bruges som en markør for, om en dosis af lægemidlet er blevet absorberet effektivt eller ej.
Distributionen af lægemidlet er høj i hele kroppen og når effektive koncentrationer i mange organer og kropsvæsker, herunder cerebrospinalvæsken . Da selve stoffet er rødt, er denne høje fordeling årsagen til spytets orange-røde farve, tårer, sved, urin og afføring. Ca. 60% til 90% af lægemidlet er bundet til plasmaproteiner.
Anvendelse inden for bioteknologi
Rifampicin hæmmer bakteriel RNA -polymerase, og det bruges derfor almindeligt til at hæmme syntesen af værtsbakterielle proteiner under rekombinant proteinekspression i bakterier. RNA, der koder for det rekombinante gen, transkriberes sædvanligvis fra DNA af en viral T7 RNA -polymerase , som ikke påvirkes af rifampicin.
Historie
I 1957 blev en jordprøve fra en fyrreskov på den franske riviera bragt til analyse til forskningslaboratoriet Lepetit Pharmaceuticals i Milano , Italien. Der opdagede en forskningsgruppe under ledelse af Piero Sensi og Maria Teresa Timbal en ny bakterie. Denne nye art producerede en ny klasse af molekyler med antibiotisk aktivitet. Fordi Sensi, Timbal og forskerne var særligt glade for den franske krimi Rififi (om en juvelhændelse og rivaliserende bander), besluttede de at kalde disse forbindelser for rifamyciner . Efter to års forsøg på at opnå mere stabile semisyntetiske produkter blev der i 1965 produceret et nyt molekyle med høj effektivitet og god tolerabilitet og fik navnet rifampicin.
Rifampicin blev først solgt i Italien i 1968 og blev godkendt af FDA i 1971.
Samfund og kultur
Kræftfremkaldende urenheder
I august 2020 blev US Food and Drug Administration (FDA) opmærksom på nitrosamin -urenheder i visse prøver af rifampin. FDA og producenterne undersøger oprindelsen af disse urenheder i rifampin, og agenturet udvikler testmetoder for regulatorer og industri for at opdage 1-methyl-4-nitrosopiperazin (MNP). MNP tilhører nitrosaminklassen af forbindelser, hvoraf nogle er klassificeret som sandsynlige eller mulige kræftfremkaldende stoffer fra mennesker (stoffer, der kan forårsage kræft), baseret på laboratorieundersøgelser som fx kræftfremkaldende undersøgelser af gnavere. Selv om der ikke er tilgængelige data til direkte vurdering af MNP's kræftfremkaldende potentiale, blev tilgængelige oplysninger om nært beslægtede nitrosaminforbindelser brugt til at beregne levetidseksponeringsgrænser for MNP.
Fra januar 2021 fortsætter FDA med at undersøge tilstedeværelsen af 1-methyl-4-nitrosopiperazin (MNP) i rifampin eller 1-cyclopentyl-4-nitrosopiperazin (CPNP) i rifapentin, der er godkendt til salg i USA.
Navne
Rifampicin er INN og BAN , mens rifampin er USAN . Rifampicin kan forkortes R, RMP, RA, RF eller RIF (US).
Rifampicin er også kendt som rifaldazin, rofact og rifampin i USA, også som rifamycin SV.
Dets kemiske navn er 5,6,9,17,19,21-hexahydroxy-23-methoxy-2,4,12,16,18,20,22-heptamethyl-8- [N- (4-methyl-1- piperazinyl) formimidoyl] -2,7- (epoxypentadeca [1,11,13] trienimino) -naphtho [2,1-b] furan-1,11 (2H) -dion 21-acetat.
Rifampicin er tilgængelig under mange mærker verden over.
Referencer
eksterne links
- "Rifampicin" . Lægemiddeloplysningsportal . US National Library of Medicine.