Spermatogenese - Spermatogenesis
| Spermatogenese | |
|---|---|
 Seminiferous tubule med modning af sæd. H & E plet .
| |
 En moden menneskelig Spermatozoon
| |
| Identifikatorer | |
| MeSH | D013091 |
| Anatomisk terminologi | |
Spermatogenesen er den proces, hvorved haploide spermatozoer udvikles fra kimceller i sædkanalerne i testis . Denne proces starter med den mitotiske opdeling af stamcellerne, der er placeret tæt på basulærmembranen i tubuli. Disse celler kaldes spermatogoniale stamceller . Den mitotiske opdeling af disse producerer to typer celler. Type A -celler genopfylder stamcellerne, og type B -celler differentieres til primære spermatocytter . Den primære spermatocyt opdeler meiotisk ( Meiose I) i to sekundære spermatocytter; hver sekundær spermatocyt deler sig i to lige haploide spermatider af Meiosis II. Sædcellerne omdannes til sædceller (sædceller) ved spermiogenese . Disse udvikler sig til modne sædceller, også kendt som sædceller . Således giver den primære spermatocyt anledning til to celler, de sekundære spermatocytter, og de to sekundære spermatocytter producerer ved deres opdeling fire spermatozoer og fire haploide celler.
Spermatozoer er de modne mandlige kønsceller i mange seksuelt reproducerende organismer. Således er spermatogenese den mandlige version af gametogenese , hvoraf den kvindelige ækvivalent er oogenese . Hos pattedyr forekommer det i de seminiferøse tubuli hos de mandlige testikler trinvist. Spermatogenese er meget afhængig af optimale betingelser for, at processen kan forekomme korrekt, og er afgørende for seksuel reproduktion . DNA -methylering og histonmodifikation har været impliceret i reguleringen af denne proces. Det starter i puberteten og fortsætter normalt uafbrudt indtil døden, selvom der kan ses et lille fald i mængden af produceret sædcelle med stigende alder (se Mandlig infertilitet ).
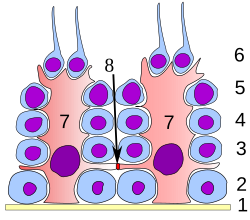
Spermatogenese starter i den nederste del af seminiferous rør og gradvist går celler dybere ned i rør og bevæger sig langs det, indtil modne spermatozoer når lumen, hvor modne spermatozoer afsættes. Opdelingen sker asynkront; hvis røret skæres på tværs, kunne man observere forskellige modningstilstande. En gruppe celler med forskellige modningstilstande, der genereres på samme tid, kaldes en spermatogen bølge.
Formål
Spermatogenese producerer modne mandlige kønsceller, almindeligvis kaldet sædceller, men mere specifikt kendt som sædceller , som er i stand til at befrugte modparten kvindelig kønscelle, oocytten , under undfangelsen for at producere et encellet individ kendt som en zygote . Dette er hjørnesten i seksuel reproduktion og involverer de to kønsceller, der begge bidrager med halvdelen af det normale sæt kromosomer ( haploide ) for at resultere i en kromosomalt normal ( diploid ) zygote.
For at bevare antallet af kromosomer i afkommet - som er forskelligt mellem arter - skal en af hver kønscelle have halvdelen af det sædvanlige antal kromosomer til stede i andre kropsceller. Ellers vil afkommet have det dobbelte af det normale antal kromosomer, og der kan opstå alvorlige abnormiteter. Hos mennesker resulterer kromosomale abnormiteter som følge af forkert spermatogenese i medfødte defekter og unormale fødselsdefekter ( Downs syndrom , Klinefelter syndrom ) og i de fleste tilfælde spontan abort af det udviklende foster.
Placering hos mennesker
Spermatogenese finder sted inden for flere strukturer i det mandlige reproduktive system . De indledende faser forekommer inden for testiklerne og går videre til epididymis, hvor de udviklende kønsceller modnes og opbevares indtil ejakulation . De sædkanalerne af testiklerne er udgangspunktet for denne proces, hvor spermatogonstamceller stamceller støder op til den indre tubulus væg kløft i en centripetal retning-begyndende ved væggene og procedure i den inderste del eller lumen -to producere umodne sædceller. Modning forekommer i epididymis. Placeringen [Testes/Scrotum] er specielt vigtig, da processen med spermatogenese kræver en lavere temperatur for at producere levedygtig sædcelle, specifikt 1 ° -8 ° C lavere end normal kropstemperatur på 37 ° C (98,6 ° F). Klinisk forårsager små udsving i temperaturen, f.eks. Fra en atletisk støttebælte, ingen nedsat levedygtighed eller tælling af sædceller.
Varighed
For mennesker anslås hele processen med spermatogenese forskelligt at tage 74 dage (ifølge tritiummærkede biopsier) og cirka 120 dage (ifølge DNA-urmålinger). Inklusive transport på ductal system tager det 3 måneder. Testikler producerer 200 til 300 millioner sædceller dagligt. Imidlertid bliver kun omkring halvdelen eller 100 millioner af disse levedygtige sædceller.
Niveauer
Hele processen med spermatogenese kan opdeles i flere forskellige stadier, der hver svarer til en bestemt celletype hos mennesker. I den følgende tabel er ploidi, kopiantal og kromosom/kromatidtællinger for en celle, generelt før DNA -syntese og division (i G1, hvis det er relevant). Den primære spermatocyt anholdes efter DNA -syntese og før deling.
| Celletype | ploidi /kromosomer hos mennesker | DNA -kopiantal/ kromatider hos mennesker | Proces indtastet af celle |
| spermatogonium (typer Ad, Ap og B) | diploid (2N) / 46 | 2C / 46 | spermatocytogenese ( mitose ) |
| primær spermatocyt | diploid (2N) / 46 | 4C / 2x46 | spermatidogenese (meiose I) |
| to sekundære spermatocytter | haploide (N) / 23 | 2C / 2x23 | spermatidogenese (meiose II) |
| fire spermatider | haploide (N) / 23 | C / 23 | spermiogenese |
| fire funktionelle spermatozoider | haploide (N) / 23 | C / 23 | spermiering |
Spermatocytogenese
Spermatocytogenese er den mandlige form for gametocytogenese og resulterer i dannelse af spermatocytter, der besidder halvdelen af det normale komplement af genetisk materiale. Ved spermatocytogenese deler et diploid spermatogonium , der ligger i basalrummet i de seminiferøse tubuli, mitotisk og producerer to diploide mellemliggende celler kaldet primære spermatocytter . Hver primære spermatocyt bevæger sig derefter ind i adluminalrummet i de seminiferøse tubuli og duplikerer dets DNA og undergår derefter meiose I for at producere to haploide sekundære spermatocytter , som senere igen vil opdele sig i haploide spermatider . Denne opdeling implicerer kilder til genetisk variation, såsom tilfældig inklusion af enten forældrekromosomer og kromosomisk crossover, der øger gamets genetiske variabilitet. Den DNA-skade respons (DDR) maskiner spiller en vigtig rolle i spermatogenesen. Proteinet FMRP binder sig til meiotiske kromosomer og regulerer dynamikken i DDR -maskineriet under spermatogenese. FMRP ser ud til at være nødvendig for reparation af DNA -skader .
Hver celledeling fra et spermatogonium til et spermatid er ufuldstændig; cellerne forbliver forbundet med hinanden af broer af cytoplasma for at tillade synkron udvikling. Ikke alle spermatogonier deler sig for at producere spermatocytter; ellers ville forsyningen af spermatogoni løbe tør. I stedet deler spermatogoniale stamceller mitotisk for at producere kopier af sig selv, hvilket sikrer en konstant forsyning af spermatogoni til brændstof af spermatogenese.
Spermatidogenese
Spermatidogenese er dannelsen af spermatider fra sekundære spermatocytter. Sekundære spermatocytter produceret tidligere kommer hurtigt ind i meiose II og deler sig for at producere haploide spermatider. Kortheden af dette stadie betyder, at sekundære spermatocytter sjældent ses i histologiske undersøgelser.
Spermiogenese
Under spermiogenese begynder spermatiderne at danne en hale ved at dyrke mikrotubuli på en af centriolerne, som bliver til basallegeme. Disse mikrotubuli danner et axonem . Senere ændres centriolen i processen med centrosomreduktion . Den forreste del af halen (kaldet midterstykke) tykner, fordi mitokondrier er arrangeret omkring axonem for at sikre energiforsyning. Spermatid DNA undergår også emballage og bliver stærkt kondenseret. DNA'et pakkes først med specifikke nukleare basiske proteiner, som efterfølgende erstattes med protaminer under forlængelse af spermatider. Det resulterende tætpakkede kromatin er transkriptionelt inaktivt. The Golgi-apparatet omgiver nu kondenseret kerne, bliver den acrosomet .
Modning sker derefter under påvirkning af testosteron, som fjerner den resterende unødvendige cytoplasma og organeller . Det overskydende cytoplasma, kendt som restlegemer , fagocyteres af omgivende Sertoli -celler i testiklerne . De resulterende spermatozoer er nu modne, men mangler motilitet. De modne spermatozoer frigives fra de beskyttende Sertoli -celler i lumen i det seminiferøse tubuli i en proces kaldet spermiering .
De ikke-bevægelige spermatozoer transporteres til epididymis i testikelvæske udskilt af Sertoli-cellerne ved hjælp af peristaltisk kontraktion . Mens i epididymis får sædcellerne motilitet og bliver i stand til befrugtning. Imidlertid opnås transport af de modne spermatozoer gennem resten af det mandlige reproduktive system via muskelsammentrækning frem for spermatozons nyligt erhvervede motilitet.
Sertoli -cellers rolle
På alle differentieringsstadier er de spermatogene celler i tæt kontakt med Sertoli -celler, som menes at give strukturel og metabolisk støtte til de udviklende sædceller. En enkelt Sertoli -celle strækker sig fra basalmembranen til lumen i tuben, selvom de cytoplasmatiske processer er vanskelige at skelne på det lysmikroskopiske niveau.
Sertoli -celler tjener en række funktioner under spermatogenese, de understøtter de udviklende gameter på følgende måder:
- Bevar det miljø, der er nødvendigt for udvikling og modning, via blod-testikelbarrieren
- Sekrete stoffer, der starter meiose
- Sekret understøttende testikelvæske
- Sekret androgenbindende protein (ABP), som koncentrerer testosteron i nærheden af de udviklende gameter
- Testosteron er nødvendig i meget store mængder til vedligeholdelse af reproduktive kanaler, og ABP tillader et meget højere frugtbarhedsniveau
- Sekrete hormoner, der påvirker hypofysekontrol af spermatogenese, især polypeptidhormonet, inhibin
- Fagocytose resterende cytoplasma tilbage fra spermiogenese
- Udskillelse af anti-müller-hormon forårsager forringelse af Müller-kanalen
- Beskyt spermatider mod hanens immunsystem via blod-testis-barrieren
- Bidrager til den spermatogontesten stamcelle niche
De intercellulære adhæsionsmolekyler ICAM-1 og opløselige ICAM-1 har antagonistiske virkninger på de tætte kryds, der danner blod-testis-barrieren. ICAM-2- molekyler regulerer spermatidadhæsion på den apikale side af barrieren (mod lumen ).
Indflydelsesfaktorer
Processen med spermatogenese er meget følsom over for udsving i miljøet, især hormoner og temperatur. Testosteron er påkrævet i store lokale koncentrationer for at opretholde processen, som opnås via binding af testosteron af androgenbindende protein til stede i seminiferous tubuli. Testosteron produceres af interstitielle celler, også kendt som Leydig -celler , som ligger ved siden af seminiferous tubuli.
Seminifer epitel er følsom over for forhøjet temperatur hos mennesker og nogle andre arter og vil blive påvirket negativt af temperaturer så høje som normale kropstemperaturer. Derfor er testiklerne placeret uden for kroppen i en hudpose kaldet pungen . Den optimale temperatur holdes ved 2 ° C ( mand ) (8 ° C mus ) under kropstemperatur. Dette opnås ved regulering af blodgennemstrømning og positionering mod og væk fra kroppens varme af den kremasteriske muskel og dartos glatte muskler i pungen.
En vigtig mekanisme er en termisk udveksling mellem testikelarterielle og venøse blodstrømme. Specialiserede anatomiske arrangementer består af to zoner med vikling langs den indre spermatiske arterie. Dette anatomiske arrangement forlænger kontakttiden og den termiske udveksling mellem testikelarteriel og venøs blodstrøm og kan til dels forklare temperaturgradienten mellem aorta- og testikelarterielblod rapporteret hos hunde og vædder. Desuden reduceres pulstrykket, der forekommer i den proksimale tredjedel af den indviklede længde af den indre spermatiske arterie. Desuden falder aktiviteten af spermatogen rekombinase, og dette formodes at være en vigtig faktor for testikeldegeneration.
Kostmangel (såsom vitamin B, E og A), anabolske steroider , metaller (cadmium og bly), røntgeneksponering, dioxin , alkohol og infektionssygdomme vil også påvirke spermatogeneses hastighed negativt. Derudover er den mandlige kønslinje modtagelig for DNA -skader forårsaget af oxidativt stress, og denne skade har sandsynligvis en betydelig indvirkning på befrugtning og graviditet. Eksponering for pesticider påvirker også spermatogenese.
Hormonel kontrol
Hormonal kontrol af spermatogenese varierer mellem arter. Hos mennesker er mekanismen ikke fuldstændig forstået; det er imidlertid kendt, at initiering af spermatogenese sker i puberteten på grund af samspillet mellem hypothalamus , hypofyse og Leydig -celler . Hvis hypofysen fjernes, kan spermatogenese stadig initieres af follikelstimulerende hormon (FSH) og testosteron . I modsætning til FSH synes luteiniserende hormon (LH) at have en lille rolle i spermatogenese uden for inducering af gonadal testosteronproduktion.
FSH stimulerer både produktionen af androgenbindende protein (ABP) af Sertoli-celler og dannelsen af blod-testis-barrieren . ABP er afgørende for at koncentrere testosteron i niveauer, der er høje nok til at starte og vedligeholde spermatogenese. Intratestikulære testosteronniveauer er 20-100 eller 50-200 gange højere end koncentrationen i blod, selvom der er variation over et 5- til 10-folds interval blandt raske mænd. FSH kan starte udskillelse af testosteron i testiklerne, men når det først er udviklet, kræves kun testosteron for at opretholde spermatogenese. Imidlertid øger niveauet af FSH øget produktion af spermatozoer ved at forhindre apoptose af type A spermatogoni . Hormonet inhibin virker til at reducere niveauerne af FSH. Undersøgelser fra gnavermodeller tyder på, at gonadotropiner (både LH og FSH) understøtter processen med spermatogenese ved at undertrykke de proapoptotiske signaler og derfor fremmer spermatogen celleoverlevelse.
Sertoli -cellerne medierer selv dele af spermatogenese gennem hormonproduktion. De er i stand til at producere hormonerne estradiol og inhibin. Leydig -cellerne er også i stand til at producere østradiol ud over deres hovedprodukt testosteron. Østrogen har vist sig at være afgørende for spermatogenese hos dyr. Imidlertid blev en mand med østrogenfølsomhedssyndrom (en defekt ERα ) fundet producere sædceller med et normalt sædtal , omend unormalt lav sædbarhed ; om han var steril eller ej, er uklart. For høje østrogenniveauer kan være skadelige for spermatogenese på grund af undertrykkelse af gonadotropinsekretion og i forlængelse heraf intratestikulær testosteronproduktion. Prolactin ser også ud til at være vigtig for spermatogenese.
Se også
Referencer
Yderligere læsning
- Okano, Tsukasa; Ishiniwa, Hiroko; Onuma, Manabu; Shindo, Junji; Yokohata, Yasushi; Tamaoki, Masanori (23. marts 2016). "Virkninger af miljøstråling på testikler og spermatogenese i vilde store japanske markmus (Apodemus speciosus) fra Fukushima" . Videnskabelige rapporter . 6 (1): 23601. Bibcode : 2016NatSR ... 623601O . doi : 10.1038/srep23601 . PMC 4804236 . PMID 27005329 .
- Johnson, L .; Blanchard, TL; Varner, DD; Scrutchfield, WL (november 1997). "Faktorer, der påvirker spermatogenese i hingsten". Teriogenologi . 48 (7): 1199–1216. doi : 10.1016/s0093-691x (97) 00353-1 . PMID 16728209 .
- Bardin, CW (1991). "Hypofyse-testikelakse". I Yen, SSC; Jaffee, RB (red.). Reproduktiv endokrinologi (3. udgave). Philadelphia: WB Saunders. ISBN 0721632068.
- Chambers, Christopher V .; Shafer, Mary-Ann; Adger, Hoover; Ohm-Smith, Marilyn; Millstein, Susan G .; Irwin, Charles E .; Schachter, Julius; Sweet, Richard (februar 1987). "Mikroflora i urinrøret hos unge drenge: Forhold til seksuel aktivitet og nongonokok urethritis". Journal of Pediatrics . 110 (2): 314–321. doi : 10.1016/s0022-3476 (87) 80180-4 . PMID 3100755 .
- Czyba, JC; Girod, C. (1980). "Udvikling af normale testikler". I Hafez, ESE (red.). Nedstigende og Cryptorchid Testis . Haag: Martinus Nijhoff. ISBN 9024723337.
- Whitmore, Willet F .; Karsh, Lawrence; Gittes, Ruben F. (oktober 1985). "Rollen af germinalepitel og spermatogenese i den privilegerede overlevelse af intratestikulære graft". Journal of Urology . 134 (4): 782–786. doi : 10.1016/s0022-5347 (17) 47438-6 . PMID 2863395 .