Transmembranprotein - Transmembrane protein
Et transmembranprotein ( TP ) er en type integreret membranprotein, der spænder over hele cellemembranen . Mange transmembrane proteiner fungerer som gateways for at tillade transport af specifikke stoffer hen over membranen. De gennemgår ofte betydelige konformationsændringer for at flytte et stof gennem membranen. De er normalt meget hydrofobe og tilsluttes og udfældes i vand. De kræver vaskemidler eller upolare opløsningsmidler til ekstraktion, selvom nogle af dem ( beta-tønder ) også kan ekstraheres ved hjælp af denatureringsmidler .
Den peptidsekvens , der spænder over membranen, eller det transmembrane segment , er stort set hydrofobe og kan visualiseres ved anvendelse af hydropatiafbildning . Afhængigt af antallet af transmembransegmenter kan transmembrane proteiner klassificeres som single-span (eller bitopic ) eller multi-span (polytopic). Nogle andre integrerede membranproteiner kaldes monotopiske , hvilket betyder, at de også er permanent fastgjort til membranen, men ikke passerer igennem den.
Typer
Klassificering efter struktur
Der er to grundlæggende typer transmembranproteiner: alfa-spiralformede og beta-tønder . Alfa-spiralformede proteiner er til stede i de indre membraner i bakterieceller eller plasmamembranen i eukaryote celler og undertiden i den bakterielle ydre membran . Dette er hovedkategorien af transmembrane proteiner. Hos mennesker er det anslået, at 27% af alle proteiner er alfa-spiralformede membranproteiner. Betatøndeproteiner findes indtil videre kun i ydre membraner af gramnegative bakterier , cellevægge af grampositive bakterier , ydre membraner i mitokondrier og kloroplaster eller kan udskilles som poredannende toksiner . Alle beta-tønde transmembrane proteiner har den enkleste op-og-ned topologi, som kan afspejle deres fælles evolutionære oprindelse og lignende foldemekanisme.
Ud over proteindomæner er der usædvanlige transmembrane elementer dannet af peptider. Et typisk eksempel er gramicidin A , et peptid, der danner en dimer transmembran β-helix. Dette peptid udskilles af grampositive bakterier som et antibiotikum . En transmembran polyprolin-II helix er ikke blevet rapporteret i naturlige proteiner. Ikke desto mindre blev denne struktur eksperimentelt observeret i specifikt designede kunstige peptider.
Klassificering efter topologi
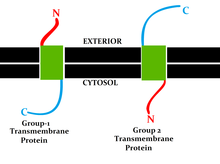
Denne klassifikation refererer til placeringen af proteinet N- og C-termini på de forskellige sider af lipid-dobbeltlaget . Type I, II, III og IV er single-pass molekyler . Type I transmembranproteiner er forankret til lipidmembranen med en stop-transfer ankersekvens og har deres N-terminale domæner målrettet mod det endoplasmatiske retikulum (ER) lumen under syntese (og det ekstracellulære rum, hvis modne former er placeret på cellemembraner ) . Type II og III er forankret med en signalanker-sekvens, hvor type II er målrettet mod ER-lumen med sit C-terminaldomæne, mens type III har deres N-terminale domæner målrettet mod ER-lumen. Type IV er opdelt i IV-A, med deres N-terminale domæner målrettet mod cytosol og IV-B, med et N-terminal domæne målrettet mod lumen. Implikationerne for opdelingen i de fire typer er især tydelige på tidspunktet for translokation og ER-bundet translation, når proteinet skal passeres gennem ER-membranen i en retning, der er afhængig af typen.
3D struktur
Membranproteinstrukturer kan bestemmes ved røntgenkrystallografi , elektronmikroskopi eller NMR-spektroskopi . De mest almindelige tertiære strukturer af disse proteiner er transmembran helix bundt og beta tønde . Den del af membranproteinerne, der er knyttet til lipid -dobbeltlaget (se ringformet lipidskal ) består hovedsageligt af hydrofobe aminosyrer.
Membranproteiner, der har hydrofobe overflader, er relativt fleksible og udtrykkes ved relativt lave niveauer. Dette skaber vanskeligheder med at få nok protein og derefter vokse krystaller. På trods af membranproteiners betydelige funktionelle betydning er det derfor vanskeligere at bestemme atomopløsningsstrukturer for disse proteiner end globulære proteiner. Fra januar 2013 var mindre end 0,1% af de bestemte proteinstrukturer membranproteiner på trods af at de var 20-30% af det totale proteom. På grund af denne vanskelighed og betydningen af denne klasse af proteiner metoder til forudsigelse af proteinstruktur baseret på hydropati -plots er den positive inderside -regel og andre metoder blevet udviklet.
Termodynamisk stabilitet og foldning
Stabilitet af alfa-spiralformede transmembrane proteiner
Transmembrane alfa-spiralformede (α-spiralformede) proteiner er usædvanligt stabile at dømme ud fra termiske denatureringsundersøgelser , fordi de ikke udfolder sig helt inden i membranerne (den komplette udfoldelse ville kræve nedbrydning af for mange α-spiralformede H-bindinger i de upolære medier). På den anden side folder disse proteiner let fejl på grund af ikke-native aggregering i membraner, overgang til de smeltede kugletilstande , dannelse af ikke-native disulfidbindinger eller udfoldelse af perifere regioner og ikke-regulære sløjfer, der er lokalt mindre stabile.
Det er også vigtigt at definere den udfoldede tilstand korrekt . Den udfoldede tilstand af membranproteiner i detergent- miceller er forskellig fra den i de termiske denaturering eksperimenter. Denne tilstand repræsenterer en kombination af foldede hydrofobe a-helixer og delvist udfoldede segmenter dækket af vaskemidlet. For eksempel har den "udfoldede" bakteriorhodopsin i SDS- miceller fire transmembrane a-helixer foldet, mens resten af proteinet er placeret ved micelle-vand-grænsefladen og kan adoptere forskellige typer ikke-native amfifile strukturer. Frie energiforskelle mellem sådanne detergent-denaturerede og native tilstande ligner stabiliteten af vandopløselige proteiner (<10 kcal/mol).
Foldning af α-spiralformede transmembrane proteiner
Refoldning af α-spiralformede transmembrane proteiner in vitro er teknisk svært. Der er relativt få eksempler på de vellykkede genfoldningsforsøg, som for bacteriorhodopsin . In vivo foldes alle sådanne proteiner normalt co-translationelt inden for den store transmembrane translokon . Translokon-kanalen tilvejebringer et yderst heterogent miljø for de spirende transmembrane a-helixer. En relativt polær amfifil α-helix kan adoptere en transmembranorientering i translokonen (selvom den ville være ved membranoverfladen eller udfoldet in vitro ), fordi dens polære rester kan vende mod translokonets centrale vandfyldte kanal. En sådan mekanisme er nødvendig for inkorporering af polære a-helixer i strukturer af transmembrane proteiner. De amfifile spiraler forbliver knyttet til translokonen, indtil proteinet er fuldstændigt syntetiseret og foldet. Hvis proteinet forbliver udfoldet og fastgjort til translokonen for længe, nedbrydes det af specifikke "kvalitetskontrol" cellulære systemer.
Stabilitet og foldning af beta-tønde transmembrane proteiner
Stabilitet af beta-tønde (β-tønde) transmembrane proteiner svarer til stabilitet af vandopløselige proteiner, baseret på kemiske denatureringsundersøgelser. Nogle af dem er meget stabile, selv i kaotropiske midler og høj temperatur. Deres foldning in vivo lettes af vandopløselige chaperoner , såsom protein Skp. Det menes, at β-tønde membranproteiner kommer fra en forfader, selv med et forskelligt antal ark, der kunne tilføjes eller fordobles under evolution. Nogle undersøgelser viser en enorm sekvensbevaring blandt forskellige organismer og også bevarede aminosyrer, der holder strukturen og hjælper med foldning.
3D strukturer
Letabsorberingsdrevne transportører
- Bacteriorhodopsin -lignende proteiner inklusive rhodopsin (se også opsin )
- Bakterielle fotosyntetiske reaktionscentre og fotosystemer I og II
- Lyshøstkomplekser fra bakterier og kloroplaster
Oxidoreduktionsdrevne transportører
- Transmembran cytochrom b -lignende proteiner: coenzym Q - cytochrom c reduktase (cytochrom bc1); cytokrom b6f -kompleks ; formiat dehydrogenase, respiratorisk nitratreduktase ; succinat - coenzym Q -reduktase (fumaratreduktase); og succinat dehydrogenase . Se elektrontransportkæde .
- Cytokrom c -oxidaser fra bakterier og mitokondrier
Elektrokemiske potentialdrevne transportører
- Proton- eller natriumtranslokerende F-type og V-type ATPaser
PP-bond hydrolysedrevne transportører
- P-type calcium ATPase (fem forskellige konformationer)
- Calcium ATPase -regulatorer phospholamban og sarcolipin
- ABC transportører
- General secretory pathway (Sec) translokon (preprotein translocase SecY)
Portører (uniporters, symporters, antiporters)
- Mitokondriale bærerproteiner
- Major Facilitator Superfamily (Glycerol-3-phosphat-transporter, laktose permease , og multimedikamenttransportøren EmrD)
- Resistens-nodulation-celledeling (multidrug efflux transportør AcrB, se multilægemodstand )
- Dicarboxylat/aminosyre: kation symporter (proton glutamat symporter)
- Monovalent kation/proton antiporter (Sodium/proton antiporter 1 NhaA)
- Neurotransmitter natrium symporter
- Ammoniak transportører
- Lægemiddel-/metabolittransportør (lille multiresistent transportør EmrE - strukturerne trækkes tilbage som fejlagtige)
Alfa-spiralformede kanaler inklusive ionkanaler
- Spændingsstyret ionkanal , herunder kaliumkanaler KcsA og KvAP, og indad-ensretter kaliumionkanal Kirbac
- Mekanosensitiv kanal med stor konduktans, MscL
- Mekanosensitiv ionkanal med lille konduktans (MscS)
- CorA metalion transportører
- Ligand-gated ion kanal af neurotransmitter receptorer ( acetylcholin receptor )
- Aquaporiner
- Kloridkanaler
- Ydre membran -hjælpeproteiner (polysaccharid -transportør) - α -spiralformede transmembranproteiner fra den ydre bakteriemembran
Enzymer
- Methanmonooxygenase
- Rhomboid protease
- Disulfidbindingsdannelsesprotein (DsbA-DsbB-kompleks)
Proteiner med alfa-spiralformede transmembranankre
- T -celle receptor transmembran dimeriseringsdomæne]
- Cytokrom c nitritreduktase kompleks
- Steryl-sulfat sulfohydrolase
- Stannin
- Glycophorin En dimer
- Inovirus ( filamentøs fag ) major coat protein
- Pilin
- Pulmonal overfladeaktivt stof -associeret protein
- Monoaminoxidaser A og B
- Fedtsyreamidhydrolase
- Cytokrom P450 oxidaser
- Corticosteroid 11β-dehydrogenases .
- Signalpeptidpeptidase
- Membranprotease specifik for en stomatinhomolog
Betatønder sammensat af en enkelt polypeptidkæde
- Betatønder fra otte beta-tråde og med et "forskydningsnummer" på ti ( n = 8, S = 10 ). De omfatter:
- OmpA-lignende transmembrane domæne (OmpA)
- Virulensrelateret ydre membranproteinfamilie (OmpX)
- Ydre membranprotein W -familie (OmpW)
- Antimikrobiel peptidresistens og lipid A -acyleringsproteinfamilie (PagP)
- Lipid A deacylase PagL
- Opacity familie porins (NspA)
- Autotransporter domæne ( n = 12, S = 14 )
- FadL ydre membranproteintransportfamilie , herunder fedtsyretransportør FadL ( n = 14, S = 14 )
- Generel bakteriel porinfamilie , kendt som trimeriske poriner ( n = 16, S = 20 )
- Maltoporin , eller sukker poriner ( n = 18, S = 22 )
- Nukleosidspecifik porin ( n = 12, S = 16 )
- Ydermembranphospholipase A1 ( n = 12, S = 16 )
- TonB-afhængige receptorer og deres plug-domæne . De er ligand-gated ydre membrankanaler ( n = 22, S = 24 ), herunder cobalamin transporter BtuB, Fe (III) -pyochelin receptor FptA, receptor FepA, ferric hydroxamat optagelsesreceptor FhuA, transportør FecA og pyoverdin receptor FpvA
- Ydre membranprotein OpcA familie ( n = 10, S = 12 ), der indbefatter ydre membran protease OmpT og adhæsin / invasindomæne OpcA protein
- Ydre membranprotein G porin familie ( n = 14, S = 16 )
Bemærk: n og S er henholdsvis antallet af beta-tråde og "forskydningsnummeret" for betatønderen
Betatønder sammensat af flere polypeptidkæder
- Trimerisk autotransportør ( n = 12, S = 12 )
- Ydre membranudstrømningsproteiner , også kendt som trimeriske ydre membranfaktorer (n = 12, S = 18) inklusive TolC- og multiresistensproteiner
- MspA porin (oktamer, n = S = 16 ) og a-hæmolysin (heptamer n = S = 14 ). Disse proteiner udskilles.


