Furan - Furan
|
|
|||
|
|
|||
| Navne | |||
|---|---|---|---|
|
Foretrukket IUPAC -navn
Furan |
|||
|
Systematisk IUPAC -navn
1,4-Epoxybuta-1,3-dien 1-Oxacyclopenta-2,4-dien |
|||
| Andre navne
Oxol
Oxa [5] annulen 1,4-Epoxy-1,3-butadien 5-Oxacyclopenta-1,3-dien 5-Oxacyclo-1,3-pentadien Furfuran Divinylenoxid |
|||
| Identifikatorer | |||
|
3D -model ( JSmol )
|
|||
| ChEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| ECHA InfoCard |
100.003.390 |
||
| KEGG | |||
|
PubChem CID
|
|||
| UNII | |||
|
CompTox Dashboard ( EPA )
|
|||
|
|||
|
|||
| Ejendomme | |||
| C 4 H 4 O | |||
| Molar masse | 68,075 g · mol −1 | ||
| Udseende | Farveløs, flygtig væske | ||
| Massefylde | 0,936 g/ml | ||
| Smeltepunkt | −85,6 ° C (−122,1 ° F; 187,6 K) | ||
| Kogepunkt | 31,3 ° C (88,3 ° F; 304,4 K) | ||
| -43,09 · 10 −6 cm 3 /mol | |||
| Farer | |||
| Sikkerhedsdatablad | Pennakem | ||
| R-sætninger (forældet) | R26/27/28 , R45 | ||
| S-sætninger (forældet) | S16 , S37 , S45 , S28 | ||
| NFPA 704 (brand diamant) | |||
| Flammepunkt | −36 ° C (−33 ° F; 237 K) | ||
| 390 ° C (734 ° F; 663 K) | |||
| Eksplosive grænser | Nedre: 2,3% Øvre: 14,3% ved 20 ° C |
||
| Dødelig dosis eller koncentration (LD, LC): | |||
|
LD 50 ( median dosis )
|
> 2 g/kg (rotte) | ||
| Relaterede forbindelser | |||
|
Relaterede heterocyklusser
|
Pyrrol Thiophene |
||
|
Relaterede forbindelser
|
Tetrahydrofuran (THF) 2,5-Dimethylfuran benzofuran dibenzofuran |
||
| Struktur | |||
| C 2v | |||
|
Medmindre andet er angivet, angives data for materialer i deres standardtilstand (ved 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Infobox referencer | |||
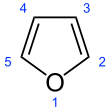
Furan er en heterocyklisk organisk forbindelse , der består af en fem-leddet aromatisk ring med fire carbon atomer og et oxygen atom. Kemiske forbindelser, der indeholder sådanne ringe, kaldes også furaner.
Furan er en farveløs, brandfarlig , meget flygtig væske med et kogepunkt tæt ved stuetemperatur. Det er opløseligt i almindelige organiske opløsningsmidler , herunder alkohol , ether og acetone , og er let opløseligt i vand . Dens lugt er "stærk, æterisk; chloroformlignende ". Det er giftigt og kan være kræftfremkaldende hos mennesker. Furan bruges som udgangspunkt for andre specialkemikalier .
Historie
Navnet "furan" kommer fra det latinske furfur , hvilket betyder klid . ( Furfural fremstilles af klid.) Det første furanderivat, der skulle beskrives, var 2-furonsyre , af Carl Wilhelm Scheele i 1780. Et andet vigtigt derivat, furfural , blev rapporteret af Johann Wolfgang Döbereiner i 1831 og karakteriseret ni år senere af John Stenhouse . Furan selv blev først fremstillet ved Heinrich Limpricht i 1870, selv om han kaldte det "tetraphenol" (som om det var en fire-carbon analog til phenol , C 6 H 6 O).
Produktion
Industrielt fremstilles furan ved palladiumkatalyseret decarbonylering af furfural eller ved kobberkatalyseret oxidation af 1,3 -butadien :
I laboratoriet kan furan fås fra furfural ved oxidation til 2-furonsyre efterfulgt af decarboxylering . Det kan også fremstilles direkte ved termisk nedbrydning af pentoseholdige materialer og celluloseholdige faste stoffer, især fyrretræ .
Syntese af furaner
Den Feist-Benary syntese er en klassisk måde at syntetisere furaner, selv om der er udviklet mange synteser. En af de enkleste syntesemetoder for furaner er reaktionen af 1,4-diketoner med phosphorpentoxid (P 2 O 5 ) i Paal-Knorr-syntesen . Den thiophen reaktionen, hvor 1,4-diketoner med Lawessons reagens danner også furaner som biprodukter. Der findes mange ruter til syntese af substituerede furaner.
Kemi
Furan er aromatisk fordi en af de lone pairs af elektroner på oxygenatomet er delokaliseret i ringen, hvilket skaber en 4 n + 2 aromatisk system (se Huckel regel ) svarende til benzen . På grund af aromatikken er molekylet fladt og mangler diskrete dobbeltbindinger . Det andet ensomme elektronpar i oxygenatomet strækker sig i plan for det flade ringsystem. Den sp 2 hybridisering er at tillade en af de enlige par af ilt til ophold i en p orbital og dermed gør det muligt at interagere i π-systemet .
På grund af sin aromatik er furans adfærd ganske forskellig fra den for de mere typiske heterocykliske etere, såsom tetrahydrofuran .
- Det er betydeligt mere reaktivt end benzen ved elektrofile substitutionsreaktioner på grund af elektrondonerende virkninger af oxygen-heteroatom. Undersøgelse af resonansbidragerne viser ringens øgede elektrontæthed, hvilket fører til øgede frekvenser af elektrofil substitution.
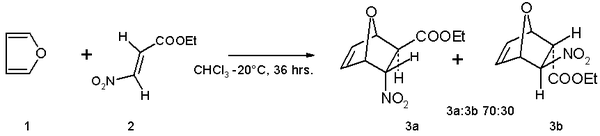
- Furan fungerer som dien i Diels-Alder-reaktioner med elektronmangel dienofiler, såsom ethyl ( E ) -3-nitroacrylat. Reaktionsproduktet er en blanding af isomerer med præference for endo -isomeren :
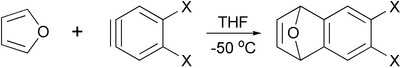
- Diels-Alder-reaktion af furan med arynes tilvejebringer tilsvarende derivater af dihydronaphthalener , som er nyttige mellemprodukter ved syntese af andre polycykliske aromatiske forbindelser .
- Hydrogenering af furaner giver i rækkefølge dihydrofuraner og tetrahydrofuraner .
- I Achmatowicz -reaktionen omdannes furaner til dihydropyranforbindelser .
- Pyrrol kan fremstilles industrielt ved at omsætte furan og ammoniak i nærvær af faste sure katalysatorer , såsom SiO 2 og Al 2 O 3 .
Sikkerhed
Furan findes i varmebehandlede kommercielle fødevarer og fremstilles ved termisk nedbrydning af naturlige fødevarekomponenter. Det kan findes i ristet kaffe , instant kaffe og forarbejdede babymad . Forskning har vist, at kaffe lavet i espressomaskine beslutningstagere og kaffe lavet af kapsler indeholder mere furan end der gjorde i traditionelle drop kaffemaskiner , selvom niveauerne er stadig inden for sikre sundhedsmæssige grænser.
Eksponering for furan i doser omkring 2.000 gange det forventede niveau for menneskelig eksponering fra fødevarer øger risikoen for hepatocellulære tumorer hos rotter og mus og galdegangstumorer hos rotter. Furan er derfor opført som et muligt kræftfremkaldende stof hos mennesker .
Se også
- BS 4994 - Furanharpiks som termohærdende FRP til udstyr til kemisk procesanlæg
- Furanocoumarin
- Furanoflavonoid
- Furanose
- Furantetracarboxylsyre
- Enkle aromatiske ringe
- Furan fedtsyrer
- Tetrahydrofuran