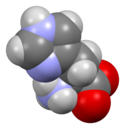
Histidin - Histidine

Skeletformel af histidin ( zwitterionisk form)
|
|||
|
|
|||
| Navne | |||
|---|---|---|---|
|
IUPAC navn
Histidin
|
|||
| Andre navne
2-Amino-3- (1 H- imidazol-4-yl) propansyre
|
|||
| Identifikatorer | |||
|
3D -model ( JSmol )
|
|||
| ChEBI | |||
| CHEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard |
100.000.678 |
||
| KEGG | |||
|
PubChem CID
|
|||
| UNII | |||
|
CompTox Dashboard ( EPA )
|
|||
|
|||
|
|||
| Ejendomme | |||
| C 6 H 9 N 3 O 2 | |||
| Molar masse | 155,157 g · mol −1 | ||
| 4,19 g/100 g ved 25 ° C | |||
| Farer | |||
| Sikkerhedsdatablad | Se: dataside | ||
| NFPA 704 (brand diamant) | |||
| Supplerende dataside | |||
|
Brydningsindeks ( n ), Dielektrisk konstant (ε r ) osv. |
|||
|
Termodynamiske
data |
Faseadfærd fast – flydende – gas |
||
| UV , IR , NMR , MS | |||
|
Medmindre andet er angivet, angives data for materialer i deres standardtilstand (ved 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Infobox referencer | |||
Histidin (symbol His eller H ) er en a-aminosyre, der bruges i biosyntesen af proteiner . Den indeholder en a-aminogruppe (som er i den protonerede –NH 3 + -form under biologiske forhold ), en carboxylsyregruppe (som er i den deprotonerede –COO - form under biologiske forhold) og en imidazolsidekæde (som er delvist protoneret), hvilket klassificerer det som en positivt ladet aminosyre ved fysiologisk pH . I første omgang menes det kun vigtigt for spædbørn, og det har nu vist sig i længerevarende undersøgelser, at det også er vigtigt for voksne. Det er kodet af kodonerne CAU og CAC.
Histidin blev først isoleret af den tyske læge Albrecht Kossel og Sven Gustaf Hedin i 1896. Det er også en forløber for histamin , et vigtigt inflammatorisk middel i immunresponser. Acyl -radikal er histidyl .
Egenskaber ved imidazolsidekæden
Konjugatsyren (protoneret form) af imidazol sidekæden i histidin har en p K en på ca. 6,0. Under en pH på 6 er imidazolringen for det meste protoneret (som beskrevet af Henderson -Hasselbalch -ligningen ). Den resulterende imidazoliumring bærer to NH -bindinger og har en positiv ladning. Den positive ladning er ligeligt fordelt mellem begge nitrogener og kan repræsenteres med to lige så vigtige resonansstrukturer . Over pH 6 går en af de to protoner tabt. Den resterende proton af imidazolringen kan ligge på enten nitrogen, hvilket giver anledning til, hvad der er kendt som N1-H eller N3-H tautomerer . N3-H-tautomeren, vist i figuren ovenfor, er protoneret på #3-nitrogenet, længere fra aminosyreskelettet, der bærer amino- og carboxylgrupperne, hvorimod N1-H-tautomeren er protoneret på nitrogenet tættere på rygraden. Imidazol/imidazoliumringen af histidin er aromatisk ved alle pH -værdier.
Syre-baseegenskaberne af imidazolsidekæden er relevante for den katalytiske mekanisme for mange enzymer . I katalytiske triader abstraherer det basiske nitrogen af histidin en proton fra serin , threonin eller cystein for at aktivere det som en nukleofil . I en histidin -proton -shuttle bruges histidin til hurtigt at transportere protoner. Det kan gøre dette ved at abstrahere en proton med dets basiske nitrogen for at lave et positivt ladet mellemprodukt og derefter bruge et andet molekyle, en buffer, til at ekstrahere protonen fra dets sure nitrogen. I carbonanhydraser , er en histidin proton shuttle anvendes til hurtigt shuttle protoner væk fra en zink -bundet vandmolekyle til hurtigt regenerere den aktive form af enzymet. I spiraler E og F af hæmoglobin påvirker histidin bindingen af dioxygen såvel som kulilte . Denne interaktion øger affiniteten af Fe (II) til O2, men destabiliserer bindingen af CO, som kun binder 200 gange stærkere i hæmoglobin sammenlignet med 20.000 gange stærkere i fri hæmning .
Tautomerismen og syre-baseegenskaberne af imidazolsidekæden er blevet karakteriseret ved 15 N NMR-spektroskopi. De to 15 N kemiske skift er ens (ca. 200 ppm i forhold til salpetersyre på sigma -skalaen, hvor øget afskærmning svarer til øget kemisk skift ). NMR- spektrale målinger viser, at det kemiske skift af N1-H falder en smule, hvorimod det kemiske skift af N3-H falder betydeligt (ca. 190 vs. 145 ppm). Denne ændring indikerer, at N1-H tautomeren foretrækkes, muligvis på grund af hydrogenbinding til det nærliggende ammonium . Afskærmningen ved N3 reduceres væsentligt på grund af den andenordens paramagnetiske virkning, som indebærer en symmetri-tilladt interaktion mellem nitrogen-ensomparret og de exciterede π* -tilstande i den aromatiske ring . Ved pH> 9 er de kemiske forskydninger af N1 og N3 cirka 185 og 170 ppm.
Ligand


Histidin danner komplekser med mange metalioner. Imidazolsidekæden af histidinresten fungerer almindeligvis som en ligand i metalloproteiner . Et eksempel er den aksiale base, der er knyttet til Fe i myoglobin og hæmoglobin. Poly-histidinmærker (med seks eller flere på hinanden følgende H-rester) anvendes til proteinrensning ved binding til søjler med nikkel eller kobolt med mikromolær affinitet. Naturlige poly-histidinpeptider, der findes i giften af hugormen Atheris squamigera, har vist sig at binde Zn (2+), Ni (2+) og Cu (2+) og påvirke funktionen af giftmetalloproteaser. Ydermere findes histidinrige områder med lav kompleksitet i metalbindende og især nikkel-koboltbindende proteiner.
Metabolisme
Biosyntese
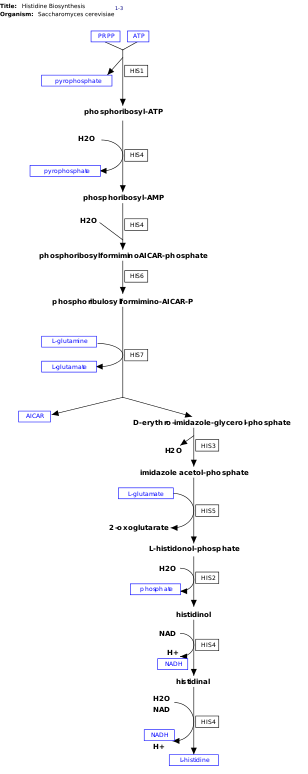
l -Histidin er en essentiel aminosyre, der ikke syntetiseres de novo hos mennesker. Mennesker og andre dyr skal indtage histidin eller histidinholdige proteiner. Biosyntesen af histidin er blevet bredt undersøgt i prokaryoter såsom E. coli . Histidinsyntese i E. coli involverer otte genprodukter (His1, 2, 3, 4, 5, 6, 7 og 8), og det sker i ti trin. Dette er muligt, fordi et enkelt genprodukt har evnen til at katalysere mere end én reaktion. For eksempel, som vist i stien, katalyserer His4 4 forskellige trin i vejen.
Histidin syntetiseres fra phosphoribosylpyrophosphat (PRPP), som er fremstillet af ribose-5-phosphat af ribose-phosphatdiphosphokinase i pentosefosfatvejen . Den første reaktion ved histidinbiosyntese er kondensering af PRPP og adenosintrifosfat (ATP) af enzymet ATP-phosphoribosyltransferase . ATP-phosphoribosyltransferase er angivet med His1 i billedet. His4-genproduktet hydrolyserer derefter produktet fra kondensationen, phosphoribosyl-ATP, der producerer phosphoribosyl-AMP (PRAMP), hvilket er et irreversibelt trin. His4 katalyserer derefter dannelsen af phosphoribosylformiminoAICAR-phosphat, som derefter omdannes til phosphoribulosylformimino-AICAR-P af His6-genproduktet. His7 deler phosphoribulosylformimino-AICAR-P for at danne d- erytro-imidazol-glycerol-phosphat. Herefter danner His3 imidazolacetol-phosphatfrigivende vand. His5 laver derefter l -histidinol -phosphat, som derefter hydrolyseres af His2, der fremstiller histidinol . His4 katalyserer oxidationen af l -histidinol til dannelse af l -histidinal, et aminoaldehyd. I det sidste trin, l -histidinal omdannes til l histidin.
Ligesom dyr og mikroorganismer har planter brug for histidin til deres vækst og udvikling. Mikroorganismer og planter ligner hinanden, idet de kan syntetisere histidin. Begge syntetiserer histidin fra det biokemiske mellemprodukt phosphoribosylpyrophosphat. Generelt er histidinbiosyntesen meget ens i planter og mikroorganismer.
Regulering af biosyntese
Denne vej kræver energi for at forekomme, derfor aktiverer tilstedeværelsen af ATP det første enzym i vejen, ATP-phosphoribosyltransferase (vist som His1 i billedet til højre). ATP-phosphoribosyltransferase er det hastighedsbestemmende enzym, som reguleres gennem feedbackinhibering, hvilket betyder, at det hæmmes i nærvær af produktet, histidin.
Nedbrydning
Histidin er en af de aminosyrer, der kan omdannes til mellemprodukter i tricarboxylsyre (TCA) cyklussen. Histidin, sammen med andre aminosyrer, såsom prolin og arginin, deltager i deaminering, en proces, hvor dets aminogruppe fjernes. I prokaryoter omdannes histidin først til urocanat af histidase. Derefter omdanner urocanase urocanat til 4-imidazolon-5-propionat. Imidazolonepropionase katalyserer reaktionen til dannelse af formiminoglutamat (FIGLU) fra 4-imidazolon-5-propionat. Formimino -gruppen overføres til tetrahydrofolat , og de resterende fem carbonatomer danner glutamat. Samlet set resulterer disse reaktioner i dannelsen af glutamat og ammoniak. Glutamat kan derefter deamineres af glutamatdehydrogenase eller transamineres til dannelse af a-ketoglutarat.
Omdannelse til andre biologisk aktive aminer
- Histidinaminosyren er en forløber for histamin , en amin produceret i kroppen, der er nødvendig for betændelse.
- Enzymet histidin-ammoniak-lyase omdanner histidin til ammoniak og urocansyre . En mangel på dette enzym er til stede i den sjældne metaboliske lidelse histidinæmi , der producerer urocanic aciduria som et vigtigt diagnostisk fund.
- Histidin kan omdannes til 3-methylhistidin , som fungerer som en biomarkør for skeletmuskulaturskader, ved hjælp af visse methyltransferase- enzymer.
- Histidin er også en forløber for carnosin biosyntese , som er et dipeptid, der findes i skeletmuskulaturen.
- I Actinobacteria og filamentøse svampe, såsom Neurospora crassa , kan histidin omdannes til antioxidanten ergothionein .
Krav
Food and Nutrition Board (FNB) fra US Institute of Medicine fastlagde anbefalede kosttilskud (RDA'er) for essentielle aminosyrer i 2002. For histidin, for voksne 19 år og ældre, 14 mg/kg legemsvægt/dag.
Se også
Referencer
eksterne links