Bugspytkirteløer - Pancreatic islets
| Pankreasøer/ holme af langerhans | |
|---|---|
 Bukspyttkjerteløerne er grupper af celler i bugspytkirtlen, der frigiver hormoner
| |
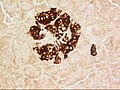
 En bugspytkirtelø fra en mus i en typisk position, tæt på et blodkar; insulin i rødt, kerner i blåt.
| |
| detaljer | |
| Del af | Bugspytkirtel |
| System | Endokrine |
| Identifikatorer | |
| Latin | insulae pancreaticae |
| MeSH | D007515 |
| TA98 | A05.9.01.019 |
| TA2 | 3128 |
| FMA | 16016 |
|
Anatomiske termer for mikroanatomi | |
De pancreasøer eller Langerhanske øer er regionerne i bugspytkirtlen , der indeholder dens endokrine (hormon-producerende) celler, opdaget i 1869 af tysk patologisk anatom Paul Langerhans . Pankreasøerne udgør 1-2% af bugspytkirtlen og modtager 10-15% af dets blodgennemstrømning. Pankreasøerne er arrangeret i densitetsruter i hele den menneskelige bugspytkirtel og er vigtige i metabolismen af glukose .
Struktur
Der er omkring 1 million øer fordelt i form af tæthedsruter gennem bugspytkirtlen hos et sundt voksent menneske, som hver måler i gennemsnit ca. 0,2 mm i diameter. : 928 Hver adskilles fra det omgivende bugspytkirtelvæv af en tynd fibrøs bindevævskapsel, der er kontinuerlig med det fibrøse bindevæv, der er sammenvævet i resten af bugspytkirtlen. : 928
Mikroanatomi
Hormoner produceret i bugspytkirtlen er udskilt direkte i blodgennemstrømningen af (mindst) fem typer celler. I rotteøer fordeles endokrine celletyper som følger:
- Alfa -celler, der producerer glucagon (20% af de samlede ø -celler)
- Betaceller , der producerer insulin og amylin (≈70%)
- Delta -celler, der producerer somatostatin (<10%)
- Epsilon -celler, der producerer ghrelin (<1%)
- PP -celler (gamma -celler eller F -celler), der producerer pancreatisk polypeptid (<5%)
Det er blevet anerkendt, at cytoarchitecturen i bugspytkirtlen er forskellige fra art til art. Især mens gnaverøer er karakteriseret ved en overvejende andel af insulinproducerende betaceller i klyngens kerne og ved knappe alfa-, delta- og PP-celler i periferien, viser menneskelige øer alfa- og betaceller i tæt forhold til hinanden i hele klyngen.
Andelen af betaceller i øer varierer afhængigt af arten, hos mennesker er det omkring 40-50%. Ud over endokrine celler er der stromaceller (fibroblaster), vaskulære celler (endotelceller, pericytter), immunceller (granulocytter, lymfocytter, makrofager, dendritiske celler) og neurale celler.
En stor mængde blod strømmer gennem øerne, 5-6 ml/min pr. 1 g ø. Det er op til 15 gange mere end i det eksokrine væv i bugspytkirtlen.
Øer kan påvirke hinanden gennem parakrin og autokrin kommunikation, og betaceller kobles elektrisk til seks til syv andre betaceller, men ikke til andre celletyper.
Fungere
Den parakrine feedback-system af pancreas-øerne har følgende struktur:
- Glukose/insulin: aktiverer betaceller og hæmmer alfaceller
- Glykogen/glukagon: aktiverer alfaceller, som aktiverer betaceller og deltaceller
- Somatostatin: hæmmer alfa -celler og betaceller
Et stort antal G-proteinkoblede receptorer (GPCR'er) regulerer udskillelsen af insulin, glucagon og somatostatin fra bugspytkirtlen, og nogle af disse GPCR'er er mål for lægemidler, der bruges til behandling af type-2-diabetes (ref GLP-1-receptoragonister, DPPIV -hæmmere).
Elektrisk aktivitet
Elektrisk aktivitet af bugspytkirteløerne er blevet undersøgt ved hjælp af patch clamp -teknikker. Det har vist sig, at cellernes adfærd i intakte øer adskiller sig væsentligt fra adspredte celler.
Klinisk betydning
Diabetes
De betaceller i de Langerhanske øer udskiller insulin , og så spille en væsentlig rolle i diabetes . Det menes, at de ødelægges af immunangreb. Dog er der også tegn på, at betaceller ikke er blevet ødelagt, men kun er blevet ikke-funktionelle.
Transplantation
Fordi betacellerne i bugspytkirtlen er selektivt ødelagt af en autoimmun proces ved type 1 -diabetes , forfølger klinikere og forskere aktivt øtransplantation som et middel til at genoprette den fysiologiske betacellefunktion, hvilket ville tilbyde et alternativ til en fuldstændig bugspytkirteltransplantation eller kunstig bugspytkirtel . Isletransplantation fremkom som en levedygtig mulighed for behandling af insulin, der kræver diabetes i begyndelsen af 1970'erne med en stabil fremgang i de følgende tre årtier. Nylige kliniske forsøg har vist, at insulinuafhængighed og forbedret metabolisk kontrol reproducerbart kan opnås efter transplantation af kadaveriske donorøer til patienter med ustabil type 1 -diabetes .
Personer med et højt kropsmasseindeks (BMI) er uegnede pancreasdonorer på grund af større tekniske komplikationer under transplantation. Det er imidlertid muligt at isolere et større antal øer på grund af deres større bugspytkirtel, og derfor er de mere egnede donorer af holme.
Isletransplantation involverer kun overførsel af væv bestående af betaceller, der er nødvendige som behandling af denne sygdom. Det repræsenterer således en fordel i forhold til hele bugspytkirteltransplantation, som er mere teknisk krævende og udgør en risiko for, at f.eks. Pancreatitis kan føre til organtab. En anden fordel er, at patienter ikke kræver generel anæstesi.
Øtransplantation for type 1 -diabetes kræver i øjeblikket kraftig immunsuppression for at forhindre værtafvisning af donorøer.
Øerne transplanteres i en portalåre , som derefter implanteres i leveren. Der er en risiko for portal venøs trombose og den lave værdi af holmeoverlevelse et par minutter efter transplantation, fordi den vaskulære tæthed på dette sted efter operationen er flere måneder lavere end i endogene øer. Således er neovaskularisering nøglen til holmeoverlevelse, der understøttes f.eks. Af VEGF produceret af øer og vaskulære endotelceller. Imidlertid har intraportal transplantation nogle andre mangler, og derfor undersøges andre alternative steder, der ville give et bedre mikromiljø for øerimplantation. Øtransplantationsforskning fokuserer også på ø-indkapsling, CNI-fri (calcineurin-hæmmer) immunosuppression, biomarkører for ø-skader eller mangel på donor-don.
En alternativ kilde til betaceller, sådanne insulinproducerende celler, der stammer fra voksne stamceller eller stamceller, ville bidrage til at overvinde manglen på donororganer til transplantation. Området for regenerativ medicin udvikler sig hurtigt og giver stort håb for den nærmeste fremtid. Type 1 -diabetes er imidlertid resultatet af den autoimmune ødelæggelse af betaceller i bugspytkirtlen. Derfor vil en effektiv kur kræve en sekventiel, integreret tilgang, der kombinerer tilstrækkelige og sikre immuninterventioner med betacelleregenerative tilgange. Det er også blevet påvist, at alfa -celler spontant kan skifte skæbne og transdifferentiere til betaceller i både raske og diabetiske øer i mennesker og mus i bugspytkirtlen, en mulig fremtidig kilde til regenerering af betaceller. Faktisk har det vist sig, at ø -morfologi og endokrin differentiering er direkte relateret. Endokrine stamceller differentieres ved at migrere i samhørighed og danne knoppelignende ø-forstadier eller "halvøer", hvor alfaceller udgør det halvøns ydre lag, og betaceller dannes senere under dem.
Yderligere billeder
Strukturelle forskelle mellem rotteøer (øverst) og menneskeøer (nederst) samt den ventrale del (venstre) og den dorsale del (højre) i bugspytkirtlen . Forskellige celletyper er farvekodede. Gnaverøer viser, i modsætning til de menneskelige, den karakteristiske insulinkerne .
Se også
- Betatrophin
- Neuroendokrin tumor
- Pankreas neuroendokrine tumor
- Adrift Just Off the Islets of Langerhans , en roman af Harlan Ellison