Cellestyrke - Cell potency
Cellepotentiale , baseret på Hans R. Schölers værker fra 2007 "The Potential of Stem Cells: An Inventory", er en celles evne til at differentiere sig til andre celletyper. Jo flere celletyper en celle kan differentiere sig til, jo større er dens styrke. Potens beskrives også som genaktiveringspotentialet i en celle, der ligesom et kontinuum begynder med totipotens for at betegne en celle med størst differentieringspotentiale, pluripotens , multipotens , oligopotens og endelig unipotens .

Totipotens
Totipotens (lat. Totipotentia, "evne til alle [ting]") er en enkelt celles evne til at dele og producere alle de differentierede celler i en organisme . Sporer og zygoter er eksempler på totipotente celler. I spektret af cellestyrke repræsenterer totipotens cellen med det største differentieringspotentiale , idet den er i stand til at differentiere sig til enhver embryonal celle såvel som ekstraembryoniske celler. I modsætning hertil kan pluripotente celler kun differentiere sig til embryonale celler.
Det er muligt for en fuldt differentieret celle at vende tilbage til en tilstand af totipotens. Denne konvertering til totipotens er kompleks, ikke fuldt ud forstået og genstand for nyere forskning. Forskning i 2011 har vist, at celler ikke kan differentiere sig til en fuldt totipotent celle, men i stedet til en "kompleks cellulær variation" af totipotens. Stamceller, der ligner totipotente blastomerer fra 2-cellestadieembryoer, kan opstå spontant i musens embryonale stamcellekulturer og kan også induceres til at opstå oftere in vitro gennem nedregulering af chromatinsamlingsaktiviteten af CAF-1 .
Den menneskelige udviklingsmodel er en, der kan bruges til at beskrive, hvordan totipotente celler opstår. Menneskelig udvikling begynder, når en sæd befrugter et æg, og det resulterende befrugtede æg skaber en enkelt totipotent celle, en zygote . I de første timer efter befrugtningen deler denne zygote sig i identiske totipotente celler, som senere kan udvikle sig til et af de tre kimlag af et menneske ( endoderm , mesoderm eller ektoderm ) eller i placenta celler ( cytotrophoblast eller syncytiotrophoblast ). Efter at have nået en 16-celle stadiet, de totipotente celler i morula differentiere til celler, som i sidste ende vil blive enten blastocyst 's indre cellemasse eller de ydre trofoblaster . Cirka fire dage efter befrugtning og efter flere cyklusser med celledeling begynder disse totipotente celler at specialisere sig. Den indre cellemasse, kilden til embryonale stamceller , bliver pluripotent.
Forskning om Caenorhabditis elegans tyder på, at flere mekanismer, herunder RNA -regulering, kan spille en rolle i at opretholde totipotens på forskellige udviklingsstadier hos nogle arter. Arbejde med zebrafisk og pattedyr tyder på et yderligere samspil mellem miRNA og RNA-bindende proteiner (RBP'er) ved bestemmelse af udviklingsforskelle.
Urkimceller
I muse primordial kimceller , genom -dækkende omprogrammering fører til totipotens indebærer sletning af epigenetiske aftryk. Omprogrammering letter ved aktiv DNA -demethylering, der involverer DNA -basen excision -reparationsenzymatisk vej. Denne vej medfører sletning af CpG- methylering (5mC) i urkimceller via den indledende omdannelse af 5mC til 5-hydroxymethylcytosin (5hmC), en reaktion drevet af høje niveauer af de ti-elleve dioxygenase-enzymer TET-1 og TET-2 .
Pluripotens
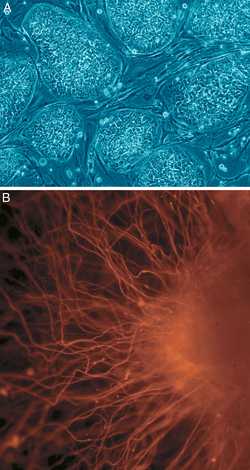
B: Nerve celler
I cellebiologi refererer pluripotens (Lat. Pluripotentia , "evne til mange [ting]") til en stamcelle, der har potentiale til at differentiere sig til et hvilket som helst af de tre kimlag : endoderm (indre maveforing, mave -tarmkanal, lunger) , mesoderm (muskel, knogle, blod, urogenital) eller ektoderm (epidermalt væv og nervesystem), men ikke i ekstra-embryonale væv som moderkagen. Cellepluripotens er imidlertid et kontinuum, der spænder fra den fuldstændigt pluripotente celle, der kan danne hver celle i det rigtige embryo, f.eks. Embryonale stamceller og iPSC'er (se nedenfor), til den ufuldstændigt eller delvist pluripotente celle, der kan danne celler af alle tre kimlag, men det udviser muligvis ikke alle egenskaberne ved fuldstændigt pluripotente celler.
Fremkaldt pluripotens
Inducerede pluripotente stamceller, almindeligvis forkortet som iPS-celler eller iPSC'er, er en type pluripotente stamceller, der kunstigt stammer fra en ikke-pluripotent celle, typisk en voksen somatisk celle , ved at inducere et "tvunget" udtryk for visse gener og transkriptionsfaktorer . Disse transkriptionsfaktorer spiller en central rolle i bestemmelsen af disse cellers tilstand og fremhæver også det faktum, at disse somatiske celler bevarer den samme genetiske information som tidlige embryonale celler. Evnen til at inducere celler til en pluripotent tilstand blev oprindeligt banebrydende i 2006 ved hjælp af musefibroblaster og fire transkriptionsfaktorer, Oct4 , Sox2 , Klf4 og c- Myc ; denne teknik, kaldet omprogrammering , gav senere Shinya Yamanaka og John Gurdon Nobelprisen i fysiologi eller medicin. Dette blev derefter fulgt i 2007 af den vellykkede induktion af humane iPSC'er afledt af humane dermale fibroblaster ved hjælp af metoder svarende til dem, der blev brugt til induktion af museceller. Disse inducerede celler udviser lignende egenskaber som embryonale stamceller (ESC'er), men kræver ikke brug af embryoner. Nogle af lighederne mellem ESC'er og iPSC'er omfatter pluripotens , morfologi , evne til selvfornyelse, et træk, der indebærer, at de kan dele sig og replikere på ubestemt tid og genekspression .
Epigenetiske faktorer menes også at være involveret i selve omprogrammeringen af somatiske celler for at fremkalde pluripotens. Det er blevet teoretiseret, at visse epigenetiske faktorer faktisk kan fungere for at rydde de originale somatiske epigenetiske mærker for at erhverve de nye epigenetiske mærker, der er en del af at opnå en pluripotent tilstand. Chromatin er også reorganiseret i iPSC'er og bliver som det, der findes i ESC'er, ved at det er mindre kondenseret og derfor mere tilgængeligt. Eukromatin modifikationer er også almindelige som også er i overensstemmelse med tilstanden af eukromatin fundet i sektorrådene.
På grund af deres store lighed med ESC'er har iPSC'er været af stor interesse for det medicinske og forskningsmiljø. iPSC'er kan potentielt have de samme terapeutiske implikationer og anvendelser som ESC'er, men uden den kontroversielle brug af embryoner i processen, et emne for stor bioetisk debat. Faktisk blev den inducerede pluripotens af somatiske celler i udifferentierede iPS -celler oprindeligt hyldet som afslutningen på den kontroversielle anvendelse af embryonale stamceller . Imidlertid viste det sig, at iPSC'er var potentielt tumorigene , og på trods af fremskridt blev de aldrig godkendt til klinisk faseundersøgelse i USA. Der er også stødt på tilbageslag som lave replikationshastigheder og tidlig ældning ved fremstilling af iPSC'er, hvilket forhindrer deres anvendelse som udskiftninger af ESC'er.
Derudover er det blevet bestemt, at den somatiske ekspression af kombinerede transkriptionsfaktorer direkte kan fremkalde andre definerede somatiske celleskæbner ( transdifferentiering ); forskere identificerede tre neurale slægtsspecifikke transkriptionsfaktorer, der direkte kunne konvertere musefibroblaster (hudceller) til fuldt funktionelle neuroner . Dette resultat udfordrer den terminale karakter af celledifferentiering og integriteten af slægtskabsengagement; og indebærer, at med de rigtige værktøjer er alle celler totipotente og kan danne alle slags væv.
Nogle af de mulige medicinske og terapeutiske anvendelser for iPSC'er, der stammer fra patienter, inkluderer deres anvendelse i celle- og vævstransplantationer uden risiko for afvisning, som man ofte støder på. iPSC'er kan potentielt erstatte dyremodeller, der er uegnede, såvel som in vitro -modeller, der bruges til sygdomsforskning.
Naive vs. primede pluripotensstilstande
Nylige fund med hensyn til epiblaster før og efter implantation har frembragt forslag til klassificering af pluripotens i to forskellige faser: "naiv" og "primet". Grundlinjestamcellerne, der almindeligvis bruges i videnskaben, der omtales som embryonale stamceller (ESC'er), stammer fra en præimplantation epiblast; sådan epiblast er i stand til at generere hele fosteret, og en epiblast -celle er i stand til at bidrage til alle cellelinier, hvis den injiceres i en anden blastocyst. På den anden side kan der observeres adskillige markante forskelle mellem præ- og postimplantation-epiblasterne, såsom deres forskel i morfologi, hvor epiblasten efter implantation ændrer sin morfologi til en koplignende form kaldet "æggecylinderen" som samt kromosomændring, hvor et af X-kromosomerne under tilfældig inaktivering i æggecylinderens tidlige stadie, kendt som X-inaktivering . Under denne udvikling målrettes æggecylinderens epiblast -celler systematisk af fibroblast -vækstfaktorer , Wnt -signalering og andre induktive faktorer via den omgivende æggeblommesæk og trofoblastvævet, således at de bliver instruktivt specifikke i henhold til den rumlige organisation.
En anden stor forskel, der blev observeret med hensyn til cellestyrke, er, at epiblast-stamceller efter implantation ikke er i stand til at bidrage til blastocyst- kimærer , som adskiller dem fra andre kendte pluripotente stamceller. Cellelinjer afledt af sådanne epiblaster efter implantation omtales som epiblast-afledte stamceller, der først blev afledt i laboratoriet i 2007; trods deres nomenklatur, at både økonomiske og sociale råd EpiSCs er afledt epiblasts, bare på forskellen udviklingsfaser, og at pluripotens er stadig intakt i den post-implantation epiblastcelle som påvist ved den konserverede ekspression af Nanog , Fut4 , og Oct-4 i EpiSC'er, indtil somitogenese og kan vendes midtvejs gennem induceret ekspression af Oct-4 .
Indfødt pluripotens i planter
I rødder
Uinduceret pluripotens er blevet observeret i rodmeristemvævskultur , især af Kareem et al 2015, Kim et al 2018 og Rosspopoff et al 2017. Denne pluripotens reguleres af forskellige regulatorer, herunder PLETHORA 1 og PLETHORA 2 ; og overflod 3 , overflod 5 , og overflod 7 , hvis ekspression blev fundet af Kareem at være auxin -provoked. (Disse er også kendt som PLT1, PLT2, PLT3, PLT5, PLT7 og udtrykt med gener med samme navne). Fra og med 2019 forventes dette at åbne op for fremtidig forskning i pluripotens i rodvæv.
Multipotens
Multipotens beskriver stamceller, der har genaktiveringspotentialet til at differentiere til adskilte celletyper. For eksempel en multipotent blod kan stamcelle -og denne celletype differentiere sig i flere typer af blodlegemer ligesom lymfocytter , monocytter , neutrofiler osv, men det er stadig usikkert, om HSC besidder evnen til at differentiere til hjerneceller , knogleceller eller andre typer ikke-blodlegemer.
Ny forskning relateret til multipotente celler tyder på, at multipotente celler kan være i stand til at konvertere til ikke -relaterede celletyper. I et andet tilfælde blev humane navlestrengsblodstamceller omdannet til humane neuroner. Forskning fokuserer også på at konvertere multipotente celler til pluripotente celler.
Multipotente celler findes i mange, men ikke alle humane celletyper. Multipotente celler er fundet i ledningsblod , fedtvæv, hjerteceller, knoglemarv og mesenkymale stamceller (MSC'er), som findes i den tredje molar .
MSC'er kan vise sig at være en værdifuld kilde til stamceller fra kindtænder i 8-10 års alderen, før voksen tandkalkning. MSC'er kan differentiere sig til osteoblaster, chondrocytter og adipocytter.
Oligopotens
I biologi er oligopotens stamcellernes evne til at differentiere sig til få celletyper . Det er en grad af styrke . Eksempler på oligopotente stamceller er lymfoide eller myeloide stamceller. En lymfoid celle specifikt kan give anledning til forskellige blodlegemer såsom B- og T -celler, dog ikke til en anden blodcelletype som en rød blodlegeme. Eksempler på stamceller er vaskulære stamceller, der har kapacitet til at blive både endotel- eller glatte muskelceller.
Enmagt
I cellebiologi er en unipotent celle konceptet om, at en stamcelle har kapacitet til kun at differentiere sig til én celletype. Det er i øjeblikket uklart, om der findes ægte unipotente stamceller. Hepatoblaster, der differentieres til hepatocytter (som udgør det meste af leveren ) eller cholangiocytter (galdegangens epitelceller), er bipotente. Et tæt synonym for unipotent celle er forstadiecelle .


