Natriumthiosulfat - Sodium thiosulfate

|
|
|
|

|
|
| Navne | |
|---|---|
|
IUPAC navn
Natriumthiosulfat
|
|
| Andre navne
Natriumhyposulfit
Hyposulfit af sodavand |
|
| Identifikatorer | |
|
3D -model ( JSmol )
|
|
| ChEBI | |
| CHEMBL | |
| ChemSpider | |
| ECHA InfoCard |
100.028.970 |
| E -nummer | E539 (surhedsregulatorer, ...) |
|
PubChem CID
|
|
| RTECS nummer | |
| UNII | |
|
CompTox Dashboard ( EPA )
|
|
|
|
|
|
| Ejendomme | |
|
Na 2S 2O 3 |
|
| Molar masse | 158,11 g/mol (vandfri) 248,18 g/mol (pentahydrat) |
| Udseende | Hvide krystaller |
| Lugt | Lugtfri |
| Massefylde | 1.667 g/cm 3 |
| Smeltepunkt | 48,3 ° C (118,9 ° F; 321,4 K) (pentahydrat) |
| Kogepunkt | 100 ° C (212 ° F; 373 K) (pentahydrat, - 5H 2 O sønderdeling) |
| 20,1 g/100 ml (20 ° C) 231 g/100 ml (100 ° C) |
|
| Opløselighed | ubetydelig i alkohol |
|
Brydningsindeks ( n D )
|
1.489 |
| Struktur | |
| monoklinisk | |
| Farer | |
| Sikkerhedsdatablad | Eksternt datablad |
| R-sætninger (forældet) | R21 R36 R37 R38 |
| NFPA 704 (brand diamant) | |
| Flammepunkt | Ikke-brændbar |
| Relaterede forbindelser | |
|
Andre kationer
|
Thiosvovlsyre Lithium thiosulfat kaliumthiosulfat |
|
Medmindre andet er angivet, angives data for materialer i deres standardtilstand (ved 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Infobox -referencer | |
Natriumthiosulfat ( natriumthiosulfat ) er en uorganisk forbindelse med formlen Na 2 S 2 O 3 . x H 2 O. Typisk er tilgængeligt som hvidt eller farveløst pentahydrat , Na 2 S 2 O 3 · 5 H 2 O . Det faste stof er et udblusende (taber let vand) krystallinsk stof, der opløses godt i vand.
Natriumthiosulfat bruges i guld minedrift , vandbehandling , analytisk kemi , udvikling af sølv -baseret fotografiske film og aftryk , og medicin . De medicinske anvendelser af natriumthiosulfat omfatter behandling af cyanidforgiftning og pityriasis . Det er på Verdenssundhedsorganisationens liste over essentielle lægemidler , de sikreste og mest effektive lægemidler, der er nødvendige i et sundhedssystem .
Anvendelser
Natriumthiosulfat anvendes hovedsageligt i industrien. For eksempel bruges det til at konvertere farvestoffer til deres opløselige leuco -form. Det bruges også til at blegge "uld, bomuld, silke, ... sæber, lim, ler, sand, bauxit og ... spiselige olier, spiselige fedtstoffer og gelatine."
Medicinske anvendelser
Natriumthiosulfat bruges til behandling af cyanidforgiftning . Andre anvendelser omfatter topisk behandling af ringorm og tinea versicolor og behandling af nogle bivirkninger af hæmodialyse og kemoterapi .
Fotografisk behandling
Sølvhalogenider , f.eks. AgBr , typiske komponenter i fotografiske emulsioner, opløses ved behandling med vandigt thiosulfat. Denne applikation som fotografisk fixer blev opdaget af John Herschel . Det bruges til både film- og fotografisk papirbehandling ; natriumthiosulfatet er kendt som en fotografisk fixer og omtales ofte som 'hypo' fra det oprindelige kemiske navn, hyposulfit af sodavand. Ammoniumthiosulfat foretrækkes typisk frem for natriumthiosulfat til denne anvendelse.
Neutralisering af chloreret vand
Det bruges til at dechlorere postevand, herunder sænkning af klorniveauer til brug i akvarier, svømmebassiner og kurbade (f.eks. Efter superchlorering ) og inden for vandbehandlingsanlæg til behandling af bundfældet skyllevand, før det slippes ud i floder. Reduktionsreaktionen er analog med iodreduktionsreaktionen.
Ved pH- test af blegemiddelstoffer neutraliserer natriumthiosulfat de farve-fjernende virkninger af blegemiddel og gør det muligt at teste pH-værdien af blegemiddelopløsninger med flydende indikatorer. Den relevante reaktion ligner jodreaktionen: thiosulfat reducerer hypochloritten (aktiv ingrediens i blegemiddel ) og oxideres derved til sulfat. Den fulde reaktion er:
- 4 NaClO + Na
2S
2O
3 + 2 NaOH → 4 NaCl + 2 Na
2SÅ
4 + H
2O
På samme måde reagerer natriumthiosulfat med brom og fjerner det frie brom fra opløsningen. Opløsninger af natriumthiosulfat bruges almindeligvis som en sikkerhedsforanstaltning i kemilaboratorier ved arbejde med brom og til sikker bortskaffelse af brom, jod eller andre stærke oxidationsmidler.
Struktur
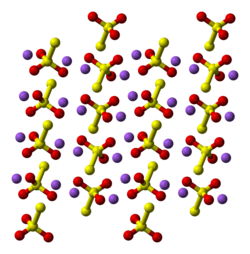
To polymorfer kendes om pentahydratet. Det vandfrie salt findes i flere polymorfer. I fast tilstand, den thiosulfat anionen er sige tetraedrisk i form og teoretisk afledt ved at erstatte et af de oxygenatomer med et svovlatom i en sulfat -anion. SS-afstanden angiver en enkelt binding, hvilket indebærer, at det terminale svovl har en betydelig negativ ladning, og SO-interaktionerne har mere dobbeltbindingskarakter.
Produktion
På industriel skala fremstilles natriumthiosulfat hovedsageligt fra flydende affaldsprodukter fra fremstilling af natriumsulfid eller svovlfarvestof .
I laboratoriet kan dette salt fremstilles ved opvarmning af en vandig opløsning af natriumsulfit med svovl eller ved kogning af vandigt natriumhydroxid og svovl i henhold til denne ligning:
- 6 NaOH + 4 S → 2 Na
2S + Na
2S
2O
3 + 3 H
2O
Hovedreaktioner
Ved opvarmning til 300 ° C, det dekomponerer til natriumsulfat og natrium polysulfid :
- 4 Na
2S
2O
3 → 3 Na
2SÅ
4 + Na
2S
5
Thiosulfatsalte nedbrydes karakteristisk ved behandling med syrer. Indledende protonation sker ved svovl. Når protonering udføres i diethylether ved -78 ° C, H 2 S 2 O 3 ( thiosvovlsyre fås). Det er en noget stærk syre med pK a s på 0,6 og 1,7 for henholdsvis den første og anden dissociation.
Under normale forhold resulterer forsuring af opløsninger af dette saltoverskud med selv fortyndede syrer i fuldstændig nedbrydning til svovl , svovldioxid og vand :
- Na
2S
2O
3 + 2 HCl → 2 NaCl + "S" + SO
2 + H
2O
Denne reaktion er kendt som en " urreaktion ", for når svovlet når en bestemt koncentration, bliver opløsningen fra farveløs til en lysegul. Denne reaktion er blevet anvendt til at danne kolloidt svovl. Denne proces bruges til at demonstrere begrebet reaktionshastighed i kemiklasser.
Koordineringskemi
Thiosulfat er en potent ligand for bløde metalioner. En typisk kompleks er [Pd (S 2 O 3 ) 2 ( ethylendiamin )] 2- , som har et par af S-bundet thiosulfat- ligander. Natriumthiosulfat og ammoniumthiosulfat er blevet foreslået som alternative afføringsmidler til cyanid til ekstraktion af guld . Fordelene ved denne fremgangsmåde er, at (i) thiosulfat er langt mindre toksisk end cyanid og (ii) at malmtyper, der er ildfaste for guldcyanisering (f.eks. Kulstofholdige eller Carlin-type malme ) kan udvaskes af thiosulfat. Nogle problemer med denne alternative proces omfatter det høje forbrug af thiosulfat og manglen på en passende genvindingsteknik, da [Au (S
2O
3)
2] 3− adsorberes ikketil aktivt kul , som er standardteknikken, der anvendes i guldcyanidation til at adskille guldkomplekset fra malmopslæmningen.
Jodometri
I analytisk kemi kommer den vigtigste anvendelse, fordi thiosulfatanionen reagerer støkiometrisk med jod i vandig opløsning, hvilket reducerer det til iodid, da thiosulfatet oxideres til tetrathionat :
- 2 S
2O2−
3 + Jeg
2 → S
4O2−
6 + 2 I-
På grund af denne reaktions kvantitative karakter, såvel som fordi Na
2S
2O
3· 5H 2 O har en fremragende holdbarhed, det bruges som titreringsmiddel i jodometri . Na
2S
2O
3· 5H 2 O er også en bestanddel af jod ur eksperimenter.
Denne særlige anvendelse kan konfigureres til at måle iltindholdet i vand gennem en lang række reaktioner i Winkler -testen for opløst ilt . Det bruges også til at estimere volumenmæssigt koncentrationerne af visse forbindelser i opløsning (f.eks. Hydrogenperoxid ) og til at estimere chlorindholdet i kommercielt blegepulver og vand.
Aluminium kation reaktion
Natriumthiosulfat bruges i analytisk kemi . Det kan, når det opvarmes med en prøve indeholdende aluminiumkationer, producere et hvidt bundfald:
- 2 Al 3+ + 3 S
2O2−
3 + 3 H
2O → 3 SO
2 + 3 S + 2 Al (OH)
3
Organisk kemi
Alkylering af natriumthiosulfat giver S -alkylthiosulfater, som kaldes Bunte -salte . Alkylthiosulfaterne er modtagelige for hydrolyse, hvilket giver thiolen. Denne reaktion illustreres ved en syntese af thioglycolsyre :
- ClCH
2CO
2H + Na
2S
2O
3 → Na [O
3S
2CH
2CO
2H] + NaCl - Na [O
3S
2CH
2CO
2H] + H
2O → HSCH
2CO
2H + NaHSO
4

