Agouti -signalprotein - Agouti-signaling protein
Agouti-signalprotein er et protein, der hos mennesker er kodet af ASIP- genet . Det er ansvarligt for fordelingen af melaninpigment hos pattedyr. Agouti interagerer med melanocortin 1 -receptoren for at afgøre, om melanocyt (pigmentcelle) producerer phaeomelanin (et rødt til gult pigment) eller eumelanin (et brunt til sort pigment). Denne interaktion er ansvarlig for at danne tydelige lyse og mørke bånd i hårene på dyr, såsom agouti , som genet er opkaldt efter. I andre arter som heste er agouti -signalering ansvarlig for at bestemme, hvilke dele af kroppen der vil være røde eller sorte. Mus med vildtype agouti vil være grå , hvor hvert hår er dels gult og dels sort. Tab af funktionsmutationer hos mus og andre arter forårsager sort pelsfarve, mens mutationer forårsager udtryk i hele kroppen hos mus forårsager gul pels og fedme.
Agouti-signalproteinet (ASIP) er en konkurrencedygtig antagonist med alfa-melanocytstimulerende hormon (α-MSH) til binding med melanocortin 1-receptor (MC1R) proteiner . Aktivering af α-MSH forårsager produktion af det mørkere eumelanin, mens aktivering af ASIP forårsager produktion af det rødere phaeomelanin. Det betyder, at hvor og mens agouti kommer til udtryk, vil den del af håret, der vokser, komme ud gult frem for sort.
Fungere
Hos mus koder agouti -genet for et paracrin signalmolekyle, der får hårsækkens melanocytter til at syntetisere det gule pigment pheomelanin i stedet for det sorte eller brune pigment eumelanin . Pleiotropiske virkninger af konstitutiv ekspression af muse-genet indbefatter voksen-debut fedme , øget tumor modtagelighed, og for tidlig infertilitet. Dette gen ligner meget musegenet og koder for et udskilt protein, der kan (1) påvirke kvaliteten af hårpigmentering , (2) fungere som en invers agonist af alfa-melanocytstimulerende hormon , (3) spille en rolle i neuroendokrine aspekter af melanocortinvirkning , og (4) har en funktionel rolle i at regulere lipidmetabolisme i adipocytter .
Hos mus præsenterer vildtype agouti -allelen (A) en grå fænotype, men mange allelvarianter er blevet identificeret gennem genetiske analyser, hvilket resulterer i en lang række fænotyper, der adskiller sig fra den typiske grå pels. De mest undersøgte allelvarianter er den dødelige gule mutation (A y ) og den levedygtige gule mutation (A vy ), der er forårsaget af ektopisk ekspression af agouti . Disse mutationer er også forbundet med gul overvægtigt syndrom, der er kendetegnet ved tidlig fedme , hyperinsulinæmi og tumorigenese . Det murine agouti -gen -locus findes på kromosom 2 og koder for et 131 aminosyreprotein. Dette protein signalerer fordelingen af melaninpigmenter i epitelmelanocytter placeret ved bunden af hårsækkene, idet ekspression er mere følsom på ventralt hår end på dorsalt hår. Agouti udskilles ikke direkte i melanocyt, da det virker som en parakrin faktor på dermale papillaceller for at hæmme frigivelse af melanocortin . Melanocortin virker på follikulære melanocytter for at øge produktionen af eumelanin , et melaninpigment, der er ansvarligt for brunt og sort hår. Når agouti udtrykkes, dominerer produktionen af pheomelanin , et melaninpigment, der producerer gult eller rødt hår.
Struktur
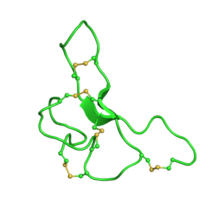
Agouti signalpeptid vedtager et hæmmende cystinknotmotiv . Sammen med det homologe Agouti-relaterede peptid er disse de eneste kendte pattedyrsproteiner, der adopterede denne fold. Peptidet består af 131 aminosyrer.
Mutationer
Den dødelige gule mutation (A y ) var den første embryonale mutation, der blev karakteriseret hos mus, da homozygote dødelige gule mus ( Ay / Ay ) dør tidligt i udviklingen på grund af en fejl i trofektodermdifferentiering . Dødelige gule homozygoter er sjældne i dag, mens dødelige gule og levedygtige gule heterozygoter (A y /a og A vy /a) forbliver mere almindelige. Hos vildtype-mus udtrykkes agouti kun i huden under hårvækst, men disse dominerende gule mutationer får den også til at udtrykkes i andre væv . Denne ektopiske ekspression af agouti -genet er forbundet med det gule fede syndrom , kendetegnet ved tidlig begyndende fedme , hyperinsulinæmi og tumorigenese .
Den dødelige gule (A y ) mutation skyldes en opstrøms sletning ved startstedet for agouti -transkription. Denne sletning får den genomiske sekvens af agouti til at gå tabt, undtagen promotoren og den første ikke-kodende exon af Raly , et allestedsnærværende udtrykt gen hos pattedyr. De kodende exoner af agouti placeres under kontrol af Raly -promotoren, hvilket initierer allestedsnærværende ekspression af agouti , øger produktionen af pheomelanin frem for eumelanin og resulterer i udviklingen af en gul fænotype.
Den levedygtige gule (A vy ) mutation skyldes en ændring i mRNA -længden af agouti , da det udtrykte gen bliver længere end den normale genlængde for agouti. Dette skyldes indsættelse af en enkelt intracistern A -partikel (IAP) retrotransposon opstrøms til startstedet for agouti -transkription. I den proximale ende af genet får en ukendt promotor derefter agouti til at blive forfatningsmæssigt aktiveret, og individer præsenterer fænotyper i overensstemmelse med den dødelige gule mutation. Selvom mekanismen til aktivering af promotoren, der kontrollerer den levedygtige gule mutation, er ukendt, er pelsfarvens styrke korreleret med graden af genmethylering , som bestemmes af moderens kost og miljøeksponering. Da agouti selv hæmmer melanocortinreceptorer, der er ansvarlige for eumelaninproduktion, forværres den gule fænotype i både dødelige gule og levedygtige gule mutationer, når agouti -genekspression øges. Agouti er unik, selvom det er en recessiv allel, vil heterozygoter fremstå gule, ikke den dominerende brune eller sorte.
Levedygtig gul (A vy /a) og dødelig gul (A y /a) heterozygoter har forkortet levetiden og øget risiko for at udvikle tidlig fedme, type II diabetes mellitus og forskellige tumorer. Den øgede risiko for at udvikle fedme skyldes dysregulering af appetit, da agouti agoniserer det agouti-relaterede protein (AGRP), der er ansvarlig for stimulering af appetit via hypothalamiske NPY/AGRP-orexigeniske neuroner. Agouti fremmer også fedme ved at modvirke melanocytstimulerende hormon (MSH) ved melanocortinreceptoren (MC4R), da MC4R er ansvarlig for at regulere fødeindtag ved at hæmme appetitssignaler. Stigningen i appetit er koblet til ændringer i næringsstofskiftet på grund af agouti 's parakrinvirkninger på fedtvæv, stigende niveauer af hepatisk lipogenese , faldende lipolyse og stigende adipocythypertrofi. Dette øger kropsmassen og fører til vanskeligheder med vægttab, da metaboliske veje bliver dysregulerede. Hyperinsulinæmi er forårsaget af mutationer til agouti , da agoutiproteinet fungerer på en calciumafhængig måde for at øge insulinsekretion i pancreas -beta -celler, hvilket øger risikoen for insulinresistens . Øget tumordannelse skyldes de øgede mitotiske hastigheder for agouti , som er lokaliseret til epitel- og mesenkymale væv.
Methylering og kostintervention

Korrekt funktion af agouti kræver DNA -methylering. Methylering forekommer i seks guanin-cytosin (GC) rige sekvenser i den 5 'lange terminale gentagelse af IAP-elementet i den levedygtige gule mutation. Methylering på et gen får genet til ikke at blive udtrykt, fordi det vil få promotoren til at blive slukket. I livmoderen kan moderens kost forårsage methylering eller demethylering. Når dette område er umetyleret, sker ektopisk ekspression af agouti , og gule fænotyper vises, fordi phaeomelanin udtrykkes i stedet for eumelanin. Når regionen er methyleret, udtrykkes agouti normalt, og grå og brune fænotyper (eumelanin) forekommer. Den epigenetiske tilstand af IAP -elementet bestemmes af methyleringsniveauet, da individer viser en lang række fænotyper baseret på deres grad af DNA -methylering. Øget methylering er korreleret med øget ekspression af det normale agouti -gen. Lave methyleringsniveauer kan forårsage genprintning, hvilket resulterer i, at afkom viser konsekvente fænotyper til deres forældre, da ektopisk ekspression af agouti arves gennem ikke-genomiske mekanismer.
DNA -methylering bestemmes i livmoderen ved moderens ernæring og miljøeksponering. Methyl syntetiseres de novo, men opnås gennem kosten af folsyre, methionin, betain og cholin, da disse næringsstoffer føder til en konsekvent metabolisk vej til methylsyntese. Tilstrækkelig zink og vitamin B12 er påkrævet til methylsyntese, da de fungerer som kofaktorer til overførsel af methylgrupper.
Når utilstrækkelig methyl er tilgængelig under tidlig embryonal udvikling, kan DNA -methylering ikke forekomme, hvilket øger ektopisk ekspression af agouti og resulterer i præsentation af de dødelige gule og levedygtige gule fænotyper, der vedvarer til voksenalderen. Dette fører til udviklingen af det gule fede syndrom , som forringer normal udvikling og øger modtageligheden for udviklingen af kronisk sygdom. At sikre, at moderens kost er højt i methylækvivalenter, er en vigtig forebyggende foranstaltning til at reducere ektopisk ekspression af agouti hos afkom. Kostintervention gennem methyltilskud reducerer aftryk på agouti -locus, da øget methylforbrug får IAP -elementet til at blive fuldstændigt methyleret og ektopisk ekspression af agouti reduceret. Dette sænker andelen af afkom, der præsenteres med den gule fænotype, og øger antallet af afkom, der ligner agouti vildtype mus med grå frakker. To genetisk identiske mus kunne se meget forskellige fænotypisk ud på grund af mødrenes kost, mens musene var i livmoderen. Hvis musene har agouti -genet, kan det udtrykkes på grund af, at moderen spiser en typisk kost, og afkommet ville have en gul pels. Hvis den samme mor havde spist en methylrig kost suppleret med zink, vitamin B12 og folsyre, ville afkomets agouti-gen sandsynligvis blive methyleret, det ville ikke blive udtrykt, og pelsfarven ville være brun i stedet. Hos mus er den gule pelsfarve også forbundet med sundhedsproblemer hos mus, herunder fedme og diabetes.
Menneskelig homolog
Agouti signalprotein (ASP) er den humane homolog for murin agouti . Det kodes af det humane agouti -gen på kromosom 20 og er et protein bestående af 132 aminosyrer. Det udtrykkes meget bredere end murine agouti og findes i fedtvæv, bugspytkirtel, testikler og æggestokke, mens murine agouti udelukkende udtrykkes i melanocytter. ASP har 85% lighed med den murine form for agouti . Da ektopisk ekspression af murin agouti fører til udviklingen af det gule fede syndrom , forventes dette at være konsistent hos mennesker. Det gule fede syndrom øger udviklingen af mange kroniske sygdomme, herunder fedme, type II diabetes mellitus og tumorigenese.
ASP har lignende farmakologisk aktivering som murine agouti , da melanocortinreceptorer hæmmes gennem konkurrencedygtig antagonisme. Inhibering af melanocortin med ASP kan også være ved ikke-konkurrencedygtige metoder, der udvider dets rækkevidde. ASP's funktion adskiller sig fra murine agouti . ASP påvirker kvaliteten af hårpigmentering, mens murine agouti styrer fordelingen af pigmenter, der bestemmer pelsens farve. ASP har neuroendokrine funktioner, der er i overensstemmelse med murine agouti , da det agoniserer via AgRP -neuroner i hypothalamus og modvirker MSH ved MC4R'er, som reducerer mæthedssignaler. AgRP fungerer som en appetitstimulator og øger appetitten, samtidig med at metabolismen reduceres. På grund af disse mekanismer kan AgRP være forbundet med øget kropsmasse og fedme hos både mennesker og mus. Overekspression af AgRP er blevet forbundet med fedme hos mænd, mens visse polymorfismer af AgRP har været forbundet med spiseforstyrrelser som anorexia nervosa . Mekanismen, der ligger til grund for hyperinsulinæmi hos mennesker, er i overensstemmelse med murine agouti , da insulinsekretion øges gennem calciumfølsom signalering i pancreas -beta -celler. Mekanismen for ASP -induceret tumorigenese er stadig ukendt hos mennesker.
Se også
Referencer
Yderligere læsning
- Wilczynski AM, Joseph CG, Haskell-Luevano C (september 2005). "Aktuelle tendenser i struktur-aktivitetsrelationsundersøgelser af den endogene agouti-relaterede protein (AGRP) melanocortinreceptorantagonist". Medicinske forskningsanmeldelser . 25 (5): 545–56. doi : 10.1002/med.20037 . PMID 16044415 . S2CID 116767 .
- Pritchard LE, White A (oktober 2005). "Agouti-relateret protein: mere end en melanocortin-4-receptorantagonist?". Peptider . 26 (10): 1759–70. doi : 10.1016/j.peptides.2004.11.036 . PMID 15996791 . S2CID 21598037 .
- Stütz AM, Morrison CD, Argyropoulos G (oktober 2005). "Det agouti-relaterede protein og dets rolle i energi-homeostase". Peptider . 26 (10): 1771–81. doi : 10.1016/j.peptides.2004.12.024 . PMID 15961186 . S2CID 9749408 .
- Millhauser GL, McNulty JC, Jackson PJ, Thompson DA, Barsh GS, Gantz I (juni 2003). "Sløjfer og links: strukturel indsigt i det agouti-relaterede proteins bemærkelsesværdige funktion" (PDF) . Annaler fra New York Academy of Sciences . 994 (1): 27–35. Bibcode : 2003NYASA.994 ... 27M . doi : 10.1111/j.1749-6632.2003.tb03159.x . HDL : 2027,42 / 75.746 . PMID 12851295 . S2CID 46576434 .
- Barsh GS, He L, Gunn TM (2002). "Genetiske og biokemiske undersøgelser af Agouti-attractin-systemet". Journal of Receptor and Signal Transduction Research . 22 (1–4): 63–77. doi : 10.1081/RRS-120014588 . PMID 12503608 . S2CID 25089838 .
- Millington GW (maj 2006). "Proopiomelanocortin (POMC): dets melanocortin -produkters og receptorers kutane roller". Klinisk og eksperimentel dermatologi . 31 (3): 407–12. doi : 10.1111/j.1365-2230.2006.02128.x . PMID 16681590 . S2CID 25213876 .
eksterne links
- agouti+protein på US National Library of Medicine Medical Subject Headings (MeSH)
Denne artikel indeholder tekst fra United States National Library of Medicine , som er offentligt tilhørende .



