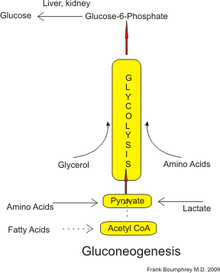
Glukoneogenese - Gluconeogenesis
Gluconeogenese ( GNG ) er en metabolisk vej, der resulterer i dannelse af glukose fra visse ikke- kulhydratkulissubstrater . Det er en allestedsnærværende proces, der findes i planter, dyr, svampe, bakterier og andre mikroorganismer. Hos hvirveldyr, glukoneogenese sker hovedsageligt i leveren og i mindre grad, i cortex af nyrerne . Det er en af to primære mekanismer - den anden er nedbrydning af glykogen ( glykogenolyse ) - brugt af mennesker og mange andre dyr til at opretholde blodsukkerniveauer og undgå lave niveauer ( hypoglykæmi ). Hos drøvtyggere , fordi diæt kulhydrater har en tendens til at blive metaboliseret af vommens organismer, forekommer glukoneogenese uanset fastende, lavt kulhydrat kost, motion osv. I mange andre dyr sker processen i perioder med faste , sult , lavt kulhydrat kost eller intens træning .
Hos mennesker kan substrater til glukoneogenese komme fra alle ikke-kulhydratkilder, der kan omdannes til pyruvat eller mellemprodukter af glykolyse (se figur). Til nedbrydning af proteiner inkluderer disse substrater glucogene aminosyrer (dog ikke ketogene aminosyrer ); fra nedbrydning af lipider (såsom triglycerider ) inkluderer de glycerol , ulige kædede fedtsyrer (selvom det ikke er ensartede fedtsyrer, se nedenfor); og fra andre dele af stofskiftet inkluderer de lactat fra Cori -cyklussen . Under betingelser med langvarig faste kan acetone afledt af ketonlegemer også tjene som et substrat, der giver en vej fra fedtsyrer til glucose. Selvom de fleste gluconeogenese forekommer i leveren, øges det relative bidrag fra gluconeogenese fra nyrerne ved diabetes og langvarig faste.
Glukoneogenesebanen er meget endergonisk, indtil den er koblet til hydrolysen af ATP eller GTP , hvilket effektivt gør processen exergonisk . For eksempel kræver den vej, der fører fra pyruvat til glucose-6-phosphat , 4 molekyler ATP og 2 molekyler GTP for at forløbe spontant. Disse ATP'er tilføres fra fedtsyrekatabolisme via beta -oxidation .
Forstadier

- Glukogene aminosyrer har denne evne
- Ketogene aminosyrer gør det ikke. Disse produkter kan stadig bruges til ketogenese eller lipidsyntese .
- Nogle aminosyrer nedbrydes til både glukogene og ketogene produkter.
Hos mennesker er de vigtigste glukoneogene forstadier lactat , glycerol (som er en del af triglyceridmolekylet ), alanin og glutamin . Alt i alt tegner de sig for over 90% af den samlede glukoneogenese. Andre glukogene aminosyrer og alle mellemprodukter af citronsyrecyklus (gennem omdannelse til oxaloacetat ) kan også fungere som substrater for glukoneogenese. Generelt medfører menneskeligt forbrug af glukoneogene substrater i fødevarer ikke øget glukoneogenese.
Hos drøvtyggere er propionat det vigtigste glukoneogene substrat. Hos nonruminants, herunder mennesker, opstår propionat fra β-oxidation af ulige og forgrenede fedtsyrer er et (relativt lille) substrat for glukoneogenese.
Laktat transporteres tilbage til leveren, hvor det omdannes til pyruvat ved Cori -cyklus ved hjælp af enzymet lactat dehydrogenase . Pyruvat, det første udpegede substrat for den glukoneogene vej, kan derefter bruges til at generere glucose. Transaminering eller deamination af aminosyrer letter indtrængen af deres kulstofskelet i cyklussen direkte (som pyruvat eller oxaloacetat) eller indirekte via citronsyrecyklussen. Bidraget fra Cori -cykluslaktat til den samlede glukoseproduktion stiger med fastetid . Specifikt efter 12, 20 og 40 timers faste ved menneskelige frivillige var Cori -cykluslaktats bidrag til gluconeogenese henholdsvis 41%, 71%og 92%.
Hvorvidt fedtsyrer med lige kæder kan omdannes til glukose hos dyr har været et mangeårigt spørgsmål inden for biokemi. Odd-kædede fedtsyrer kan oxideres til opnåelse af acetyl-CoA og propionyl-CoA , sidstnævnte fungerer som en forløber for succinyl-CoA , som kan omdannes til pyruvat og indgå i glukoneogenese. I modsætning hertil oxideres ensartede fedtsyrer til kun at give acetyl-CoA, hvis indtræden i gluconeogenese kræver tilstedeværelse af en glyoxylatcyklus (også kendt som glyoxylat shunt) for at producere fire-carbon dicarboxylsyre-forstadier. Glyoxylatshunten omfatter to enzymer, malatsyntase og isocitratlyase, og er til stede i svampe, planter og bakterier. På trods af nogle rapporter om glyoxylat shunt enzymatiske aktiviteter påvist i dyrevæv, er gener, der koder for begge enzymatiske funktioner, kun fundet i nematoder , hvor de findes som et enkelt bi-funktionelt enzym. Gener, der koder for malatsyntase alene (men ikke isocitratlyase) er blevet identificeret hos andre dyr, herunder leddyr , pighuder og endda nogle hvirveldyr . Pattedyr, der findes for at besidde malatsyntasegenet, omfatter monotremer ( næbdyr ) og pungdyr ( opossum ), men ikke placentapattedyr .
Eksistensen af glyoxylatcyklussen hos mennesker er ikke fastslået, og det er udbredt, at fedtsyrer ikke direkte kan omdannes til glukose hos mennesker. Carbon-14 har vist sig at ende i glukose, når det tilføres i fedtsyrer, men det kan forventes ved inkorporering af mærkede atomer afledt af acetyl-CoA i mellemprodukter af citronsyrecyklus, der kan udskiftes med dem, der stammer fra andre fysiologiske kilder , såsom glukogene aminosyrer. I fravær af andre glukogene kilder kan 2-carbonacetyl -CoA, der stammer fra oxidation af fedtsyrer, ikke producere et nettoudbytte af glucose via citronsyrecyklussen , da ækvivalente to carbonatomer frigives som kuldioxid under cyklussen. Under ketose giver acetyl-CoA fra fedtsyrer imidlertid ketonlegemer , herunder acetone , og op til ~ 60% af acetone kan oxideres i leveren til pyruvat-forstadierne acetol og methylglyoxal . Således kunne ketonlegemer afledt af fedtsyrer tegne sig for op til 11% af glukoneogenesen under sult. Katabolisme af fedtsyrer producerer også energi i form af ATP, der er nødvendig for glukoneogenesevejen.
Beliggenhed
Hos pattedyr menes glukoneogenese at være begrænset til leveren, nyrerne, tarmen og musklerne, men nyere beviser indikerer, at glukoneogenese forekommer i hjernens astrocytter . Disse organer bruger noget forskellige glukoneogene forstadier. Leveren bruger fortrinsvis laktat, glycerol og glucogene aminosyrer (især alanin ), mens nyren fortrinsvis bruger laktat, glutamin og glycerol. Laktat fra Cori -cyklussen er kvantitativt den største kilde til substrat til glukoneogenese, især for nyrerne. Leveren bruger både glykogenolyse og glukoneogenese til at producere glukose, hvorimod nyren kun bruger glukoneogenese. Efter et måltid skifter leveren til glykogensyntese , hvorimod nyren øger glukoneogenesen. Tarmene bruger mest glutamin og glycerol.
Propionat er det primære substrat for glukoneogenese i drøvtyggerselever, og drøvtyggerslever kan øge brugen af glukoneogene aminosyrer (f.eks. Alanin), når glukosebehovet øges. Levercellernes evne til at bruge laktat til glukoneogenese falder fra preruminantstadiet til drøvtyggeren i kalve og lam. I fårenyrevæv er der observeret meget høje niveauer af glukoneogenese fra propionat.
I alle arter er dannelsen af oxaloacetat fra pyruvat- og TCA- cyklusmellemprodukter begrænset til mitokondrion, og enzymerne, der omdanner phosphoenolpyruvinsyre (PEP) til glucose-6-phosphat, findes i cytosolen. Placeringen af enzymet, der forbinder disse to dele af glukoneogenesen ved at omdanne oxaloacetat til PEP - PEP -carboxykinase (PEPCK) - er variabel efter art: det kan findes helt i mitokondrierne , helt inden i cytosolen eller spredes jævnt mellem de to, som det er hos mennesker. Transport af PEP over mitokondriemembranen udføres af dedikerede transportproteiner; der findes imidlertid ikke sådanne proteiner for oxaloacetat . Derfor skal oxaloacetat i arter, der mangler intra-mitokondriel PEPCK, omdannes til malat eller aspartat , eksporteres fra mitokondrien og omdannes tilbage til oxaloacetat for at tillade gluconeogenese at fortsætte.
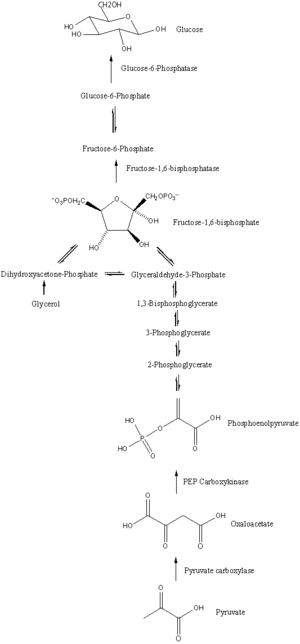
Pathway
Gluconeogenese er en vej, der består af en række elleve enzymkatalyserede reaktioner. Vejen begynder enten i leveren eller nyrerne, i mitokondrierne eller cytoplasmaet i disse celler, hvilket afhænger af, at substratet bruges. Mange af reaktionerne er omvendt af trin, der findes i glykolyse .
- Gluconeogenese begynder i mitokondrierne med dannelsen af oxaloacetat ved carboxylering af pyruvat. Denne reaktion kræver også et molekyle ATP og katalyseres af pyruvatcarboxylase . Dette enzym stimuleres af høje niveauer af acetyl-CoA (produceret ved β-oxidation i leveren) og hæmmes af høje niveauer af ADP og glucose.
- Oxaloacetat reduceres til malat ved hjælp af NADH , et trin, der kræves for dets transport ud af mitokondrierne.
- Malat oxideres til oxaloacetat ved hjælp af NAD + i cytosolen, hvor de resterende trin i gluconeogenese finder sted.
- Oxaloacetat decarboxyleres og phosphoryleres derefter til dannelse af phosphoenolpyruvat ved hjælp af enzymet PEPCK . Et molekyle af GTP hydrolyseres til BNP under denne reaktion.
- De næste trin i reaktionen er de samme som omvendt glykolyse . Imidlertid fructose 1,6-bisphosphatase omvendte fructose 1,6-bisphosphat til fructose-6-phosphat , ved hjælp af en vand-molekyle og frigive en phosphat (i glycolyse, phosphofructokinase 1 omvendte F6P og ATP til F1,6BP og ADP ). Dette er også det hastighedsbegrænsende trin i glukoneogenesen.
- Glucose-6-phosphat dannes af fructose 6-phosphat af phosphoglucoisomerase (bagsiden af trin 2 i glykolyse). Glucose-6-phosphat kan bruges i andre metaboliske veje eller dephosphoryleres til fri glukose. Mens fri glukose let kan diffundere ind og ud af cellen, er den phosphorylerede form (glucose-6-phosphat) låst i cellen, en mekanisme, hvormed intracellulære glukoseniveauer styres af celler.
- Den endelige glukoneogenese, dannelsen af glucose, forekommer i lumen i det endoplasmatiske retikulum , hvor glucose-6-phosphat hydrolyseres af glucose-6-phosphatase for at producere glucose og frigive et uorganisk phosphat. Ligesom to trin før er dette trin ikke en simpel reversering af glykolyse, hvor hexokinase katalyserer omdannelsen af glucose og ATP til G6P og ADP. Glukose transporteres ind i cytoplasmaet af glukosetransportører placeret i den endoplasmatiske retikulums membran.
| Metabolisme af almindelige monosaccharider , herunder glykolyse , glukoneogenese, glykogenese og glykogenolyse |
|---|
Regulering
Mens de fleste trin i glukoneogenesen er det modsatte af dem, der findes i glykolyse , erstattes tre regulerede og stærkt endergoniske reaktioner med mere kinetisk gunstige reaktioner. Hexokinase / glucokinase , phosphofructokinase og pyruvat kinase enzymer af glycolyse erstattes med glucose-6-phosphatase , fructose-1,6-bisphosphatase og PEP carboxykinase / pyruvat carboxylase. Disse enzymer reguleres typisk af lignende molekyler, men med modsatte resultater. For eksempel aktiverer acetyl CoA og citrat gluconeogenese-enzymer (henholdsvis pyruvatcarboxylase og fructose-1,6-bisphosphatase), samtidig med at det inhiberer det glykolytiske enzym pyruvatkinase . Dette system med gensidig kontrol tillader glykolyse og glukoneogenese at hæmme hinanden og forhindrer en forgæves cyklus med syntetisering af glukose for kun at nedbryde det. Pyruvatkinase kan også omgås af 86 veje, der ikke er relateret til gluconeogenese, med det formål at danne pyruvat og efterfølgende lactat; nogle af disse veje bruger kulstofatomer, der stammer fra glukose.
Størstedelen af de enzymer, der er ansvarlige for gluconeogenese, findes i cytosolen ; undtagelserne er mitokondriel pyruvatcarboxylase og hos dyr phosphoenolpyruvatcarboxykinase . Sidstnævnte findes som et isozym placeret i både mitokondrien og cytosolen . Hastigheden af glukoneogenese styres i sidste ende af virkningen af et nøgleenzym, fructose-1,6-bisphosphatase , som også reguleres gennem signaltransduktion af cAMP og dets phosphorylering.
Global kontrol af glukoneogenese medieres af glukagon ( frigives når blodglukoseniveauet er lavt ); det udløser phosphorylering af enzymer og regulatoriske proteiner ved hjælp af proteinkinase A (en cyklisk AMP -reguleret kinase), hvilket resulterer i inhibering af glykolyse og stimulering af glukoneogenese. Insulin modvirker glukagon ved at hæmme glukoneogenese. Type 2 -diabetes er præget af overskydende glukagon og insulinresistens fra kroppen. Insulin kan ikke længere hæmme genekspressionen af enzymer såsom PEPCK, hvilket fører til øgede niveauer af hyperglykæmi i kroppen. Det antidiabetiske lægemiddel metformin reducerer blodsukkeret primært gennem hæmning af glukoneogenese og overvinder insulins manglende hæmning af glukoneogenese på grund af insulinresistens.
Undersøgelser har vist, at fraværet af hepatisk glukoseproduktion ikke har nogen større effekt på kontrollen af fastende plasmaglukosekoncentration. Kompenserende induktion af glukoneogenese forekommer i nyrerne og tarmen, drevet af glukagon , glukokortikoider og acidose.
Insulin resistens
I leveren fremmer FOX -proteinet FOXO6 normalt glukoneogenese i fastende tilstand, men insulin blokerer FOXO6 ved fodring. I en tilstand med insulinresistens blokerer insulin ikke FOXO6, hvilket resulterer i fortsat glukoneogenese selv ved fodring, hvilket resulterer i forhøjet blodsukker ( hyperglykæmi ).
Insulinresistens er et fælles træk ved metabolisk syndrom og type 2 -diabetes . Af denne grund er glukoneogenese et mål for terapi for type 2 -diabetes, såsom det antidiabetiske lægemiddel metformin , som hæmmer glukoneogen glukosedannelse og stimulerer glukoseoptagelse af celler.