Arvelig nonpolyposis kolorektal cancer - Hereditary nonpolyposis colorectal cancer
| Arvelig nonpolyposis kolorektal cancer | |
|---|---|
| Andre navne | Lynch syndrom |
 | |
| Mikrograf, der viser tumorinfiltrerende lymfocytter (i en tyktarmskræft ), et fund forbundet med MSI -H -tumorer, som det kan ses ved Lynch syndrom. H & E plet . | |
| Specialitet |
Onkologi |
Arvelig nonpolyposis kolorektal cancer ( HNPCC ) eller Lynch syndrom er en autosomal dominerende genetisk tilstand, der er forbundet med en høj risiko for tyktarmskræft såvel som andre kræftformer, herunder endometriecancer (næstmest almindelig), æggestokke , mave , tyndtarme , lever -galdeveje , øvre urinvej , hjerne og hud . Den øgede risiko for disse kræftformer skyldes arvelige mutationer, der forringer DNA -mismatch -reparation . Det er en type kræftsyndrom . Fordi patienter med Lynch syndrom kan have polypper, er udtrykket HNPCC faldet i unåde.
tegn og symptomer
Risiko for kræft
Livstidsrisiko og middelalder ved diagnose for kræft i forbindelse med Lynch syndrom
| Kræftform | Livstidsrisiko (%) | Middelalder ved diagnose (år) |
| Kolorektal | 52-58 | 44-61 |
| Endometrial | 25-60 | 48-62 |
| Gastric | 6-13 | 56 |
| Æggestokkene | 4-12 | 42,5 |
Ud over de kræftformer, der findes i diagrammet ovenfor, er det underforstået, at Lynch syndrom også bidrager til en øget risiko for kræft i tyndtarmen, kræft i bugspytkirtlen, kræft i urinleder/nyre, bækkenkræft, hjernekræft og talgneoplasmer . Øget risiko for prostatakræft og brystkræft har også været forbundet med Lynch syndrom, selvom dette forhold ikke er helt forstået.
To tredjedele af tyktarmskræft forekommer i den proksimale tyktarm, og almindelige tegn og symptomer omfatter blod i afføringen, diarré eller forstoppelse og utilsigtet vægttab . Middelalderen for diagnosen kolorektal kræft er 44 for familiemedlemmer, der opfylder Amsterdam -kriterierne. Den gennemsnitlige alder for diagnosticering af endometriecancer er omkring 46 år. Blandt kvinder med HNPCC, der har både tyktarm og livmoderhalskræft, er omkring halvdelen til stede først med livmoderhalskræft , hvilket gør livmoderkræft til den mest almindelige vagtpostkræft i Lynch syndrom. Det mest almindelige symptom på endometriecancer er unormal vaginal blødning. I HNPCC er gennemsnitsalderen for diagnosen af mavekræft 56 år, hvor tarm-type adenocarcinom er den mest almindeligt rapporterede patologi. HNPCC-associerede ovariecancer har en gennemsnitlig diagnosealder på 42,5 år gammel; cirka 30% får diagnosen før 40 år.
Der er fundet signifikant variation i kræftfrekvensen afhængigt af den involverede mutation. Op til 75 år var risikoen for kolorektal cancer, endometriecancer, kræft i æggestokkene , øvre gastrointestinal (gastrisk, duodenal, galdegang eller bugspytkirtel), urinvejskræft, prostatakræft og hjernetumorer som følger: for MLH1 -mutationer var risikoen var - 46%, 43%, 10%, 21%, 8%, 17%og 1%henholdsvis: for MSH2 -mutationer var risiciene henholdsvis 57%, 17%, 10%, 25%, 32%og 5%: for MSH6 -mutationer var risiciene henholdsvis 15%, 46%, 13%, 7%, 11%, 18%og 1%.
| Gene | Ovariecancerrisiko | Risiko for livmoderhalskræft |
|---|---|---|
| MLH1 | 4-24% | 25-60% |
| MSH2 /EPCAM | 4-24% | 25-60% |
| MSH6 | 1-11% | 16-26% |
| PMS2 | 6% (kombineret risiko) | 15% |
Genetik
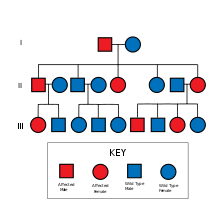
HNPCC nedarves på en autosomal dominerende måde. HNPCC's kendetegn er defekt reparation af DNA-mismatch , hvilket forårsager en forhøjet hastighed af enkelte nukleotidændringer og mikrosatellit ustabilitet , også kendt som MSI-H (H er "høj"). MSI er identificerbare i cancer prøver i patologi laboratorium. De fleste tilfælde resulterer i ændringer i længderne af dinucleotid -gentagelser af nucleobaserne cytosin og adenin (sekvens: CACACACACA ...).
De 4 hovedgener involveret i HNPCC koder normalt for proteiner, der danner dimerer til at fungere:
- MLH1-protein dimererer med PMS2-protein til dannelse af MutLα, som koordinerer bindingen af andre proteiner, der er involveret i fejlparringsreparation som DNA-helikase , enkeltstrenget-DNA-bindingsprotein (RPA) og DNA-polymeraser .
- MSH2 -protein dimererer med MSH6 -protein, som identificerer uoverensstemmelser via en glidende klemmemodel , et protein til scanning efter fejl.
Forringelsen af begge gen for proteindimeren forringer proteinfunktionen. Disse 4 gener er involveret i fejlkorrektion (mismatch reparation), så dysfunktion af generne kan føre til manglende evne til at reparere DNA -replikationsfejl og forårsage HNPCC. HNPCC er kendt for at være forbundet med andre mutationer i gener involveret i DNA -mismatch -reparationsvejen :
| OMIM navn | Gener impliceret i HNPCC | Mutationsfrekvens i HNPCC -familier | Locus | Første udgivelse |
|---|---|---|---|---|
| HNPCC1 ( 120435 ) | MSH2 /EPCAM | cirka 60% | 2p22 | Fishel 1993 |
| HNPCC2 ( 609310 ) | MLH1 | cirka 30% | 3p21 | Papadopoulos 1994 |
| HNPCC5 | MSH6 | 7-10% | 2p16 | Miyaki 1997 |
| HNPCC4 | PMS2 | relativt sjældent | 7p22 | Nicolaides 1994 |
| HNPCC3 | PMS1 | sagsrapport | 2q31-q33 | Nicolaides 1994 |
| HNPCC6 | TGFBR2 | sagsrapport | 3p22 | |
| HNPCC7 | MLH3 | omtvistet | 14q24.3 |
Mennesker med MSH6-mutationer er mere tilbøjelige til at være Amsterdamskriterier II-negative. Præsentationen med MSH6 er lidt anderledes end med MLH1 og MSH2, og udtrykket "MSH6 syndrom" er blevet brugt til at beskrive denne tilstand. I en undersøgelse var Bethesda -retningslinjerne mere følsomme end Amsterdam -kriterierne ved at opdage det.
Op til 39% af familier med mutationer i et HNPCC -gen opfylder ikke Amsterdam -kriterierne . Derfor bør familier, der har fundet en skadelig mutation i et HNPCC -gen, anses for at have HNPCC uanset omfanget af familiehistorien. Dette betyder også, at Amsterdam -kriterierne ikke identificerer mange mennesker, der er i fare for Lynch -syndrom. Forbedring af kriterierne for screening er et aktivt forskningsområde som beskrevet i afsnittet Screening Strategies i denne artikel.
De fleste mennesker med HNPCC arver tilstanden fra en forælder. På grund af ufuldstændig penetration, variabel alder for kræftdiagnose, reduktion af kræftrisiko eller tidlig død har ikke alle mennesker med en HNPCC -genmutation en forælder, der havde kræft. Nogle mennesker udvikler HNPCC de-novo i en ny generation uden at arve genet. Disse mennesker identificeres ofte kun efter at have udviklet en tyktarmskræft i et tidligt liv. Forældre med HNPCC har 50% chance for at overføre den genetiske mutation til hvert barn. Det er også vigtigt at bemærke, at skadelig mutation i et af MMR -gener alene ikke er tilstrækkelig til at forårsage kræft, men at der snarere skal forekomme yderligere mutationer i andre tumorsuppressorgener.
Diagnose
En diagnose af Lynch syndrom anvendes til mennesker med en kimlinje -DNA -mutation i et af MMR -generne (MLH1, MSH2, MSH6 og PMS2) eller EPCAM -genet, identificeret ved genetisk testning. Kandidater til genetisk test af kønsceller kan identificeres ved kliniske kriterier som Amsterdam Clinical Criteria og Bethesda Guidelines, eller gennem tumoranalyse ved immunhistokemi (IHC) eller microsatellite ustabilitet (MSI) test. I USA anbefaler professionelle samfund at teste alle tyktarmskræft for MSI eller IHC som screening for Lynch syndrom, men dette udføres ikke altid på grund af omkostnings- og ressourcebegrænsninger. Genetisk test er kommercielt tilgængelig og består af en blodprøve.
Immunhistokemi
Immunhistokemi (IHC) er en metode, der kan bruges til at påvise unormal mismatch -reparation (MMR) proteinekspression i tumorer, der er forbundet med Lynch syndrom. Selvom det ikke er diagnostisk for et Lynch -syndrom, kan det spille en rolle i at identificere mennesker, der skal have kimtest. To metoder til implementering af IHC-test inkluderer aldersbaseret test og universel test for alle mennesker. I øjeblikket er der ingen udbredt enighed om, hvilken screeningsmetode der skal anvendes. Aldersbaseret test for IHC er delvis blevet foreslået på grund af cost-benefit-analyser, hvorimod universel testning for alle mennesker med tyktarmskræft sikrer, at mennesker med Lynch-syndrom ikke går glip af. For at imødekomme omkostningerne forsøger forskere at forudsige MSI eller IHC direkte ud fra, hvordan tumoren ser ud under mikroskopet, uden at foretage molekylær testning.
Mikrosatellit ustabilitet
Mutationer i DNA -mismatch -reparationssystemer kan føre til vanskeligheder med at overføre regioner inden for DNA'et, som indeholder gentagne mønstre af to eller tre nukleotider ( mikrosatellitter ), ellers kendt som mikrosatellit -ustabilitet ( MSI ). MSI identificeres ved DNA -ekstraktion fra både en tumorvævsprøve og en normal vævsprøve efterfulgt af PCR -analyse af mikrosatellitregioner. MSI -analyse kan bruges til at identificere mennesker, der kan have Lynch syndrom, og dirigere dem til yderligere test.
Klassifikation
Tre hovedgrupper af MSI-H ( mikrosatellit ustabilitet -MSI) kræft kan genkendes efter histopatologiske kriterier:
- højresidigt dårligt differentierede kræftformer
- højresidede slimhindekræftformer
- adenocarcinomer på ethvert sted, der viser et målbart niveau af intraepitelial lymfocyt (TIL)
De histopatologiske kriterier er ikke følsomme nok til at detektere MSI fra histologi, men forskere forsøger at bruge kunstig intelligens til at forudsige MSI fra histologi.
Derudover kan HNPCC opdeles i Lynch syndrom I (familiær tyktarmskræft) og Lynch syndrom II (HNPCC forbundet med andre kræftformer i mave -tarmkanalen eller reproduktive system ).
Forebyggelse
Efter at have rapporteret et nul-fund fra deres randomiserede kontrollerede forsøg med aspirin (acetylsalicylsyre-ASA) for at forhindre kolorektal neoplasi af Lynch syndrom, har Burn og kolleger rapporteret nye data, der repræsenterer en længere opfølgningsperiode end rapporteret i det første NEJM- papir. Disse nye data viser en reduceret forekomst hos mennesker med Lynch syndrom, som blev udsat for mindst fire års højdosis aspirin med en tilfredsstillende risikoprofil. Disse resultater er blevet bredt omtalt i medierne; fremtidige undersøgelser vil se på at ændre (sænke) dosis (for at reducere risikoen forbundet med den høje dosis af ASA).
Screening
Genetisk rådgivning og genetisk test anbefales til familier, der opfylder Amsterdam -kriterierne, helst inden starten på tyktarmskræft.
Tyktarmskræft
Koloskopi anbefales som en forebyggende overvågningsmetode for personer, der har Lynch syndrom eller LS-associerede gener. Specifikt anbefales det, at koloskopier begynder i alderen 20-25 for MLH1- og MSH2 -mutationsbærere og 35 år for MSH6- og PMS2 -mutationsbærere. Koloskopisk overvågning bør derefter udføres med 1-2 års mellemrum for patienter med Lynch syndrom.
Endometrial/Ovarian cancer
En transvaginal ultralyd med eller uden endometriebiopsi anbefales årligt til screening af æggestokke og endometrial cancer. For kvinder med Lynch syndrom kan en årlig CA-125 blodprøve bruges til at screene for kræft i æggestokkene, men der er begrænsede data om effektiviteten af denne test til at reducere dødeligheden.
Andre kræftformer
Der er også strategier til at opdage andre kræftformer tidligt eller reducere chancerne for at udvikle dem, som mennesker med Lynch syndrom kan diskutere med deres læge, men deres effektivitet er ikke klar. Disse muligheder omfatter:
- Øvre endoskopier til påvisning af mave- og tyndkræft hvert 3. -5. År, tidligst tidligt i en alder af 30 år (helst i en forskningsindstilling)
- Årlig urinanalyse for at opdage blærekræft , tidligst ved en alder af 30 år (helst i en forskningsindstilling)
- Årlige fysiske og neurologiske undersøgelser for at opdage kræft i centralnervesystemet ( hjerne eller rygmarv) tidligst fra 25 år
Amsterdam kriterier
Følgende er Amsterdam-kriterierne til at identificere højrisikokandidater til molekylær genetisk testning:
Amsterdam I -kriterier (alle punkter skal være opfyldt): Amsterdam I -kriterierne blev offentliggjort i 1990; man mente imidlertid, at de var utilstrækkeligt følsomme.
- Tre eller flere familiemedlemmer med en bekræftet diagnose af tyktarmskræft, hvoraf den ene er en første grad (forælder, barn, søskende) slægtning til de to andre
- To på hinanden følgende berørte generationer
- En eller flere tyktarmskræft diagnosticeret under 50 år
- Familiel adenomatøs polypose (FAP) er udelukket
Amsterdam II -kriterierne blev udviklet i 1999 og forbedrede den diagnostiske følsomhed for Lynch -syndrom ved at inkludere kræft i endometriet , tyndtarmen, urinlederen og nyrebækkenet.
Amsterdam Criteria II (alle punkter skal være opfyldt):
- Tre eller flere familiemedlemmer med HNPCC-relaterede kræftformer, hvoraf den ene er en førstegrads slægtning til de to andre
- To på hinanden følgende berørte generationer
- En eller flere af de HNPCC-relaterede kræftformer diagnosticeret under 50 år
- Familiel adenomatøs polypose (FAP) er udelukket
Bethesda -kriterierne blev udviklet i 1997 og senere opdateret i 2004 af National Cancer Institute for at identificere personer, der kræver yderligere test for Lynch syndrom gennem MSI. I modsætning til Amsterdam -kriterierne bruger de reviderede Bethesda -retningslinjer patologiske data ud over kliniske oplysninger til at hjælpe sundhedsudbydere med at identificere personer med høj risiko.
Reviderede Bethesda -retningslinjer
Hvis en person opfylder et af 5 kriterier, bør tumor (erne) fra personen testes for MSI:
1. Kolorektal kræft diagnosticeret før 50 år
2. Tilstedeværelse af synkron eller metakron kolorektal eller anden Lynch -syndrom -associeret kræft (f.eks. Kræft i endometrium, æggestok, mave, tyndtarm, bugspytkirtel, galdeveje, urinleder, nyrebækken, hjerne, talgkirtler, keratoacanthomer )
3. Kolorektal cancer med MSI-høj patologi hos en person, der er yngre end 60 år
4. Kolorektal kræft diagnosticeret hos en person med en eller flere første graders slægtning med kolorektal cancer eller Lynch syndrom-associeret tumor diagnosticeret under 50 år
5. Person med tyktarmskræft og to eller flere første- eller andengrads-slægtninge med tyktarmskræft eller Lynch syndrom-associeret kræft diagnosticeret i alle aldre.
Det er vigtigt at bemærke, at disse kliniske kriterier kan være vanskelige at bruge i praksis, og kliniske kriterier alene bruges til at savne mellem 12 og 68 procent af Lynch syndrom tilfælde.
Kirurgi
Profylaktisk hysterektomi og salpingo-oophorektomi (fjernelse af livmoderen , æggelederne og æggestokkene for at forhindre kræft i at udvikle sig) kan udføres før kræft i æggestokkene eller endometrium udvikler sig.
Behandling
Kirurgi er fortsat frontlinjeterapien for HNPCC. Patienter med Lynch syndrom, der udvikler tyktarmskræft, kan behandles med enten delvis kolektomi eller total kolektomi med ileorektal anastomose. På grund af øget risiko for tyktarmskræft efter partiel kolektomi og lignende livskvalitet efter begge operationer, kan en total kolektomi være en foretrukken behandling for HNPCC, især hos yngre patienter.
Der er en løbende kontrovers om fordelene ved 5-fluorouracil- baserede adjuvante terapier til HNPCC-relaterede kolorektale tumorer, især dem i trin I og II.
- Anti-PD-1 antistofbehandling kan være effektiv.
Checkpoint-blokade med anti-PD-1-behandling foretrækkes nu førstelinjeterapi til avanceret Microsatellite-Instabilitet – Høj kolorektal cancer.
Epidemiologi
Selvom den nøjagtige forekomst af Lynch-syndrom-forårsagende mutationer i den generelle befolkning stadig er ukendt, anslår nyere undersøgelser, at prævalensen er 1 ud af 279 individer eller 0,35%. Visse populationer vides at have en højere forekomst af grundlæggermutationer, herunder, men ikke begrænset til, franske canadiere , islændere , afroamerikanere og Ashkenazi -jøder . Lynch syndrom-forårsagende mutationer findes i cirka 3% af alle diagnosticerede kolorektale kræftformer og 1,8% af alle diagnosticerede endometriecancer. Gennemsnitsalderen for kræftdiagnose hos patienter med dette syndrom er 44 år gammel, sammenlignet med 64 år hos mennesker uden syndromet.
Terminologi
Henry T. Lynch , professor i medicin ved Creighton University Medical Center , karakteriserede syndromet i 1966. I sit tidligere arbejde beskrev han sygdommen som "kræftfamiliesyndrom". Udtrykket "Lynch syndrom" blev opfundet i 1984 af andre forfattere; Lynch navngav tilstanden HNPCC i 1985. Siden da er de to udtryk blevet brugt i flæng, indtil senere fremskridt i forståelsen af sygdommens genetik førte til, at udtrykket HNPCC faldt i unåde.
Andre kilder forbeholder sig udtrykket "Lynch syndrom", når der er en kendt DNA -mismatch -reparationsdefekt , og bruger udtrykket "familiel kolorektal cancer type X", når Amsterdam -kriterierne er opfyldt, men der ikke er nogen kendt DNA -mismatch -reparationsdefekt. De formodede "type X" -familier ser ud til at have en lavere samlet forekomst af kræft og lavere risiko for ikke-kolorektal kræft end familier med dokumenteret mangel på reparation af DNA-mismatch. Omkring 35% af de mennesker, der opfylder Amsterdam-kriterierne, har ikke en genmutation med DNA-mismatch-reparation.
Komplicerende spørgsmål er tilstedeværelsen af et alternativt sæt kriterier, kendt som "Bethesda -retningslinjerne".
Samfund
Der er en række non-profit organisationer, der leverer information og support, herunder Lynch Syndrome International , AliveAndKickn , Lynch Syndrome UK og Tarmkræft UK. I USA er National Lynch Syndrome Awareness Day den 22. marts.
Referencer
Yderligere læsning
Bøger
- McKay, Ami (2019). Datter af familie G.: en erindring om kræftgener, kærlighed og skæbne . Toronto: Alfred A. Knopf Canada. ISBN 978-0-345-80946-9. OCLC 1089450897 . Paperback -version med titlen Before My Time.
eksterne links
| Klassifikation | |
|---|---|
| Eksterne ressourcer |
