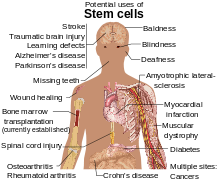
Stamcelleterapi - Stem-cell therapy
Stamcelleterapi er brug af stamceller til behandling eller forebyggelse af en sygdom eller tilstand. Fra 2016 er den eneste etablerede terapi ved hjælp af stamceller hæmatopoietisk stamcelletransplantation . Dette har normalt form af en knoglemarvstransplantation , men cellerne kan også stammer fra navlestrengsblod . Forskning er i gang for at udvikle forskellige kilder til stamceller samt at anvende stamcellebehandlinger til neurodegenerative sygdomme og tilstande som diabetes og hjertesygdomme .
Stamcelleterapi er blevet kontroversiel efter udviklinger såsom videnskabernes evne til at isolere og dyrke embryonale stamceller , til at oprette stamceller ved hjælp af somatiske cellekerneoverførsler og deres anvendelse af teknikker til at skabe inducerede pluripotente stamceller . Denne kontrovers er ofte relateret til abortpolitik og til kloning af mennesker . Derudover indsats for at markedsføre behandlinger baseret på transplantation af lagret navlestreng navlestrengsblod har været kontroversiel.
Medicinske anvendelser
I over 30 år er hæmatopoietisk stamcelletransplantation (HSCT) blevet brugt til at behandle mennesker med lidelser som leukæmi og lymfom ; dette er den eneste udbredte form for stamcelleterapi. Under kemoterapi dræbes de fleste voksende celler af de cytotoksiske midler. Disse midler kan imidlertid ikke skelne mellem leukæmi eller neoplastiske celler og de hæmatopoietiske stamceller i knoglemarven. Dette er bivirkningen af konventionelle kemoterapistrategier, som stamcelletransplantationen forsøger at vende; en donors sunde knoglemarv genindfører funktionelle stamceller for at erstatte de celler, der går tabt i værtens krop under behandlingen. De transplanterede celler genererer også et immunrespons, der hjælper med at dræbe kræftcellerne; denne proces kan imidlertid gå for langt, hvilket kan føre til transplantat vs værtsygdom , den alvorligste bivirkning af denne behandling.
En anden stamcelleterapi, kaldet Prochymal , blev betinget godkendt i Canada i 2012 til behandling af akut transplantat-mod-vært-sygdom hos børn, der ikke reagerer på steroider. Det er en allogen stamcelleterapi baseret på mesenkymale stamceller (MSC'er), der stammer fra knoglemarv hos voksne donorer. MSC'er renses fra marven, dyrkes og pakkes med op til 10.000 doser afledt af en enkelt donor. Doserne opbevares frosset, indtil det er nødvendigt.
FDA har godkendt fem hæmatopoietiske stamcelleprodukter, der stammer fra navlestrengsblod, til behandling af blod og immunologiske sygdomme.
I 2014 anbefalede Det Europæiske Lægemiddelagentur godkendelse af limbal stamceller til mennesker med alvorlig limbal stamcelle mangel på grund af forbrændinger i øjet.
Forskning
Stamceller undersøges af flere årsager. Molekyler og exosomer frigivet fra stamceller undersøges også i et forsøg på at lave medicin. Ud over funktionerne i selve cellerne har paracrinopløselige faktorer produceret af stamceller, kendt som stamcellesekretomet , vist sig at være en anden mekanisme, ved hvilken stamcellebaserede terapier formidler deres virkninger ved degenerative , autoimmune og inflammatoriske sygdomme .
Stamcelleudvidelse
For at blive brugt til forsknings- eller behandlingsapplikationer er der brug for et stort antal stamceller af høj kvalitet. Det er således nødvendigt at udvikle kultursystemer, der producerer rene populationer af vævsspecifikke stamceller in vitro uden tab af stamcellepotentiale. To hovedmetoder tages til dette formål: todimensionel og tredimensionel cellekultur.
Cellekultur i to dimensioner er rutinemæssigt blevet udført i tusinder af laboratorier verden over i de sidste fire årtier. I todimensionale platforme udsættes celler typisk for en fast, stiv flad overflade på basalsiden og for væske ved den apikale overflade. At bo i et sådant todimensionalt stift substrat kræver en dramatisk tilpasning til de overlevende celler, fordi de mangler den ekstracellulære matrix, der er unik for hver celletype, og som kan ændre cellemetabolisme og reducere dens funktionalitet.
Tredimensionelle cellekultursystemer kan skabe et biomimikerende mikromiljø for stamceller, der ligner deres native tredimensionelle ekstracellulære matrix (ECM). Avancerede biomaterialer har betydeligt bidraget til tredimensionelle cellekultursystemer i de seneste årtier, og mere unikke og komplekse biomaterialer er blevet foreslået til forbedring af stamcelleproliferation og kontrolleret differentiering. Blandt dem er nanostrukturerede biomaterialer af særlig interesse, fordi de har fordelen af et højt forhold mellem overflade og volumen, og de efterligner de fysiske og biologiske egenskaber ved naturligt ECM i nanoskalaen.
Ansøgninger
Neurodegeneration
Der er forsket i stamcellernes effekt på dyremodeller for hjernedegeneration , såsom ved Parkinsons sygdom , Amyotrofisk lateral sklerose og Alzheimers sygdom . Foreløbige undersøgelser relateret til multipel sklerose er blevet udført, og et fase 2 -forsøg i 2020 fandt signifikant forbedrede resultater for mesenkymale stamcellebehandlede patienter sammenlignet med dem, der modtog en lurvebehandling. I januar 2021 godkendte FDA det første kliniske forsøg med en stamcelleterapi med henblik på at genoprette tabte hjerneceller hos mennesker med fremskreden Parkinsons sygdom.
Sunde voksne hjerner indeholder neurale stamceller , som deler sig for at opretholde generelle stamcelleantal eller bliver stamceller . Hos raske voksne laboratoriedyr vandrer stamceller i hjernen og fungerer primært for at opretholde neuronpopulationer for lugt (lugtesansen). Farmakologisk aktivering af endogene neurale stamceller er blevet rapporteret at fremkalde neurobeskyttelse og adfærdsmæssig genopretning i voksne rottemodeller af neurologisk lidelse.
Hjerne- og rygmarvsskade
Stroke og traumatisk hjerneskade fører til celledød , karakteriseret ved tab af neuroner og oligodendrocytter i hjernen. Der er udført kliniske og dyreforsøg vedrørende brugen af stamceller i tilfælde af rygmarvsskade .
Svaghedssyndrom
En lille undersøgelse af personer på 60 år eller ældre med ældningssvaghed viste efter intravenøs behandling med MSC’er fra raske unge donorer betydelige forbedringer i fysiske præstationsmål.
Hjerte
Stamceller undersøges hos mennesker med alvorlig hjertesygdom . Arbejdet ved Bodo-Eckehard Strauer blev miskrediteret ved at identificere hundredvis af faktuelle modsætninger. Blandt flere kliniske forsøg, der rapporterer, at voksen stamcelleterapi er sikker og effektiv, er der kun rapporteret faktiske tegn på fordel ved kun få undersøgelser. Nogle indledende kliniske forsøg opnåede kun beskedne forbedringer i hjertefunktionen efter brug af knoglemarvsstamcelleterapi .
Stamcelleterapi til behandling af myokardieinfarkt gør normalt brug af autologe knoglemarvsstamceller, men andre typer af voksne stamceller kan anvendes, såsom fedtafledte stamceller.
Mulige genopretningsmekanismer omfatter:
- Generering af hjertemuskelceller
- Stimulerer vækst af nye blodkar for at genbefolke beskadiget hjertevæv
- Sekretion af vækstfaktorer
Kritik
I 2013 viste undersøgelser af autologe knoglemarvsstamceller om ventrikelfunktion at indeholde "hundredvis" af uoverensstemmelser. Kritikere rapporterer, at ud af 48 rapporter syntes kun fem underliggende forsøg at blive brugt, og at det i mange tilfælde var modstridende mellem rapporterne om det samme forsøg, om de var randomiserede eller blot observationsmæssige accept-versus-afviser. Et par rapporter om identiske baseline-karakteristika og endelige resultater blev præsenteret i to publikationer som henholdsvis et randomiseret forsøg med 578 patienter og som et 391-forsøgs observationsstudie. Andre rapporter krævede (umulige) negative standardafvigelser i undersæt af mennesker eller indeholdt fraktionerede emner, negative NYHA -klasser. Samlet set blev der rapporteret om mange flere mennesker, der havde modtaget stamceller i forsøg, end antallet af stamceller, der blev behandlet på hospitalets laboratorium i løbet af denne tid. En universitetsundersøgelse, lukket i 2012 uden rapportering, blev genåbnet i juli 2013.
I 2014 afslørede en metaanalyse af stamcelleterapi ved hjælp af knoglemarvsstamceller til hjertesygdomme uoverensstemmelser i offentliggjorte kliniske forsøgsrapporter, hvorved undersøgelser med et større antal uoverensstemmelser viste en stigning i effektstørrelser. En anden metaanalyse baseret på de intra-subjekt data fra 12 randomiserede forsøg kunne ikke finde nogen væsentlige fordele ved stamcelleterapi på primære endepunkter, såsom større bivirkninger eller stigning i hjertefunktionsforanstaltninger, hvilket konkluderede, at der ikke var nogen fordel.
TIME-forsøget, der brugte et randomiseret, dobbeltblindet, placebokontrolleret forsøgsdesign, konkluderede, at "mononukleære celleadministration af knoglemarv ikke forbedrede genopretning af LV-funktion over 2 år" hos mennesker, der havde et myokardieinfarkt. Følgelig rapporterede BOOST-2-forsøget udført i 10 medicinske centre i Tyskland og Norge, at forsøgsresultatet "ikke understøtter brugen af kerneformede BMC'er hos patienter med STEMI og moderat reduceret LVEF". Desuden opfyldte forsøget heller ikke andre sekundære MRI -endepunkter, hvilket førte til en konklusion om, at intrakoronar knoglemarvsstamcelleterapi ikke giver en funktionel eller klinisk fordel.
Dannelse af blodceller
Specificiteten af det humane immuncelle-repertoire er det, der gør det muligt for menneskekroppen at forsvare sig mod hurtigt tilpasning af antigener. Imidlertid er immunsystemet sårbart over for nedbrydning ved sygdommens patogenese, og på grund af den kritiske rolle, det spiller i det samlede forsvar, er dets nedbrydning ofte dødelig for organismen som helhed. Sygdomme i hæmatopoietiske celler diagnosticeres og klassificeres via en subspecialitet af patologi kendt som hæmatopatologi . Immuncellernes specificitet er det, der tillader genkendelse af fremmede antigener, hvilket forårsager yderligere udfordringer i behandlingen af immunsygdomme. Identiske match mellem donor og modtager skal foretages for vellykkede transplantationsbehandlinger, men matches er ualmindelige, selv mellem førstegrads slægtninge. Forskning ved hjælp af både hæmatopoietiske voksne stamceller og embryonale stamceller har givet indsigt i de mulige mekanismer og metoder til behandling af mange af disse lidelser.
Fuldt modne humane røde blodlegemer kan genereres ex vivo af hæmatopoietiske stamceller (HSC'er), som er forstadier til røde blodlegemer. I denne proces dyrkes HSC'er sammen med stromaceller , hvilket skaber et miljø, der efterligner betingelserne i knoglemarv, det naturlige sted for vækst af røde blodlegemer. Erythropoietin , en vækstfaktor , tilføjes, hvilket lokker stamcellerne til at fuldføre terminal differentiering til røde blodlegemer. Yderligere forskning i denne teknik bør have potentielle fordele for genterapi, blodtransfusion og aktuel medicin.
Regrowing tænder
I 2004 opdagede forskere ved King's College London en måde at dyrke en komplet tand hos mus og var i stand til at dyrke biotekniske tænder enkeltstående i laboratoriet. Forskere er overbeviste om, at tandregenereringsteknologien kan bruges til at dyrke levende tænder hos mennesker.
I teorien kan stamceller taget fra patienten blive lokket i laboratoriet og blive til en tandknopp, der, når den implanteres i tandkødet, vil give anledning til en ny tand og forventes at blive dyrket i løbet af tre uger. Det vil smelte sammen med kæbebenet og frigive kemikalier, der tilskynder nerver og blodkar til at forbinde det. Processen ligner det, der sker, når mennesker vokser deres oprindelige voksne tænder. Mange udfordringer er imidlertid tilbage, før stamceller kan være et valg til udskiftning af manglende tænder i fremtiden.
Cochlear hårcelles genvækst
Heller har rapporteret succes med genvoksende cochleahårceller ved brug af embryonale stamceller .
I en anmeldelse fra 2019, der kiggede på høregenerering og regenerativ medicin, har stamcelleafledte otiske forfædre potentialet til i høj grad at forbedre hørelsen.
Blindhed og synshandicap
Siden 2003 har forskere med succes transplanteret hornhindestamceller i beskadigede øjne for at genoprette synet. "Ark af nethindeceller, der bruges af teamet, høstes fra aborterede fostre, som nogle mennesker finder stødende." Når disse plader transplanteres over den beskadigede hornhinde , stimulerer stamcellerne fornyet reparation og i sidste ende genopretter synet. Den seneste udvikling var i juni 2005, da forskere ved Queen Victoria Hospital i Sussex , England, var i stand til at genoprette synet af fyrre mennesker ved hjælp af den samme teknik. Gruppen, ledet af Sheraz Daya , var i stand til med succes at bruge voksne stamceller hentet fra patienten, en slægtning eller endda en kadaver . Yderligere forsøgsrunder er i gang.
Pancreas betaceller
Mennesker med type 1 diabetes mister funktionen af insulin -producerende beta-celler i bugspytkirtlen. I de seneste eksperimenter har forskere kunnet lokke embryonale stamceller til at blive til betaceller i laboratoriet. I teorien, hvis betacellen transplanteres med succes, vil de være i stand til at erstatte funktionsfejl i en diabetespatient.
Ortopædi
Anvendelse af mesenkymale stamceller (MSC'er), der stammer fra voksne stamceller, er under foreløbig forskning til potentielle ortopædiske anvendelser inden for knogle- og muskeltraumer, bruskreparation , slidgigt , intervertebral diskoperation, rotatormanchetkirurgi og muskuloskeletale lidelser , blandt andre. Andre områder inden for ortopædisk forskning til anvendelse af MSC'er omfatter vævsteknik og regenerativ medicin .
Sårheling
Stamceller kan også bruges til at stimulere væksten af humane væv. Hos en voksen erstattes såret væv oftest af arvæv , som er karakteriseret i huden ved uorganiseret kollagenstruktur, tab af hårsække og uregelmæssig vaskulær struktur. I tilfælde af såret føtalvæv udskiftes såret væv imidlertid med normalt væv gennem aktivitet af stamceller. En mulig metode til vævsregenerering hos voksne er at placere voksne stamcelle "frø" inde i et vævsleje "jord" i et sårbed og lade stamcellerne stimulere differentiering i vævsbedcellerne. Denne metode fremkalder et regenerativt svar, der mere ligner føtal sårheling end voksen dannelse af arvæv. Forskere undersøger stadig forskellige aspekter af "jord" -vævet, der bidrager til regenerering. På grund af stamcellernes generelle helbredende evner har de vundet interesse for behandling af kutane sår, såsom i hudkræft .
HIV/AIDS
Ødelæggelse af immunsystemet af HIV er drevet af tabet af CD4+ T -celler i det perifere blod og lymfoide væv. Viral indtræden i CD4+ celler medieres af interaktionen med en cellulær kemokinreceptor, hvoraf den mest almindelige er CCR5 og CXCR4 . Fordi efterfølgende viral replikation kræver cellulære genekspressionsprocesser, er aktiverede CD4+ -celler de primære mål for produktiv HIV -infektion. For nylig har forskere undersøgt en alternativ tilgang til behandling af HIV-1/AIDS, baseret på oprettelsen af et sygdomsresistent immunsystem gennem transplantation af autologe, genmodificerede (HIV-1-resistente) hæmatopoietiske stam- og stamceller (GM- HSPC).
Kliniske forsøg
Regenerative behandlingsmodeller
Stamceller menes at formidle reparation via fem primære mekanismer: 1) giver en antiinflammatorisk virkning, 2) homing til beskadigede væv og rekruttering af andre celler, såsom endotelcellestamceller , der er nødvendige for vævsvækst, 3) understøtter vævsremodellering over ardannelse, 4) hæmning af apoptose og 5) differentiering til knogle, brusk, sener og ledbåndsvæv.
For yderligere at berige blodtilførslen til de beskadigede områder og følgelig fremme vævsregenerering kunne blodpladerigt plasma bruges i forbindelse med stamcelletransplantation. Effekten af nogle stamcellepopulationer kan også påvirkes af leveringsmetoden; for eksempel for at regenerere knogle introduceres stamceller ofte i et stillads, hvor de producerer de mineraler, der er nødvendige for dannelse af funktionel knogle.
Stamceller har også vist sig at have en lav immunogenicitet på grund af det relativt lave antal MHC -molekyler, der findes på deres overflade. Derudover har de vist sig at udskille kemokiner, der ændrer immunresponset og fremmer tolerance for det nye væv. Dette gør det muligt at udføre allogene behandlinger uden høj risiko for afvisning.
Lægemiddelfund og biomedicinsk forskning
Evnen til at vokse op på funktionelt voksenvæv på ubestemt tid i kulturen gennem Directed differentiering skaber nye muligheder for medicinforskning. Forskere er i stand til at vokse op med differentierede cellelinjer og derefter teste nye lægemidler på hver celletype for at undersøge mulige interaktioner in vitro, før de udfører in vivo -undersøgelser. Dette er afgørende for udviklingen af lægemidler til brug i veterinærforskning på grund af mulighederne for artsspecifikke interaktioner. Håbet er, at at have disse cellelinjer til rådighed til forskningsbrug vil reducere behovet for forsøgsdyr, fordi virkninger på humant væv in vitro vil give indsigt, der normalt ikke er kendt før dyreforsøgsfasen.
- Med fremkomsten af inducerede pluripotente stamceller (iPSC) er det muligt at undersøge og skabe behandlinger til brug hos truede lavproduktionsdyr. I stedet for at skulle høste embryoner eller æg, som er begrænsede, kan forskerne fjerne mesenkymale stamceller med større lethed og i høj grad reducere faren for dyret på grund af ikke -invasive teknikker. Dette gør det muligt kun at anvende de begrænsede æg til reproduktive formål.
Bevarelse
Stamceller undersøges til brug i bevarelsesindsatser. Spermatogoniale stamceller er blevet høstet fra en rotte og placeret i en musvært, og fuldt modne sædceller blev produceret med evnen til at producere levedygtige afkom. I øjeblikket forskes der i gang for at finde egnede værter til introduktion af donorspermatogoniale stamceller. Hvis dette bliver en levedygtig mulighed for bevarere, kan sæd produceres fra personer af høj genetisk kvalitet, der dør, før de når seksuel modenhed, og bevarer en linje, der ellers ville gå tabt.
Kilder til stamceller
De fleste stamceller beregnet til regenerativ terapi er generelt isoleret enten fra patientens knoglemarv eller fra fedtvæv . Mesenkymale stamceller kan differentiere sig til de celler, der udgør knogle, brusk, sener og ledbånd, såvel som muskler, neurale og andre stamceller. De har været hovedtypen af stamceller undersøgt i behandlingen af sygdomme, der påvirker disse væv. Antallet af stamceller transplanteret i beskadiget væv kan ændre behandlingens effektivitet. Derfor dyrkes stamceller, der stammer fra knoglemarvsaspirater, for eksempel i specialiserede laboratorier til ekspansion til millioner af celler. Selvom fedtafledt væv også kræver behandling før brug, er dyrkningsmetodikken for fedtafledte stamceller ikke så omfattende som for knoglemarvsafledte celler. Mens det menes, at knoglemarvsafledte stamceller foretrækkes til knogler, brusk, ledbånd og senereparation, mener andre, at de mindre udfordrende indsamlingsteknikker og det multicellulære mikromiljø, der allerede findes i fedtafledte stamcellefraktioner, gør sidstnævnte den foretrukne kilde til autolog transplantation.
Nye kilder til mesenkymale stamceller undersøges, herunder stamceller til stede i huden og dermis, som er af interesse på grund af den lethed, hvormed de kan høstes med minimal risiko for dyret. Hæmatopoietiske stamceller er også blevet opdaget at bevæge sig i blodstrømmen og have samme differentieringsevne som andre mesenkymale stamceller, igen med en meget ikke-invasiv høstteknik.
Der har været nyere interesse for brugen af ekstra embryonale mesenkymale stamceller. Forskning er i gang for at undersøge de differentierende muligheder for stamceller, der findes i navlestrengen, æggeblommesækken og moderkagen fra forskellige dyr. Disse stamceller menes at have mere differentieringsevne end deres voksne modstykker, herunder evnen til lettere at danne væv af endodermal og ektodermal oprindelse.
Embryonale stamcellelinjer
Der er udbredt kontrovers om brugen af humane embryonale stamceller . Denne kontrovers retter sig primært mod de teknikker, der bruges til at udlede nye embryonale stamcellelinjer , hvilket ofte kræver ødelæggelse af blastocysten . Modstand mod brugen af menneskelige embryonale stamceller i forskning er ofte baseret på filosofiske, moralske eller religiøse indvendinger. Der er anden stamcelleforskning, der ikke involverer ødelæggelse af et menneskeligt embryo, og sådan forskning involverer voksne stamceller, fosterstamceller og inducerede pluripotente stamceller.
Den 23. januar 2009 gav US Food and Drug Administration Geron Corporation tilladelse til at starte det første kliniske forsøg med en embryonisk stamcellebaseret terapi på mennesker. Forsøget havde til formål at evaluere stoffet GRNOPC1, embryonale stamcelle -afledte oligodendrocyt stamceller, på mennesker med akut rygmarvsskade . Forsøget blev afbrudt i november 2011, så virksomheden kunne fokusere på terapier i "det nuværende miljø med mangel på kapital og usikre økonomiske forhold". I 2013 bioteknologi og regenerativ medicin selskab BioTime ( AMEX : BTX ) erhvervede Gerons stamceller aktiver i en bestand transaktion, med det formål at genstarte det kliniske forsøg.
Mesenkymale stromaceller (MSC'er)
Forskere har rapporteret, at MSC'er, når de transfunderes umiddelbart inden for få timer efter optøning, kan vise nedsat funktion eller vise nedsat effekt ved behandling af sygdomme sammenlignet med de MSC'er, der er i logfase af cellevækst (frisk), så kryokonserverede MSC'er bør bringes tilbage i loggen fase af cellevækst i invitro -kultur før administration. Omdyrkning af MSC'er hjælper med at komme sig efter det stød, cellerne får under frysning og optøning. Forskellige MSC kliniske forsøg, der brugte kryokonserveret produkt umiddelbart efter optøning, har mislykkedes i forhold til de kliniske forsøg, der brugte friske MSC'er.
Veterinærmedicin
Der er forsket i heste, hunde og katte, der kan gavne udviklingen af stamcellebehandlinger inden for veterinærmedicin og kan målrette mod en lang række skader og sygdomme som myokardieinfarkt , slagtilfælde, seneskader og ledbåndsskader , slidgigt , osteochondrose og muskeldystrofi både hos store dyr, såvel som mennesker. Mens undersøgelse af cellebaserede terapier generelt afspejler menneskelige medicinske behov, har den høje grad af hyppighed og sværhedsgrad af visse skader i racerheste sat veterinærmedicin i spidsen for denne nye regenerative tilgang. Ledsagende dyr kan tjene som klinisk relevante modeller, der tæt efterligner menneskelig sygdom.
Kilder til stamceller
Veterinære anvendelser af stamcelleterapi som et middel til vævsregenerering er stort set blevet formet af forskning, der begyndte med brug af voksenafledte mesenkymale stamceller til behandling af dyr med skader eller defekter, der påvirker knogler, brusk, ledbånd og/eller sener. Der er to hovedkategorier af stamceller, der bruges til behandlinger: allogene stamceller, der stammer fra en genetisk forskellig donor inden for samme art og autologe mesenkymale stamceller, afledt af patienten før brug i forskellige behandlinger. En tredje kategori, xenogene stamceller eller stamceller, der stammer fra forskellige arter, bruges primært til forskningsformål, især til menneskelige behandlinger.
Knoglereparation
Knogle har en unik og veldokumenteret naturlig helingsproces, der normalt er tilstrækkelig til at reparere brud og andre almindelige skader. Fejljusterede pauser på grund af alvorlige traumer samt behandlinger som tumorresektioner af knoglekræft er tilbøjelige til forkert heling, hvis de overlades til den naturlige proces alene. Stilladser, der består af naturlige og kunstige komponenter, podes med mesenkymale stamceller og placeres i defekten. Inden for fire uger efter placeringen af stilladset begynder den nydannede knogle at integrere sig med den gamle knogle, og inden for 32 uger opnås fuld forening. Yderligere undersøgelser er nødvendige for fuldt ud at karakterisere brugen af cellebaserede terapier til behandling af knoglebrud.
Stamceller er blevet brugt til behandling af degenerative knoglesygdomme. Den normalt anbefalede behandling til hunde, der har Legg – Calve – Perthes sygdom, er at fjerne lårbens hoved efter degenerationen er skredet frem. For nylig er mesenkymale stamceller blevet injiceret direkte ind i lårbenets hoved, med succes ikke kun i knogleregenerering, men også i smertereduktion.
Reparation af ledbånd og sener
Autologe stamcellebaserede behandlinger for ledbåndsskade , seneskade , slidgigt , osteochondrose og sub-chondral knoglecyster har været kommercielt tilgængelige for praktiserende dyrlæger til behandling af heste siden 2003 i USA og siden 2006 i Storbritannien. Autologe stamcellebaserede behandlinger for seneskader, ledbåndsskader og slidgigt hos hunde har været tilgængelige for dyrlæger i USA siden 2005. Over 3000 privatejede heste og hunde er blevet behandlet med autologe fedtafledte stamceller. Effekten af disse behandlinger er blevet vist i dobbeltblindede kliniske forsøg med hunde med slidgigt i hofte og albue og heste med seneskader.
Raceheste er især tilbøjelige til skader på sener og ledbånd. Konventionelle terapier er meget mislykkedes med at bringe hesten tilbage til fuldt fungerende potentiale. Naturlig helbredelse, styret af de konventionelle behandlinger, fører til dannelsen af fibrøst arvæv, der reducerer fleksibilitet og fuld ledbevægelse. Traditionelle behandlinger forhindrede et stort antal heste i at vende tilbage til fuld aktivitet og har også en høj forekomst af genskader på grund af den arvede senes stive karakter. Introduktion af både knoglemarv og fedtafledte stamceller sammen med naturlig mekanisk stimulans fremmede regenerering af senevæv. Den naturlige bevægelse fremmede tilpasningen af de nye fibre og tendocytter med den naturlige justering, der findes i uskadte sener. Stamcellebehandling tillod ikke kun flere heste at vende tilbage til fuld vagt og reducerede også voldsomt antallet af skader igen over en treårig periode.
Brugen af embryonale stamceller er også blevet anvendt til senereparation. De embryonale stamceller viste sig at have en bedre overlevelsesrate i senen samt bedre migreringsevner for at nå alle områder af beskadiget sen. Den samlede reparationskvalitet var også højere med bedre senarkitektur og kollagen dannet. Der blev heller ikke set en tumordannelse i løbet af den tre måneder lange forsøgsperiode. Langsigtede undersøgelser skal udføres for at undersøge den langsigtede effekt og risici forbundet med brugen af embryonale stamceller. Lignende resultater er fundet hos små dyr.
Fælles reparation
Slidgigt er hovedårsagen til ledsmerter både hos dyr og mennesker. Heste og hunde er oftest ramt af gigt. Naturlig bruskregenerering er meget begrænset. Forskellige typer mesenkymale stamceller og andre tilsætningsstoffer undersøges stadig for at finde den bedste celletype og metode til langtidsbehandling.
Fedtafledte mesenkymale celler bruges i øjeblikket oftest til stamcellebehandling af slidgigt på grund af den ikke-invasive høst. Dette er en nyligt udviklet, ikke-invasiv teknik udviklet til lettere klinisk brug. Hunde, der modtog denne behandling, viste større fleksibilitet i deres led og mindre smerter.
Muskel reparationer
Stamceller er med succes blevet brugt til at forbedre helingen i hjertet efter myokardieinfarkt hos hunde. Fedt- og knoglemarvsafledte stamceller blev fjernet og induceret til en hjertecelles skæbne, inden de blev injiceret i hjertet. Hjertet viste sig at have forbedret kontraktilitet og en reduktion i det beskadigede område fire uger efter, at stamcellerne blev påført.
Et andet forsøg er i gang med et plaster lavet af et porøst stof, som stamcellerne "seedes" på for at fremkalde vævsregenerering ved hjertefejl. Væv blev regenereret, og plasteret blev godt inkorporeret i hjertevævet. Dette menes delvis at skyldes forbedret angiogenese og reduktion af inflammation. Selvom der blev produceret kardiomyocytter fra de mesenkymale stamceller, så de ikke ud til at være kontraktile. Andre behandlinger, der fremkaldte en hjerteskæbne i cellerne før transplantation, havde større succes med at skabe kontraktilt hjertevæv.
Nyere forskning, såsom det europæiske nTRACK -forskningsprojekt, har til formål at demonstrere, at multimodale nanopartikler strukturelt og funktionelt kan spore stamceller i muskelregenereringsterapi. Ideen er at mærke stamceller med guld-nano-partikler, der er fuldt ud karakteriseret for optagelse, funktionalitet og sikkerhed. De mærkede stamceller injiceres i en skadet muskel og spores ved hjælp af billeddannelsessystemer. Imidlertid skal systemet stadig demonstreres i laboratorieskala.
Reparation af nervesystemet
Rygmarvsskader er en af de mest almindelige traumer, der indbringes på veterinærhospitaler. Spinalskader opstår på to måder efter traumet: den primære mekaniske skade og i sekundære processer, som betændelse og ardannelse, i dagene efter traumet. Disse celler involveret i det sekundære skaderespons udskiller faktorer, der fremmer ardannelse og hæmmer cellulær regenerering. Mesenkymale stamceller, der induceres til en neural celleskæbne, læsses på et porøst stillads og implanteres derefter på skadestedet. Cellerne og stilladset udskiller faktorer, der modvirker dem, der udskilles af ardannende celler og fremmer neural regenerering. Otte uger senere viste hunde, der blev behandlet med stamceller, en enorm forbedring i forhold til dem, der blev behandlet med konventionelle terapier. Hunde behandlet med stamceller kunne lejlighedsvis understøtte deres egen vægt, hvilket ikke er set hos hunde, der gennemgår konventionelle behandlinger.
I en undersøgelse for at evaluere behandlingen af eksperimentelt induceret MS hos hunde ved hjælp af laseraktiverede ikke-ekspanderede fedtafledte stamceller. Resultaterne viste forbedring af de kliniske tegn over tid bekræftet af opløsningen af de tidligere læsioner på MR. Positiv migration af de injicerede celler til læsionsstedet, øget remyelinisering påvist af Myelin Basic Proteins, positiv differentiering til Olig2 positive oligodendrocytter, forhindrede dannelse af glialarret og restaureret axonal arkitektur.
Behandlinger er også i kliniske forsøg for at reparere og regenerere perifere nerver. Perifere nerver er mere tilbøjelige til at blive beskadiget, men virkningerne af skaden er ikke så udbredt som man ser ved skader på rygmarven. Behandlinger er i øjeblikket i kliniske forsøg med at reparere afskårne nerver med tidlig succes. Stamceller induceret til en neural skæbne injiceret i en afskåret nerve. Inden for fire uger blev regenerering af tidligere beskadigede stamceller og fuldstændigt dannede nervebundter observeret.
Stamceller er også i kliniske faser til behandling i oftalmologi. Hæmatopoietiske stamceller er blevet brugt til behandling af hornhindeår af forskellig oprindelse hos flere heste. Disse sår var resistente over for konventionelle tilgængelige behandlinger, men reagerede hurtigt positivt på stamcellebehandlingen. Stamceller var også i stand til at genoprette synet i det ene øje af en hest med nethindeløsning, så hesten kunne vende tilbage til daglige aktiviteter.
Samfund og kultur
Marketing og omkostninger
I slutningen af 1990'erne og begyndelsen af 2000'erne var der en indledende bølge af virksomheder og klinikker, der tilbyder stamcelleterapi, uden at de underbygger sundhedsanprisninger eller har lovgivningsmæssig godkendelse. I 2012 var der opstået en anden bølge af virksomheder og klinikker, normalt placeret i udviklingslande, hvor medicin er mindre reguleret og tilbyder stamcelleterapier efter en medicinsk turismemodel . Ligesom de første bølgeselskaber og klinikker fremsatte de lignende stærke, men ubegrundede påstande, hovedsageligt af klinikker i USA, Mexico, Thailand, Indien og Sydafrika . I 2016 viste forskning, at der var mere end 550 stamcelleklinikker alene i USA, der sælger generelt uprøvede behandlinger til en lang række medicinske tilstande i næsten alle stater i landet, hvilket ændrer dynamikken i stamcelleturisme . I 2018 sendte FDA et advarselsbrev til StemGenex Biologic Laboratories i San Diego, som markedsførte en tjeneste, hvor det tog kropsfedt fra mennesker, forarbejdede det til blandinger, som det sagde indeholdt forskellige former for stamceller og administrerede det tilbage til personen ved inhalation, intravenøst eller infusion i deres rygmarv; virksomheden sagde, at behandlingen var nyttig til mange kroniske og livstruende tilstande.
Omkostninger ved stamcelleterapier spænder vidt efter klinik, tilstand og celletype, men ligger oftest mellem $ 10.000-$ 20.000. Forsikring dækker ikke stamcelleinjektioner på klinikker, så patienter bruger ofte online indsamling. I 2018 fandt den amerikanske føderale handelskommission sundhedscentre og en individuel læge, der fremsatte ubegrundede påstande om stamcelleterapier og tvunget refusion på omkring $ 500.000. FDA anlagde sag mod to stamcelleklinikfirmaer omkring samme tid og søgte permanente påbud mod deres markedsføring og brug af ikke -godkendte fedtstamcelleprodukter.
Selvom der ifølge NIH ingen stamcellebehandlinger er blevet godkendt til COVID-19, og agenturet anbefaler at bruge MSC'er til sygdommen, begyndte nogle stamcelleklinikker at markedsføre både uprøvede og ikke-FDA-godkendte stamceller og exosomer for COVID-19 19 i 2020. FDA tog hurtig handling ved at sende breve til de pågældende virksomheder. FTC advarede også et stamcellefirma om COVID-19-relateret markedsføring.