Erythropoiesis - Erythropoiesis
Erythropoiesis (fra græsk 'erythro', der betyder "rød" og "poiesis" "at lave") er den proces, der producerer røde blodlegemer (erythrocytter), som er udviklingen fra erytropoietiske stamceller til modne røde blodlegemer.
Det stimuleres af nedsat O 2 i omløb, som detekteres af nyrerne , som derefter udskiller hormonet erythropoietin . Dette hormon stimulerer proliferation og differentiering af forstadier til røde blodlegemer, som aktiverer øget erythropoiesis i de hæmopoietiske væv og i sidste ende producerer røde blodlegemer (erythrocytter). Hos postnatale fugle og pattedyr (herunder mennesker ) forekommer dette normalt inden for den røde knoglemarv . I det tidlige foster finder erythropoiesis sted i de mesodermale celler i æggeblommesækken . I den tredje eller fjerde måned flytter erythropoiesis til leveren. Efter syv måneder forekommer erythropoiesis i knoglemarven. Øget fysisk aktivitet kan forårsage en stigning i erythropoiesis. Men hos mennesker med visse sygdomme og hos nogle dyr forekommer erythropoiesis også uden for knoglemarven , inden for milten eller leveren . Dette kaldes ekstramedullær erythropoiesis .
Den knoglemarven af stort set alle de knogler producerer røde blodlegemer, indtil en person er omkring fem år gammel. Den skinneben og lårben ophører med at være vigtige steder i hematopoiese ved omkring 25 år; de ryghvirvler , brystben , bækken og ribben , og kranieknogler fortsætte med at producere røde blodlegemer gennem hele livet. Op til en alder af 20 år produceres RBC'er fra rødt knoglemarv i alle knoglerne (lange knogler og alle de flade knogler). Efter en alder af 20 år produceres RBC'er fra membranøse knogler såsom hvirvler, brystbenet, ribben, skulderblad og iliacaknogler. Efter 20 års alder bliver akslen af de lange knogler til gul knoglemarv på grund af fedtdeponering og mister den erytropoietiske funktion.
Erythrocytdifferentiering
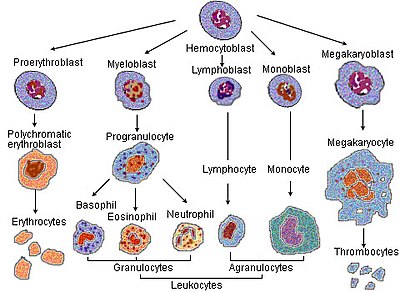
I processen med modning af rødt blodlegeme gennemgår en celle en række differentieringer . Følgende udviklingsstadier forekommer alle inden for knoglemarven :
- En hæmocytoblast , en multipotent hæmatopoietisk stamcelle , bliver
- en fælles myeloid stamfar eller en multipotent stamcelle , og derefter
- en enmægtig stamcelle, altså
- en pronormoblast , også almindeligvis kaldet en proerythroblast eller en rubriblast.
- Dette bliver en basofil eller tidlig normoblast, også almindeligvis kaldet en erythroblast
- en polykromatofil eller mellemliggende normoblast, derefter
- en ortokromatisk eller sen normoblast. På dette stadium udvises kernen, før cellen bliver
- en retikulocyt .
Cellen frigives fra knoglemarven efter trin 7, og så i nycirkulerende røde blodlegemer er der omkring 1% reticulocytter. Efter en til to dage bliver disse i sidste ende til "erythrocytter" eller modne røde blodlegemer.
Disse faser svarer til specifikke optrædener af cellen, når de farves med Wrights plet og undersøges ved lysmikroskopi, og svarer til andre biokemiske ændringer.
I modningsprocessen konverteres en basofil pronormoblast fra en celle med en stor kerne og et volumen på 900 fL til en enukleret skive med et volumen på 95 fL. Ved retikulocytstadiet har cellen ekstruderet sin kerne, men er stadig i stand til at producere hæmoglobin.
Afgørende for modning af røde blodlegemer er vitamin B 12 (cobalamin) og vitamin B 9 (folinsyre). Mangel på enten forårsager modningssvigt i processen med erythropoiesis, hvilket klinisk manifesterer sig som reticulocytopeni , en unormalt lav mængde reticulocytter.
Karakteristika set i erytrocytter under erythropoiesis
Efterhånden som de modnes, ændres en række erytrocytkarakteristika: Den samlede størrelse af erythroid -precursorcellen reduceres, når forholdet mellem cytoplasma og kerne (C: N) stiger. Kernediameteren falder, og chromatin kondenserer med farvningsreaktionen, der skrider frem fra purpurrød til mørkeblå på det sidste atomstadium af ortokromatisk erythroblast, før atomudstødning. Cytoplasmaets farve ændres fra blå ved proerythroblast og basofile stadier til en lyserød rød som et resultat af det stigende udtryk for hæmoglobin, efterhånden som cellen udvikler sig. I første omgang er kernen stor i størrelse og indeholder åbent kromatin . Men efterhånden som de røde blodlegemer modnes, falder kernens størrelse, indtil den til sidst forsvinder med kondensationen af kromatinmaterialet.
Regulering af erythropoiesis
En feedback-loop, der involverer erythropoietin, hjælper med at regulere processen med erythropoiesis, så produktionen af røde blodlegemer er lig med ødelæggelsen af røde blodlegemer i ikke-sygdomstilstande, og antallet af røde blodlegemer er tilstrækkeligt til at opretholde tilstrækkelige iltniveauer i væv, men ikke så højt, at det forårsager slam, trombose eller slagtilfælde . Erythropoietin produceres i nyrerne og leveren som reaktion på lave iltniveauer. Derudover er erythropoietin bundet af cirkulerende røde blodlegemer; lave cirkulerende tal fører til et relativt højt niveau af ubundet erythropoietin, som stimulerer produktionen i knoglemarven.
Nylige undersøgelser har også vist, at peptidhormonet hepcidin kan spille en rolle i reguleringen af hæmoglobinproduktion og dermed påvirke erythropoiesis. Leveren producerer hepcidin. Hepcidin styrer jernabsorptionen i mave -tarmkanalen og jernfrigivelse fra reticuloendothelialt væv. Jern skal frigives fra makrofager i knoglemarven for at blive inkorporeret i hæmogruppen af hæmoglobin i erytrocytter. Der er kolonidannende enheder, som cellerne følger under deres dannelse. Disse celler omtales som de engagerede celler, herunder granulocytmonocytkolonidannende enheder.
Udskillelsen af hepcidin hæmmes af et andet hormon, erythroferron , produceret af erythroblaster som reaktion på erythropoietin, og identificeret i 2014. Det ser ud til, at dette forbinder erythropoietin-drevet eyrthropoiesis med den jernmobilisering, der er nødvendig for hæmoglobinsyntese.
Tab af funktion af erythropoietinreceptoren eller JAK2 i museceller forårsager svigt i erythropoiesis, så produktionen af røde blodlegemer i embryoner og vækst forstyrres. Hvis der ikke er nogen systemisk feedback -hæmning , f.eks. Formindskelse eller fravær af suppressorer af cytokinsignalproteiner, kan der opstå gigantisme som vist i musemodeller .
Stress erythropoiesis
Ud over erythropoiesis ved steady state, stimulerer akut anæmi sandsynligvis en anden reaktion, der resulterer i hurtig udvikling af nye røde blodlegemer.Dette er blevet undersøgt hos rotter og sker i leveren gennem aktivering af den BMP4-afhængige stress-erythropoiesis-vej.
Se også
- Anæmi : en tilstand med et unormalt lavt funktionelt hæmoglobin
- Polycytæmi : en tilstand med et unormalt højt niveau af røde blodlegemer
- Dyserythropoiesis : et problem med udviklingen af røde blodlegemer