Arvelig spherocytose - Hereditary spherocytosis
| Arvelig spherocytose | |
|---|---|
| Andre navne | Minkowski -Chauffard syndrom |
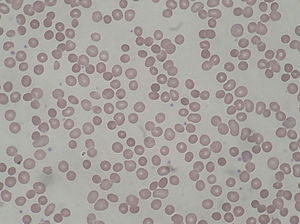 | |
| Perifert blodudstrygning fra patient med arvelig sfærocytose | |
| Specialitet | Hæmatologi |
Arvelig spherocytose er en abnormitet i røde blodlegemer eller erytrocytter . Det er en kronisk sygdom uden kur. Lidelsen er forårsaget af mutationer i gener relateret til membranproteiner, der gør det muligt for erytrocytterne at ændre form. De unormale erytrocytter er kugleformede ( sfærocytose ) frem for den normale bikonkave skiveformede. Dysfunktionelle membranproteiner forstyrrer cellens evne til at være fleksibel til at rejse fra arterierne til de mindre kapillærer . Denne forskel i form gør også de røde blodlegemer mere tilbøjelige til at briste . Celler med disse dysfunktionelle proteiner nedbrydes i milten . Denne mangel på erytrocytter resulterer i hæmolytisk anæmi .
Det blev først beskrevet i 1871. Det er den mest almindelige årsag til arvelig hæmolyse i europæiske og nordamerikanske kaukasiske befolkninger med en forekomst af 1 ud af 5000 fødsler. Den kliniske sværhedsgrad af HS varierer fra symptomfri bærer til alvorlig hæmolyse, fordi lidelsen udviser ufuldstændig penetration i sit udtryk .
Symptomer omfatter anæmi, gulsot, splenomegali og træthed . Desuden ophobes detritus af de nedbrudte blodlegemer-ukonjugeret eller indirekte bilirubin -i galdeblæren og kan få pigmenterede galdesten til at udvikle sig. Hos kroniske patienter kan en infektion eller anden sygdom forårsage en stigning i ødelæggelsen af røde blodlegemer, hvilket resulterer i udseendet af akutte symptomer, en hæmolytisk krise . På en blodprøve kan Howell-Jolly-kroppe ses inden for røde blodlegemer. Primær behandling for patienter med symptomatisk HS har været total splenektomi , som eliminerer den hæmolytiske proces, hvilket tillader normale hæmoglobin- , reticulocyt- og bilirubinniveauer . Sfærocytosepatienter, der er heterozygote for et hæmokromatosegen , kan lide af jernoverbelastning, på trods af at hæmokromatosegenerne er recessive.
Akutte tilfælde kan true med at forårsage hypoxi gennem anæmi og akut kernicterus gennem høje blodniveauer af bilirubin, især hos nyfødte. De fleste tilfælde kan opdages kort tid efter fødslen. En voksen med denne sygdom bør have deres børn testet, selv om sygdommens tilstedeværelse hos børn normalt bemærkes kort efter fødslen. Lejlighedsvis vil sygdommen gå ubemærket hen, indtil barnet er omkring 4 eller 5 år. En person kan også være bærer af sygdommen og ikke vise tegn eller symptomer på sygdommen. Andre symptomer kan omfatte mavesmerter, der kan føre til fjernelse af milten og/eller galdeblæren.
Præsentation
Komplikationer
- Hæmolytisk krise, med mere udtalt gulsot på grund af accelereret hæmolyse (kan udfældes ved infektion).
- Aplastisk krise med dramatisk fald i hæmoglobinniveau og (retikulocyttal) -kompensation, normalt på grund af modningsstop og ofte forbundet med megaloblastiske ændringer; kan udfældes ved infektion, såsom influenza, især med parvovirus B19 .
- Folatmangel forårsaget af øget krav til knoglemarv.
- Pigmenterede galdesten forekommer hos cirka halvdelen af ubehandlede patienter. Øget hæmolyse af røde blodlegemer fører til øgede bilirubinniveauer, fordi bilirubin er et nedbrydningsprodukt af hæm . De høje niveauer af bilirubin skal udskilles i galden af leveren, hvilket kan forårsage dannelsen af en pigmenteret galdesten, som består af calciumbilirubinat. Da disse sten indeholder høje niveauer af calciumcarbonater og fosfat, er de radioaktive og er synlige på røntgen.
- Bensår.
- Unormalt lave hæmoglobin A1C -niveauer. Hæmoglobin A1C (glyceret hæmoglobin) er en test til bestemmelse af de gennemsnitlige blodglukoseniveauer over en længere periode og bruges ofte til at evaluere glukosekontrol hos diabetikere. Hæmoglobin A1C-niveauerne er unormalt lave, fordi de røde blodlegemers levetid reduceres, hvilket giver mindre tid til den ikke-enzymatiske glykosylering af hæmoglobin. Selv med højt samlet blodsukker vil A1C således være lavere end forventet.
Patofysiologi
Arvelig spherocytose kan være et autosomalt recessivt eller autosomalt dominerende træk. Arvelig spherocytose findes oftest (dog ikke udelukkende) i nordeuropæiske og japanske familier, selvom anslået 25% af tilfældene skyldes spontane mutationer . En patient har en 50% chance for at overføre mutationen til hvert sit afkom.
Arvelig spherocytose er forårsaget af en række forskellige molekylære defekter i generne, der koder for de røde blodlegemers proteiner spectrin ( alfa og beta ), ankyrin , band 3 -protein, protein 4.2 og andre røde blodlegememembranproteiner:
| Type | OMIM | Gene | Locus |
|---|---|---|---|
| HS1 | 182900 | ANK1 | 8p11.2 |
| HS2 | 182870 | SPTB | 14q22-q23 |
| HS3 | 270970 | SPTA | 1q21 |
| HS4 | 612653 | SLC4A1 | 17q21-q22 |
| HS5 | 612690 | EPB42 | 15q15 |
Disse proteiner er nødvendige for at opretholde den normale form af en rød blodlegeme, som er en bikonkave skive. Det integrerende protein, der oftest er defekt, er spektrin, der er ansvarlig for inkorporering og binding af spektrin, og derfor følger cytoskeletale ustabilitet i sin dysfunktion.
Den primære defekt ved arvelig spherocytose er en mangel på membranoverflade. Nedsat overfladeareal kan frembringes ved to forskellige mekanismer: 1) Defekter i spectrin, ankyrin (oftest) eller protein 4.2 fører til reduceret densitet af membranskelettet, destabiliserer det overliggende lipid -dobbeltlag og frigiver bånd 3 -indeholdende mikrovesikler . 2) Defekter i bånd 3 fører til mangel på bånd 3 og tab af dets lipidstabiliserende effekt. Dette resulterer i tab af bånd 3-frie mikrovesikler. Begge veje resulterer i membrantab, nedsat overfladeareal og dannelse af sfærocytter med nedsat deformerbarhed.
Da milten normalt retter sig mod unormalt formede røde blodlegemer (som typisk er ældre), ødelægger det også sfærocytter. I milten kan passagen fra Billroths snore til sinusoiderne ses som en flaskehals, hvor røde blodlegemer skal være fleksible for at kunne passere igennem. Ved arvelig spherocytose passerer røde blodlegemer ikke igennem og bliver fagocytoseret, hvilket forårsager ekstravaskulær hæmolyse .
Diagnose
I en perifert blod smear , de røde blodlegemer vil blive vist unormalt lille og mangler den centrale blegt område, der er til stede i normale røde blodlegemer. Disse ændringer ses også i ikke-arvelig sfærocytose, men de er typisk mere udtalt i arvelig sfærocyte. Antallet af umodne røde blodlegemer ( retikulocyttal ) vil blive forhøjet. En stigning i den gennemsnitlige corpuskulære hæmoglobinkoncentration er også i overensstemmelse med arvelig spherocytose.
Andre proteinmangel forårsager arvelig elliptocytose , pyropoikilocytose eller stomatocytose .
I mangeårige tilfælde og hos patienter, der har taget jerntilskud eller modtaget mange blodtransfusioner , kan jernoverbelastning være et betydeligt problem. Dette er en potentiel årsag til hjertemuskleskader og leversygdom . Måling af jernlagre betragtes derfor som en del af den diagnostiske tilgang til arvelig sfærocytose.
En osmotisk skrøbelighedstest kan hjælpe med diagnosen. I denne test vil spherocytterne briste i flydende opløsninger, der er mindre koncentrerede end indersiden af de røde blodlegemer. Dette skyldes øget permeabilitet af sfærocytmembranen for salt og vand, som kommer ind i det koncentrerede indre miljø i RBC og fører til dets brud. Selvom den osmotiske skrøbelighedstest i vid udstrækning betragtes som guldstandarden for diagnosticering af arvelig spherocytose, savner den hele 25% af tilfældene. Flowcytometrisk analyse af eosin-5′-maleimid-mærkede intakte røde blodlegemer og den forsurede glycerollystest er to yderligere muligheder for at hjælpe diagnosen.
Behandling
Selvom forskningen er i gang, er der på dette tidspunkt ingen kur mod den genetiske defekt, der forårsager arvelig sfærocytose. Nuværende ledelse fokuserer på interventioner, der begrænser sygdommens sværhedsgrad. Behandlingsmuligheder omfatter:
- Splenektomi : Som ved ikke-arvelig spherocytose indikerer akutte symptomer på anæmi og hyperbilirubinæmi behandling med blodtransfusioner eller udvekslinger og kroniske symptomer på anæmi og en forstørret milt indikerer kosttilskud af folsyre og miltenektomi , kirurgisk fjernelse af milten. Splenektomi er indiceret til moderate til svære tilfælde, men ikke milde tilfælde. For at reducere risikoen for sepsis kræver post-splenektomi sfærocytose patienter immunisering mod influenzavirus , indkapslede bakterier som Streptococcus pneumoniae og meningococcus og profylaktisk antibiotikabehandling. Imidlertid er brugen af profylaktiske antibiotika, såsom penicillin, stadig kontroversiel.
- Delvis splenektomi : Da milten er vigtig for at beskytte mod indkapslede organismer, er sepsis forårsaget af indkapslede organismer en mulig komplikation af splenektomi. Muligheden for delvis splenektomi kan overvejes for at bevare immunfunktionen. Forskning om resultater er i øjeblikket begrænset, men gunstig.
- Kirurgisk fjernelse af galdeblæren kan være nødvendig.
Epidemiologi
Arvelig spherocytose er den mest almindelige lidelse i de røde cellemembraner og rammer 1 ud af 2.000 mennesker af nordeuropæisk herkomst. Ifølge Harrisons principper for intern medicin er frekvensen mindst 1 ud af 5.000.
Forskning
Eksperimentel genterapi eksisterer til behandling af arvelig spherocytose i laboratoriemus; denne behandling er imidlertid endnu ikke blevet forsøgt på mennesker på grund af alle de risici, der er forbundet med human genterapi.
Se også
Referencer
eksterne links
| Klassifikation | |
|---|---|
| Eksterne ressourcer |
