ALOX12 - ALOX12
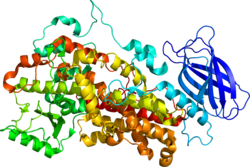
ALOX12 ( EF 1.13.11.31 ), også kendt som arachidonat 12-lipoxygenase , 12-lipoxygenase , 12 S -Lipoxygenase , 12-LOX , og 12 S LOX er en lipoxygenase -type enzym at i mennesker kodes af ALOX12 gen som er placeret sammen med andre lipoyxgenaser på kromosom 17p13.3. ALOX12 er 75 kilodalton protein sammensat af 663 aminosyrer.
Nomenklatur
| arachidonat 12-lipoxygenase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identifikatorer | |||||||||
| EF -nr. | 1.13.11.31 | ||||||||
| CAS -nr. | 82391-43-3 | ||||||||
| Databaser | |||||||||
| IntEnz | IntEnz -visning | ||||||||
| BRENDA | BRENDA indgang | ||||||||
| ExPASy | NiceZyme udsigt | ||||||||
| KEGG | KEGG -indtastning | ||||||||
| MetaCyc | metabolisk vej | ||||||||
| PRIAM | profil | ||||||||
| PDB -strukturer | RCSB PDB PDBe PDBsum | ||||||||
| Genontologi | AmiGO / QuickGO | ||||||||
| |||||||||
Andre systematiske navne for ALOX12 omfatter 12S-Lipoxygenase, trombocytype 12-lipoxygenase, arachidonat: oxygen 12-oxidoreduktase, Delta12-lipoxygenase, 12Delta-lipoxygenase og C-12 lipoxygenase. ALOX12, ofte betegnet pladepladetype 12-lipoxygenase, adskiller sig fra leukocyt-type 12-lipoxygenase, som findes hos mus, rotter, køer og svin, men ikke mennesker. Leukocyt-type 12-lipoxygenase i disse dyrearter deler 73-86% aminosyreidentitet med human ALOX15, men kun 57-66% identitet med human trombocytype 12-lipoxygenase og metaboliserer, ligesom ALOX15, primært arachidonsyre til 15 ( S ) -hydroperoxy-5 Z , 8 Z , 11 Z , 13 E- eicosatetraensyre (dvs. 15 ( S ) -HpETE; se 15-Hydroxyeicosatetraensyre ). Følgelig betragtes gnaverleukocyt 12-lipoxygenase som en ortolog af ALOX15 og betegnes som Alox15 .
Human ALOX12 og ALOX15 sammen med gnaver-leukocyt-type Alox12 og Alox15 betegnes almindeligvis 12/15-lipoxygenaser baseret på deres evne til at metabolisere arachidonsyre til både 12 ( S ) -HpETE og 15 ( S ) -HpETE og til at udføre det samme stofskifte på arachidonsyre, som er esterificeret til membran phospholipider ; human ALOX15B laver 15 ( S ) -HpETE men ikke 12 ( S ) -HpETE og betragtes derfor ikke som en 12/15-lipoxygenase. Undersøgelser af ALOX12's rolle i patofysiologien ved hjælp af hovedmodellerne for sådanne funktionelle undersøgelser, rotter og mus, er komplicerede, fordi ingen af arterne besidder en lipoxygenase, der har en overvægt på 12 ( S ) -HETE og derfor er metabolisk ækvivalent med ALOX12. For eksempel kan de funktioner, der udledes for Alox12 hos mus, der er mangelfulde i Alox12 ved hjælp af knockout -metoder, muligvis ikke indikere en lignende funktion for ALOX12 hos mennesker på grund af forskelle i disse to enzymers metaboliske aktiviteter. ALOX12's funktion er yderligere uklar af human ALOX15, der metaboliserer arachidonsyre primært til 15 ( S ) -HpETE, men også gør mindre, men stadig betydelige mængder af 12 ( S ) -HpETE (se ALOX15 ).
ALOX12 adskiller sig også fra arachidonat 12-lipoxygenase, 12R type (ALOX12B), som metaboliserer arachidonsyre til R- stereoisomeren af 12 ( S ) -HpETE, dvs. 12 ( R ) -hydroperoxy-5 Z , 8 Z , 10 E , 14 Z -icosatetraensyre (12 ( R ) -HpETE), et produkt med meget forskellige patofysiologiske roller end 12 ( S ) -HpETE (se ALOX12B ).
Opdagelse
ALOX12, oprindeligt kaldet arachidonat 12-lipoxygenase, blev først karakteriseret af Nobelpristageren, Bengt I. Samuelsson , og hans berømte kollega, Mats Hamberg, i 1974 ved at vise, at menneskelige blodplader metaboliserer arachidonsyre, ikke kun af den velkendte cyclooxygenase- vej til prostaglandiner og 12-hydroxyheptadecatrienonsyre, men også via en cyclooxygenase-uafhængig vej til 12 ( S ) -hydroperoxy-5,8,10,14-eicosatetraensyre; denne aktivitet var den første mammale lipoxygenaseaktivitet, der blev karakteriseret. I 1975 blev den første biologiske aktivitet knyttet til denne metabolit i undersøgelser, der viste, at den simulerede kemotaxi fra humane neutrofiler . I løbet af de flere år derefter blev human ALOX12 renset, karakteriseret biokemisk og fået sit gen molekylært klonet .
Vævsfordeling
Baseret overvejende på tilstedeværelsen af dets mRNA , distribueres human ALOX12 overvejende i blodplader og leukocytter og på lavere niveauer i epidermis basallag (især i hudlæsioner af psoriasis ), øer af Langerhans i bugspytkirtlen og visse kræftformer .
Enzymaktiviteter
Styringen af ALOX12 aktivitet synes at hvile hovedsagelig af tilgængeligheden af dets polyumættet fedtsyre (PUFA) substrater, som frigives fra lagrene membran phospholipider ved cellestimulering. Enzymet deltager i arachidonsyremetabolisme ved at udføre den følgende kemiske reaktion, hvor dets substrater er arachidonsyre (også betegnet som arachidonat eller kemisk som 5 Z , 8 Z , 11 Z , 14 Z -eicosatetraensyre) og O 2 (dvs. oxygen ) og dets produkt er 12 S -hydroperoxy -5 Z , 8 Z , 10 E , 14 Z -eicosatetraensyre (dvs. 12 S -hydroperoxyeicosatetraensyre eller 12 S -HpETE):
- arachidonat + O 2 → 12 S -hydroperoxy -5 Z , 8 Z , 10 E , 14 Z -eicosatetraensyre
I celler kan 12 S HpETE yderligere metaboliseres af ALOX12 selv, af ALOXE3 eller muligvis andre, endnu ikke fuldstændigt identificerede, hepoxilinsyntaser til hepoxilin A3 (8 R/S -hydroxy-11,12-oxido-5 Z , 9 E , 14 Z -eicosatrienonsyre) og B3 (10 R/S -hydroxy -11,12 -oxido -5 Z , 8 Z , 14 Z -eicosatrienonsyre):
- 12 S -hydroperoxy-5Z, 8Z, 10E, 14Z-eicosatetraensyre → 8 R/S -hydroxy-11,12-oxido-5 Z , 9 E , 14 Z- eicosatrieninsyre + 10 R/S -hydroxy-11, 12-oxido-5 Z , 8 Z , 14 Z- eicosatrienonsyre
Hepoxiliner kan fremme visse betændelsesreaktioner , øge smerteopfattelsen (dvs. taktil allodyni ), regulere regional blodgennemstrømning og bidrage til regulering af blodtryk i dyremodeller (se Hepoxilins ). Langt mere almindeligt reduceres imidlertid 12 S -HpETE hurtigt til sit hydroxylprodukt ved allestedsnærværende cellulære peroxidaseaktiviteter, hvorved der dannes 12 S -hydroxy -5 Z , 8 Z , 10 E , 14 Z -eicosatetraensyre, dvs. 12 -hydroxyeicosatetraensyre eller 12 S -HETE:
- 12 S -hydroperoxy-5 ( Z ), 8 ( Z ), 10 ( E ), 14 ( Z ) -eicosatetraensyre → 12 S -hydroxy-5 ( Z ), 8 ( Z ), 10 ( E ), 14 ( Z ) -eicosatetraensyre
12 S -HETE fremmer inflammatoriske reaktioner, kan være involveret i opfattelsen af puritis (dvs. kløe) i huden og regulerer regional blodgennemstrømning i dyremodeller; det fremmer også ondartet adfærd hos dyrkede humane kræftceller samt vækst af visse kræftformer i dyremodeller (se 12-HETE ). Mens arachidonat og 12 ( S ) -HETE er henholdsvis de dominerende substrater og produkter af ALOX12, metaboliserer enzymet også anden PUFA. Det metaboliserer omega-3 fedtsyren , docosahexaensyre (DHA dvs. 4 ( Z ), 7 ( Z ), 10 ( Z ), 13 ( Z ), 16 ( Z ), 19 ( Z ) -docosahexaensyre til 14 ( R ) -hydroperoxy-4 ( Z ), 8 ( Z ), 10 ( Z ), 12 ( E ), 16 ( Z ), 19 ( Z ) -docosahexaensyre) (dvs. 17-hydroperoxy-DHA); derefter kan ALOX12 eller et uidentificeret enzym af epoxidase-typen metabolisere dette mellemprodukt til et epoxid, 13,14-epoxy-4 ( Z ), 7 ( Z ), 9 ( E ), 11 ( E ), 16 ( Z ), 19 ( Z ) -docosahexaensyre (dvs. 13,14-e-maresin), der metaboliseres til 7 R , 14 S- dihydroxy-4 Z , 8 E , 10 E , 12 Z , 16 Z , 19 Z -docosahexaensyre (dvs. Maresin 1), af et uidentificeret enzym af epoxidhydrolase -type:
- DHA → 17-hydroperoxy-DHA → 13,14-e-maresin → Maresin-1
Maresin 1 har et sæt aktiviteter, der kan modsætte sig aktiviteterne for 12 ( S ) -HETE og hepoxilinerne; det er medlem af en klasse af PUFA-metabolitter kaldet Specialized pro-resolution mediators (SPM'er), der besidder antiinflammatoriske, smertelindrende og andre defensive aktiviteter. ALOX12 virker også på leukotrien A4 (LTA4) i en tocellelig reaktion kaldet transcellulær metabolisme: humane neutrofiler metaboliserer arachidonsyre til dets 5,6-epoxid, LTA4, og frigiver dette mellemprodukt til nærliggende neutrofiler, der metaboliserer det til lipoxin A4 (5 S , 6 R , 15 S -trihydroxy -7 E , 9 E , 11 Z , 13 Z -eicosatetraensyre) og lipoxin B4 (5 S , 14 R , 15 S -trihydroxy -6 E , 8 Z , 10 E , 12 E - eicosatetraensyre); begge lipoxiner er SPM'er med mange SPM-lignende aktiviteter (se lipoxin ). ALOX12 kan også metabolisere mindre mængder DHA til sekundære produkter, herunder 17-hydroperoxy-DHA, 11-hydroperoxy-DHA og 8,14-dihydroxy-DHA ALOX12 kan ligeledes metabolisere 5 ( S ) -HETE til 5 S , 12 S -dihydroxyeicosatetraenoic syre (12,15 -diHETE) og 15 S -HETE til 14,15 S -diETE. Selvom disse forbindelser ikke er blevet grundigt evalueret for bioaktivitet, har 17-hydroperoxy-HDHA og det reducerede produkt, som det hurtigt omdannes til i celler, 17-hydroxy-HDHA, vist sig at hæmme væksten af dyrkede humane prostatacancerceller ved at forårsage dem til at komme ind i apoptose .
Dyreforsøg
Undersøgelser om gnavere, der mangler eller er mangelfulde i leukocyt-type 12-lipoxygenase, Alox12 (som er nært beslægtet med human ALOX15) implicerer dette enzym i: a) at forhindre udvikling og komplikationer af diætinduceret og/eller genetisk induceret diabetes , fedtcelle /vævsdysfunktion og fedme; b) udviklingen af åreforkalkning og Steatohepatitis ; b) regulering af blodkarkontraktion, dilatation, tryk, ombygning og angiogenese ; c) opretholdelse af normal nyre-, neurologisk og hjernefunktion; og d) udviklingen af Alzheimers sygdom . I disse undersøgelser er det sædvanligvis uklart, om der var en eller flere metabolitter af Alox12 involveret.
Prækliniske undersøgelser
Metabolisk syndrom
Det metaboliske syndrom er en klynge af mindst tre af fem af følgende medicinske tilstande: abdominal (central) fedme , forhøjet blodtryk , forhøjet fastende plasmaglukose (eller åbenlys diabetes ), høje serumtriglycerider og lavdensitetslipoprotein (HDL ) niveauer. ALOX12 og dets metabolit, 12 ( S ) -HETE, er forhøjede i Langerhans-øerne hos patienter med type 1-diabetes eller type 2-diabetes samt i fedtcellerne i hvidt fedtvæv hos sygeligt fede type 2-diabetespatienter. De PP-celler (dvs. gamma celler) i bugspytkirtlen øer synes at være den største hvis ikke kun sted, hvor ALOX12 udtrykkes i disse patienter. Undersøgelserne foreslår, at ALOX12 på øerne i Langerhans og dets 12 ( S ) -HETE -produkt forårsager overdreven produktion af reaktive iltarter og betændelse, som fører til tab i insulin -udskillende betaceller og derved type 1 og 2 diabetes og det i fedtvæv overskuddet i AlOX12, 12 ( S ) -HETE, reaktive iltarter og betændelse fører til dysfunktion i fedtceller (se også 12-HETE#Inflammation og inflammatoriske sygdomme og 12-HETE#Diabetes ). Faktisk i en undersøgelse en enkeltnukleotidpolymorfi , rs2073438, placeret i en intron region af ALOX12 genet blev signifikant associeret med total og procentdel fedtmassen i overvægtige sammenlignet med ikke-overvægtige unge kinesiske mænd. ALOX12 og 12 ( S ) -HETE er ligeledes impliceret i essentiel hypertension (se næste afsnit). Derfor kan ALOX12 og dets metabolit (er) bidrage til udvikling og/eller progression af fedme, diabetes, hypertension og/eller det metaboliske syndrom.
Blodårer
En selektiv, men ikke helt specifik hæmmer af ALOX12 reducerede vækstrespons af dyrkede humane endotelceller til basisk fibroblastvækstfaktor og vaskulær endotelvækstfaktor (VEGF); denne reduktion blev delvist reverseret med 12 ( S ) -HETE; 12 ( S ) -HETE stimulerer også humane prostatacellelinjer til at producere VEGF. Disse resultater tyder på, at vækstresponser på de to vækstfaktorer involverer deres stimulering af 12 ( S ) -HETE-produktion af endotelceller og derfor, at ALOX12 kan være et mål for at reducere den neo-vaskularisering, der fremmer leddgigt og kræftsygdomme. 12 ( S ) -HETE udvider også humane koronar mikrocirkulationsarterier ved at aktivere disse fartøjers glatte muskler BKca Kaliumkanaler og foreslås derfor at være en endothel-afledt hyperpolariserende faktor . Endelig har en enkelt nukleotidvariant i ALOX12- genet (R261Q [3957 G> A]) været forbundet med essentiel hypertension og forhøjelse i urinudskillelsen af 12 ( S ) -HETE hos mennesker og kan være en medvirkende årsag til essentiel hypertension (se også 12-HETE#Blodtryk ).
Alzheimers sygdom
Patienter med Alzheimers sygdom eller andre former for demens har signifikant højere niveauer på 12 ( S ) -HETE (og 15 ( S ) -HETE) i cerebrospinalvæske sammenlignet med ældre matchede normale individer. Komplementære undersøgelser af gnavermodeller, der bærer humane muterede gener for Amyloid-prækursorprotein og/eller tauprotein (se tauprotein#Klinisk betydning ), der producerer Alzheimers demenslignende syndromer implicerer 12 ( S ) -HETE, 15 ( S ) -HETE og en 12/15-lipoxygenase type enzym i udviklingen og progressionen af Alzhiemers sygdomslignende symptomer og fund hos disse dyr. I en enkelt undersøgelse blev ALOX12 mRNA fundet forhøjet i hjernevævet hos patienter med Alzheimers sygdom sammenlignet med kontrolpatienter. Disse resultater tyder på, at ALOX12 (eller ALOX15) kan bidrage til udviklingen af Alzheimers sygdom hos mennesker.
Kræft
Undersøgelser af prostatakræft viser, at humane prostatacancer cellelinjer i kulturen overudtrykker ALOX12, overproducerer 12 ( S ) -HETE og reagerer på 12 ( S ) -HETE ved at øge deres proliferationshastighed, øge deres celleoverfladeekspression af integriner , øge deres overlevelse og forsinkelse af deres apoptose og forøgelse af deres produktion af vaskulær endotelvækstfaktor og MMP9 (dvs. Matrix metallopeptidase 9); selektive (men ikke helt) specifikke ALOX12-hæmmere reducerede proliferationen og overlevelsen af disse celler (se også 12-HETE#prostatakræft ). Disse fund tyder på, at ALOX12 og dets 12 ( S ) -HETE-produkt kan bidrage til vækst og spredning af prostatakræft hos mennesker. For nylig blev hypermetylering af ALOX12 -genet i prostatacancervæv forbundet med kliniske forudsigelser for en høj grad af tilbagevendende sygdom. Nogle undersøgelser har fundet ud af, at 12 ( S ) -HETE også fremmer vækst og/eller relateret pro-malign adfærd af forskellige andre typer dyrkede kræftcellelinjer (se 12-HETE#Andre kræftformer ). ALOX12 har vist sig at interagere med Keratin 5 og LMNA som screenet i et gær-to-hybrid interaktionsbibliotek fra humane epidermoid carcinom A431 celler ; disse proteiner er kandidater til regulering af 12-LOX, især i tumorceller.
Trombocytfunktion
Selvom ALOX12 og dens vigtigste metabolitter først blev identificeret i humane blodplader, er 12 ( S ) -HpETE og 12 ( S ) -HETE i trombocytfunktionen stadig kontroversiel og uklar; det er muligt, at ALOX12-12 ( S ) -HETE metaboliske vej har to funktioner til at fremme eller hæmme trombocytresponser afhængigt af det stimulerede middel og den undersøgte respons, men at inhibering af ALOX12 i sidste ende kan vise sig nyttig til at hæmme blodpladerelateret blodpropper.
Andre foreninger
Den ALOX12 genet har prædisponeringsalleler (rs6502997, rs312462, rs6502998, og rs434473) til parasitisk sygdom , human medfødt toxoplasmose . Fosterbærer af disse alleler lider således af en øget modtagelighed for denne sygdom.
Referencer
eksterne links
- Human ALOX12 genom placering og ALOX12 gen detaljer side i UCSC Genome Browser .
Yderligere læsning
- Yoshimoto T, Arakawa T, Hada T, Yamamoto S, Takahashi E (december 1992). "Struktur og kromosomal lokalisering af humant arachidonat 12-lipoxygenase-gen" . Journal of Biological Chemistry . 267 (34): 24805–9. doi : 10.1016/S0021-9258 (18) 35835-6 . PMID 1447217 .
- Izumi T, Hoshiko S, Rådmark O, Samuelsson B (oktober 1990). "Kloning af cDNA for human 12-lipoxygenase" . Procedurer ved National Academy of Sciences i Amerikas Forenede Stater . 87 (19): 7477–81. Bibcode : 1990PNAS ... 87.7477I . doi : 10.1073/pnas.87.19.7477 . PMC 54770 . PMID 2217179 .
- Funk CD, Furci L, FitzGerald GA (august 1990). "Molekylær kloning, primær struktur og ekspression af den humane trombocyt/erythroleukæmicelle 12-lipoxygenase" . Procedurer ved National Academy of Sciences i Amerikas Forenede Stater . 87 (15): 5638–42. Bibcode : 1990PNAS ... 87.5638F . doi : 10.1073/pnas.87.15.5638 . PMC 54382 . PMID 2377602 .
- Flatman S, Morgan A, McDonald-Gibson RG, Davey A, Jonas GE, Slater TF (maj 1988). "12-Lipoxygenase-aktivitet i human livmoderhals". Prostaglandiner, leukotriener og essentielle fedtsyrer . 32 (2): 87–94. doi : 10.1016/0952-3278 (88) 90101-9 . PMID 3406043 .
- Wong PY, Westlund P, Hamberg M, Granström E, Chao PH, Samuelsson B (august 1985). "15-Lipoxygenase i humane blodplader" . Journal of Biological Chemistry . 260 (16): 9162–5. doi : 10.1016/S0021-9258 (17) 39346-8 . PMID 3926763 .
- Nakamura M, Ueda N, Kishimoto K, Yoshimoto T, Yamamoto S, Ishimura K (marts 1995). "Immunocytokemisk lokalisering af trombocytype arachidonat 12-lipoxygenase i musens blodlegemer" . Journal of Histochemistry and Cytochemistry . 43 (3): 237–44. doi : 10.1177/43.3.7868854 . PMID 7868854 .
- Hussain H, Shornick LP, Shannon VR, Wilson JD, Funk CD, Pentland AP, Holtzman MJ (januar 1994). "Epidermis indeholder trombocytype 12-lipoxygenase, der er overudtrykt i keratinocytter i germinal lag ved psoriasis". American Journal of Physiology . 266 (1 punkt 1): C243-53. doi : 10.1152/ajpcell.1994.266.1.C243 . PMID 8304420 .
- Arora JK, Lysz TW, Zelenka PS (juni 1996). "En rolle for 12 (S) -HETE i responsen fra humane linseepitelceller på epidermal vækstfaktor og insulin". Undersøgende oftalmologi og visuel videnskab . 37 (7): 1411–8. PMID 8641843 .
- Hagmann W, Gao X, Timar J, Chen YQ, Strohmaier AR, Fahrenkopf C, Kagawa D, Lee M, Zacharek A, Honn KV (november 1996). "12-Lipoxygenase i A431-celler: genetisk identitet, modulering af ekspression og intracellulær lokalisering". Eksperimentel celleforskning . 228 (2): 197–205. doi : 10.1006/excr.1996.0317 . PMID 8912711 .
- Nakamura M, Yamamoto S, Ishimura K (maj 1997). "Subcellulær lokalisering af arachidonat 12-lipoxygenase og morfologisk virkning af dens overekspression på murine keratinocytter". Celle- og vævsforskning . 288 (2): 327–34. doi : 10.1007/s004410050818 . PMID 9082968 . S2CID 23548308 .
- Nigam S, Kumar GS, Sutherland M, Schewe T, Ikawa H, Yamasaki Y, Ueda N, Yamamoto S (september 1999). "Metabolsk undertrykkelse af trombocytype 12-lipoxygenase i human livmoderhals med invasivt carcinom". International Journal of Cancer . 82 (6): 827–31. doi : 10.1002/(SICI) 1097-0215 (19990909) 82: 6 <827 :: AID-IJC10> 3.0.CO; 2-Q . PMID 10446449 .
- Tornhamre S, Elmqvist A, Lindgren JA (april 2000). "15-Lipoxygenering af leukotrien A 4 : Undersøgelser af 12- og 15-lipoxygenaseffektivitet til at katalysere lipoxindannelse". Biochimica et Biophysica Acta (BBA) - Molekylær og cellebiologi af lipider . 1484 (2–3): 298–306. doi : 10.1016/S1388-1981 (00) 00017-2 . PMID 10760478 .
- Chen BK, Tsai TY, Huang HS, Chen LC, Chang WC, Tsai SB, Chang WC (2003). "Funktionel rolle for ekstracellulær signalreguleret kinaseaktivering og c-Jun-induktion i phorbolester-induceret promotoraktivering af humant 12 (S) -lipoxygenasegen". Journal of Biomedical Science . 9 (2): 156–65. doi : 10.1159/000048212 . PMID 11914583 . S2CID 46753449 .
- Winer I, Normolle DP, Shureiqi I, Sondak VK, Johnson T, Su L, Brenner DE (oktober 2002). "Ekspression af 12-lipoxygenase som en biomarkør for melanomkarcinogenese". Melanomforskning . 12 (5): 429–34. doi : 10.1097/00008390-200209000-00003 . PMID 12394183 . S2CID 27336312 .
- Gu J, Wen Y, Mison A, Nadler JL (februar 2003). "12-lipoxygenasebane øger aldosteronproduktion, 3 ', 5'-cyklisk adenosinmonophosphatresponselement-bindende proteinphosphorylering og p38 mitogenaktiveret proteinkinaseaktivering i H295R humane adrenokortikale celler" . Endokrinologi . 144 (2): 534–43. doi : 10.1210/en.2002-220580 . PMID 12538614 .
- Fridman C, Ojopi EP, Gregório SP, Ikenaga EH, Moreno DH, Demetrio FN, Guimarães PE, Vallada HP, Gattaz WF, Dias Neto E (februar 2003). "Forening af en ny polymorfisme i ALOX12 -genet med bipolar lidelse". European Archives of Psychiatry and Clinical Neuroscience . 253 (1): 40–3. doi : 10.1007/s00406-003-0404-y . PMID 12664313 . S2CID 21064663 .