P -type calciumkanal - P-type calcium channel
Den P-type calciumkanal er en type spændingsafhængig calciumkanal . I lighed med mange andre højspændingsgatede calciumkanaler bestemmer α1-underenheden de fleste af kanalens egenskaber. 'P'et betegner cerebellare Purkinje -celler med henvisning til kanalens indledende fundsted. P-type calciumkanaler spiller en lignende rolle som calciumkanalen af N-typen i neurotransmitterfrigivelse ved den presynaptiske terminal og i neuronal integration i mange neuronale typer.
Historie
Calciumkanalforsøgene, der førte til opdagelsen af calciumkanaler af P-typen, blev oprindeligt afsluttet af Llinás og Sugimori i 1980. Calciumkanaler af P-typen blev navngivet i 1989, fordi de blev opdaget i purkinje-neuroner hos pattedyr . De var i stand til at bruge et in vitro -præparat til at undersøge de ioniske strømme, der tegner sig for Purkinje -cellers elektrofysiologiske egenskaber . De fandt ud af, at der er calciumafhængige aktionspotentialer, der stiger langsomt og falder hurtigt og derefter gennemgår hyperpolarisering . Handlingspotentialerne var spændingsafhængige, og de efterhyperpolariserende potentialer blev forbundet til piggenes bursts, der var placeret inden for dendritterne i Purkinje -cellerne. Uden calciumstrømning i Purkinje -cellerne affyres aktionspotentialer sporadisk ved en høj frekvens.
Grundlæggende funktioner og struktur
| calciumkanal, spændingsafhængig, P/Q-type, alfa 1A-underenhed | |||||||
|---|---|---|---|---|---|---|---|
| Identifikatorer | |||||||
| Symbol | CACNA1A | ||||||
| Alt. symboler | Cav2.1 , CACNL1A4, SCA6, MHP1, MHP | ||||||
| IUPHAR | 532 | ||||||
| NCBI -gen | 773 | ||||||
| HGNC | 1388 | ||||||
| OMIM | 601011 | ||||||
| RefSeq | NM_000068 | ||||||
| UniProt | O00555 | ||||||
| Andre data | |||||||
| Locus | Chr. 19 s13 | ||||||
| |||||||
P-type calciumkanaler er spændingsafhængige calciumkanaler, der er klassificeret under højspændingsaktiveret klasse kanal sammen med L-, N-, Q- og R-type kanaler. Disse kanaler kræver en stærk depolarisering for at blive aktiveret. De findes på axonterminaler såvel som i somatodendritiske områder af neuroner i central- og perifert nervesystem. P-type calciumkanaler er også kritiske for vesikelfrigivelse , specifikt neurotransmittere og hormoner ved synaptiske terminaler af excitatoriske og hæmmende synapser.
Spændingsstyrede calciumkanaler af P-type består af en hovedporedannende α1-underenhed (som mere specifikt omtales som CaV2.1 ), en α2-underenhed og en β-underenhed. Der kan findes γ -underenheder i calciumkanaler i skeletmusklerne. Α1 - underenheden er specifikt kodet af CACNA1A- genet og består af fire domæner, der hver indeholder seks transmembran (S1-S6), der spænder over α-spiraler. S1-S2-sløjfen og S6- regionen menes at være ansvarlige for kanalens inaktivering, S4-regionen fungerer som spændingssensor og S5-S6-sløjfe danner poren. Der er syv underenheder inden for α1 -underenheden. A-underenheden, kaldet α1ACa2+, svarer til det, der funktionelt defineres som P-type og Q-type isoformer. P-type og Q-type calciumkanaler er nært beslægtede, da de produceres fra det samme gen via alternativ splejsning. Som en komplikation af den alternative splejsning kan kanaler af P-type og Q-type have forskellige underenhedssammensætninger. Β -underenheden regulerer kinetikken og ekspressionen af kanalen sammen med α2δ -underenheden.
Kanaldistribution
Størstedelen af P-type calciumkanaler er placeret i nervesystemet og hjertet. Antistofmærkning er den primære metode, der bruges til at identificere kanalplacering.
Områder med højt udtryk i pattedyrssystemer omfatter:
- Purkinjecelle dendritter
- Glat endoplasmatisk retikulum
- Plasmamembran soma (cellelegemet)
- Periglomerulære celler i olfaktorisk pære
- Cerebellar cortex
- Neuroner i hjernestammen , entorhinal og pyriform cortices og habenula .
Kanalblokkere
P-type calciumkanalblokkere virker til at hæmme calciumstrømmen. Blokering af calciumstrømme kan få organismen til at opleve nedsat funktion og levedygtighed. Disse virkninger kan føre til forskellige sygdomme, som er beskrevet mere detaljeret i afsnittet nedenfor.
Den pore af P-type calciumkanaler er følsomme over for forbindelser, der kan opdeles i tre grupper:
- Peptid- ionkanalblokkere
- Lavmolekylære forbindelser
- Terapeutisk
Der er kun to peptid toksiner , der selektivt blokerer P-type kanaler: ω- agatoksin IVA og ω-agatoksin IVB. De andre nævnte blokkere, såsom den lave molekylvægt og terapeutiske blokkere, er ikke -selektive. Dette betyder, at de kan handle både på kanaler af P-type og på andre kanaler.
Selektivt peptidtoksin ω-agatoxin
De to kendte blokkere, der er specifikke for P-type calciumkanaler, er peptider, der stammer fra edderkoppegiften fra Agelenopsis aperta . De toksiner fra dette gift, der viser selektivitet for P-type kanaler, er ω-agatoxin IVA og ω-agatoxin IVB. Hver af disse peptidtoksiner er fremstillet af 48 aminosyrer, som er bundet af fire disulfidbindinger . Selvom ω-agatoxin IVA og ω-agatoxin IVB har samme affinitet og selektivitet for P-type kanaler, er deres kinetik forskellig. Ω-agatoxin IVA påvirker portmekanismen for P-type kanal. Når der er en stærk depolarisering for at aktivere kanalen, kan ω-agatoxin IVA ikke længere blokere kanalen. Derfor har ω-agatoxin IVA en meget lav affinitet for kanalen, når den er åben. Det binder sig til α 1A -underenheden på ydersiden af poren. Ω-agatoxin IVA- receptoren på P-type-kanalen er placeret ved S3-S4-linkeren. På den anden side sker kanalblokering med ω-agatoxin IVB meget langsommere. Alligevel ligner ω-agatoxin IVA, kan ω-agatoxin IVB ikke binde sig til kanalen ved en stærk depolarisering.
Ikke-selektive peptid toksiner
- ω-Grammotoxin SIA er et peptidtoksin afledt af edderkoppen Grammostola spatulata . Det virker til at ændre P-type kanal gating .
- ω-PnTx3-3, PnTx3-3 og phonetoxin IIA er alle toksiner fra edderkoppen Phonoetrica nigriventer, der virker for at blokere strømmen gennem P-type calciumkanaler.
- DW13.3 er et peptidtoksin fra edderkoppen Filistata hibernalis og består af 74 aminosyrer. Det fungerer også for at blokere strømmen gennem P-type calciumkanaler.
- ω- Konotoksiner stammer fra keglesneglens gift . ω-Conotoxin MVIIC virker inden for de hippocampus CA1 pyramidale neuroner for at blokere kanalerne af P-typen. Også inden for hippocampus CA3 -neuroner blokerer dette toksin synaptisk transmission . Dens virkninger er langsomme.
- Calcicludine er fra gift fra Dendroaspis angusticeps , som er en grøn mamba . Det har evnen til at spændingsafhængigt blokere P-type kanaler.
- Kurotoksin er fra gift fra skorpionen Parabuthus . I neuroner i thalamus reducerer kurtoxin calciumstrømme med høj tærskel , men i Purkinje -cellerne øger det calciumstrømmene.
Lavmolekylær kanalblokkere af P-type
Kanalblokkere med lav molekylvægt har fordele i forhold til peptidblokkere i lægemiddeludvikling. En fordel ved lavmolekylære kanalblokkere er, at de kan trænge ind i væv , hvilket er vigtigt for at krydse blod-hjerne-barrieren . Der er ingen specifik lavmolekylær kanalblokker til kanaler af P-type. Der er imidlertid en række af disse blokeringsforbindelser, som kan påvirke aktiviteten af P-type kanalerne. Disse omfatter:
- Roscovitine er en hæmmer af cyclinafhængig kinase . Det øger calciumstrømmen i neostriatale interneuroner ved at bremse deaktiveringen af kanalen. Roscovitin kan også enten fungere som en agonist eller antagonist for calciumkanalerne af P-typen i den presynaptiske membran.
- Isoprenalin er en β-adrenoceptoragonist, og det forårsager en stigning i P-type calciumkanalstrøm. Isoprenalin virker gennem en cAMP -signalvej .
- Eliprodil og antazolin er NMDA-receptorantagonister og virker til at blokere P-type kanaler. Eliprodil kan reducere kanalstrømme af P-typen i Purkinje-neuronerne i lillehjernen .
- Dodecylamin kan kun blokere P-kanaler, når de er i åben tilstand.
- Ethanol kan blokere P-type kanaler, når den er i en høj nok koncentration. Blokering af kanalerne af P-typen kan være årsagen til ataksi, når man drikker alkohol .
Terapeutisk
Der er klinisk anvendte terapeutiske midler, som kan påvirke aktiviteten af calciumkanaler af P-type. Imidlertid menes det primære mål for disse terapier ikke at være kanaler af P-type. For eksempel virker calciumantagonister , der bruges til behandling af koronar hjertesygdom , hypertension og hjertearytmi , ved at hæmme calciumkanaler af L-type eller T-type . Nogle af disse calciumantagonister inkluderer verapamil , diltiazem , amlodipin , benidipin , cilnidipin , nicardipin og barnidipin . Selvom deres hovedmål ikke er P-type kanaler, virker disse calciumantagonister også til at blokere funktionen af P-type kanaler. Desuden er flunarizin en anden calciumantagonist, der bruges til behandling af migræne . Dets hovedmål er spændingsgatede calciumkanaler og natriumkanaler . Flunarizin hæmmer kanalerne af P-typen, der er placeret i de neokortikale skiver . Det virker for at hæmme den indadgående strøm af calcium. Migrænen, som det hjælper med at forhindre, skyldes mutationer inden for "cacna1a" -genet i P-type kanalunderenheden. Også forbindelser, der blokerer P-type kanaler, viser sig at hjælpe med anfald . Epileptiske anfald skyldes øget neurotransmission , som delvist er et resultat af P-type kanaler. Forbindelser som levetiracetam , lamotrigin og carbamazepin vides at blokere kanalerne af P-typen, hvilket har bidraget til at reducere forekomsten af anfald. Samlet set er der forskellige ikke-selektive calciumkanalblokkere, der hjælper med at lindre symptomer på hypertension , skizofreni , hjertearytmi , epilepsi , smerter , astma , bradykardi , angina pectoris og Alzheimers sygdom . Selvom mange af de terapeutiske forbindelsers hovedmål ikke er kanaler af P-typen, skal yderligere forskning afgøre, om de kliniske virkninger af disse forbindelser også påvirkes af P-type kanalblokering.
Relaterede sygdomme
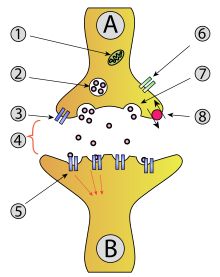
Der er en række neurologiske sygdomme, der er blevet tilskrevet funktionsfejl eller muterede P/Q -type kanaler.
Alzheimers sygdom
Ved Alzheimers sygdom er der en progressiv akkumulering af β-amyloidprotein (Aβ) i hjernen. Amyloide plaques udvikler sig, hvilket resulterer i de vigtigste symptomer på Alzheimers sygdom. Aβ globulomer protein er et kunstigt stof, der bruges i forskningsforsøg, der har lignende egenskaber som Aβ oligomer, som er til stede i kroppen. Aβ -oligomer regulerer direkte calciumkanaler af P/Q -typen. Α1A -underenheden er ansvarlig for ledningen af calciumstrøm. Når kun calciumkanaler af P/Q -type er til stede med Aβ -globulomerprotein, er der en direkte effekt på α1A -underenheden og resulterer i en øget calciumstrøm gennem calciumkanalen af P/Q -typen. Responsen er dosisafhængig, da koncentrationer på 20nM og 200nM Aβ -globulomer er nødvendige for en betydelig forøgelse af calciumstrøm gennem kanalen i Xenopus -oocytter, hvilket viser, at en vis opbygning af Aβ -globulomer er nødvendig, før virkningerne ses. Når calciumstrømmen øges, stiger frigivelse af neurotransmitter også, hvilket giver en mulig årsag til toksiciteten hos patienter med Alzheimers sygdom.
Migræne hovedpine
De CACNA1A gen koder for a-underenheden af P / Q typen calcium kanal. The R192Q mutation af CACNA1A gen er et forøgelse af funktion mutation for P2X3-receptorer. P2X3 -receptorer er til stede i trigeminusganglionneuroner og menes at være en vigtig bidragyder til familiær hemiplegisk migræne . Ved at bruge et knockin -eksperiment kunne denne mutation udtrykkes i mus, så der kunne udføres forskning. Mutantmusen har en signifikant højere P2X3 -receptoraktivitet end vildtypemusen på grund af øget sandsynlighed for åben kanal og kanalaktivering ved lavere spændinger. Denne øgede receptoraktivitet resulterer i en højere strømning af calcium gennem calciumkanalen af P/Q -typen. Den øgede intracellulære calciumkoncentration kan bidrage til den akutte trigeminusmerter, der typisk resulterer i hovedpine. Beviser understøtter, at migræne er en lidelse i hjernens spænding, der er karakteriseret ved mangelfuld regulering af den kortikale excitatorisk -hæmmende balance.
Beslaglæggelser
Levetiracetam er et antiepileptisk lægemiddel, der kan bruges til behandling af partielle og generaliserede anfald . Levetiracetam hæmmer P/Q-kanal-medieret frigivelse af glutamat og reducerer de excitatoriske postsynaptiske strømme af både AMPA- og NMDA-receptorer i hippocampus , specifikt dentatgyrus , som er kendt for at sprede anfaldsaktiviteter. Inhiberingen af glutamatfrigivelse resulterer i et antiepileptisk respons hos patienter, fordi det reducerer den excitatoriske postsynaptiske strøm. Der er mange forskellige typer calciumkanaler, så for at bevise, at P/Q-type calciumkanaler er direkte involveret, blev en P/Q-type spændingshæmmet calciumkanalhæmmer, omega-agatoxin TK , brugt til at blokere kanalen. Når de blev blokeret, havde patienter ikke længere fordel af de antiepileptiske virkninger af stofferne. Når der blev anvendt blokkere for L -type og N -type calciumkanaler, blev virkningerne af Levetiracetam stadig set. Dette er et stærkt bevis på, at calciumkanaler af P/Q -typen er involveret i Levetiracetam -behandlingen, som muliggør lindring af anfald.
Mutationsundersøgelser
Mange calciumkanalmutationer af P-typen resulterer i et reduceret niveau af intracellulært frit calcium. Opretholdelse af calciumhomeostase er afgørende for normalt fungerende neuroner. Ændring af den cellulære calciumionkoncentration fungerer som en udløser for flere sygdomme, i alvorlige tilfælde kan disse sygdomme resultere i masse neuronal død.
Mutationsstudier giver eksperimenter mulighed for at studere genetisk nedarvede kanalopatier . En kanalopati er enhver sygdom, der skyldes en ionkanal med funktionssvigtige underenheder eller regulatoriske proteiner. Et eksempel på en calciumkanalkanopati af P-type er vist hos homozygote ataksiske mus, som er recessive for både de vekslende og slankere gener. Disse mus præsenterer mutationer i alfa1A -underenheden i deres P/Q -type kanaler. Mutationer i disse kanaler resulterer i mangler inden for cerebellare Purkinje -celler, der dramatisk reducerer kanalernes strømtæthed.
De vaklende mutationer i mus skyldes en missense-mutation og forårsager forsinket begyndelse af anfald og ataksi. Den vaklende mutation erstatter en enkelt prolin i stedet for en leucin inden for P-regionen af kanalen. P-regionen er ansvarlig for dannelsen af ionkanalporen . Den slankere mutation, som resulterer i mere alvorlige symptomer end den vaklende mutation, har vist sig at skyldes en enkelt nukleotidsubstitution, der forårsager splejsningssvigt inden for de kanaler, der åbner læserammen. Mutationer i den poredannende underenhed af calciumkanaler af type P forårsager ataksi, stærkt ændret åndedræt ved at reducere minutventilation og producere symptomer forbundet med atelektase . Mutationer til Ca V 2.1 har også vist sig at påvirke transmissionen inden præ-Bötzinger-komplekset , en klynge af interneuroner i hjernestammen, som hjælper med at regulere vejrtrækningen.


