Pulmonal hypertension - Pulmonary hypertension
| Pulmonal hypertension | |
|---|---|
| Andre navne | Pulmonal arteriel hypertension, Ayerza syndrom |
 | |
| Pulmonal hypertension | |
| Specialitet | Pulmologi , kardiologi |
| Symptomer | Brystsmerter, træthed |
| Almindelig start | 20 til 60 år gammel |
| Varighed | Langsigtet |
| Årsager | Ukendt |
| Risikofaktorer | Familiehistorie, lungeemboli , hiv/aids , seglcellesygdom , kokainbrug , KOL , søvnapnø , bo i store højder |
| Diagnostisk metode | Efter at have udelukket andre potentielle årsager |
| Behandling | Støttende pleje , forskellige lægemidler, lungetransplantation |
| Medicin | Epoprostenol , treprostinil , iloprost , bosentan , ambrisentan , macitentan , sildenafil |
| Frekvens | 1.000 nye sager om året (USA) |
Pulmonal hypertension ( PH eller PHTN ) er en tilstand af forhøjet blodtryk i lungerne . Symptomer omfatter åndenød , besvimelse , træthed, brystsmerter, hævelse af benene og et hurtigt hjerteslag . Tilstanden kan gøre det svært at dyrke motion. Begyndelsen er typisk gradvis.
En patient anses for at have pulmonal hypertension, hvis det pulmonale gennemsnitlige arterielle tryk er større end 25 mmHg i hvile eller større end 30 mmHg under træning.
Årsagen er ofte ukendt. Risikofaktorer omfatter en familiehistorie, tidligere blodpropper i lungerne , hiv/aids , seglcellesygdom , kokainbrug , kronisk obstruktiv lungesygdom , søvnapnø , bo i store højder og problemer med mitralventilen . Den underliggende mekanisme involverer typisk betændelse og efterfølgende ombygning af arterierne i lungerne . Diagnose indebærer først at udelukke andre potentielle årsager.
Der er i øjeblikket ingen kur mod pulmonal hypertension, selvom forskning om en kur er i gang. Behandlingen afhænger af sygdommens art. En række understøttende foranstaltninger såsom iltterapi , diuretika og medicin til at hæmme blodpropper kan anvendes. Medicin, der specifikt anvendes til behandling af pulmonal hypertension, omfatter epoprostenol , treprostinil , iloprost , bosentan , ambrisentan , macitentan og sildenafil . Lungetransplantation kan være en mulighed i alvorlige tilfælde.
Hyppigheden af forekomst anslås til omkring 1.000 nye tilfælde om året i USA. Kvinder påvirkes oftere end mænd. Starten er typisk mellem 20 og 60 år. Pulmonal hypertension blev identificeret af Ernst von Romberg i 1891.
Klassifikation
Ifølge WHO -klassificeringen er der 5 grupper af PH, hvor gruppe I (pulmonal arteriel hypertension) yderligere er opdelt i gruppe I 'og gruppe I' 'klasser. Det seneste WHO -klassificeringssystem (med tilpasninger fra de nyere ESC/ERS -retningslinjer vist i kursiv) kan opsummeres som følger:
WHO Gruppe I - Pulmonal arteriel hypertension (PAH)
- Idiopatisk
- Arvelig ( BMPR2 , ALK1 , SMAD9 , caveolin 1 , KCNK3 mutationer)
- Lægemiddel- og toksininduceret (f.eks. Anvendelse af metamfetamin )
- Tilknyttede tilstande: Bindevævssygdom , HIV -infektion , portalhypertension , medfødte hjertesygdomme , Schistosomiasis
WHO gruppe I' - Pulmonal veneokklusiv sygdom (PVOD), pulmonal kapillær hemangiomatosis (PCH)
- Idiopatisk
- Arvelige ( EIF2AK4 -mutationer)
- Narkotika, toksiner og stråleinduceret
- Tilknyttede tilstande: bindevævssygdom, HIV -infektion
WHO gruppe I " - Vedvarende pulmonal hypertension hos den nyfødte
WHO Gruppe II - Pulmonal hypertension sekundært til venstre hjerte sygdom
- Systolisk dysfunktion i venstre ventrikel
- Venstre ventrikulær diastolisk dysfunktion
- Valvulær hjertesygdom
- Medfødt/erhvervet venstre hjerteindstrømning/udstrømningskanalobstruktion og medfødt kardiomyopati
- Medfødt/erhvervet pulmonal venøs stenose
WHO Gruppe III - Pulmonal hypertension på grund af lungesygdom , kronisk hypoxi
- Kronisk obstruktiv lungesygdom (KOL)
- Interstitiel lungesygdom
- Blandede restriktive og obstruktive mønster lungesygdomme
- Søvnforstyrret vejrtrækning
- Alveolære hypoventilation lidelser
- Kronisk udsættelse for stor højde
- Udviklingsmæssige abnormiteter
WHO gruppe IV - kronisk arteriel obstruktion
- Kronisk tromboembolisk pulmonal hypertension (CTEPH)
- Andre lungearterieobstruktioner
- Angiosarcoma eller anden tumor i blodkarrene
- Arteritis
- Medfødt lungepulsåren stenose
- Parasitisk infektion ( hydatidose )
WHO Gruppe V - Pulmonal hypertension med uklare eller multifaktorielle mekanismer
- Hæmatologiske sygdomme : kronisk hæmolytisk anæmi (herunder seglcellesygdom )
- Systemiske sygdomme : sarkoidose , pulmonal Langerhans cellehistiocytose : lymfangioleiomyomatose , neurofibromatose , vaskulitis
- Metaboliske forstyrrelser : glykogenlagringssygdom , Gauchers sygdom , skjoldbruskkirtelsygdomme
- Andre: pulmonal tumoral trombotisk mikroangiopati, fibroserende mediastinitis , kronisk nyresvigt , segmentær pulmonal hypertension (pulmonal hypertension begrænset til en eller flere lapper af lungerne )
tegn og symptomer
Symptomerne på pulmonal hypertension omfatter følgende:
- Stakåndet
- Træthed
- Brystsmerter
- Hjertebanken ( øget puls )
- Højersidige mavesmerter
- Dårlig appetit
- Svimmelhed
- Besvimelse
- Hævelse (ben/ankler)
- Cyanose
Mindre almindelige tegn/symptomer omfatter ikke-produktiv hoste og træningsfremkaldt kvalme og opkastning. Hoste af blod kan forekomme hos nogle patienter, især dem med specifikke undertyper af pulmonal hypertension, såsom arvelig pulmonal arteriel hypertension, Eisenmenger syndrom og kronisk tromboembolisk pulmonal hypertension . Pulmonal venøs hypertension viser sig typisk med åndenød, mens den ligger fladt eller sover ( orthopnea eller paroxysmal natdyspnø ), mens pulmonal arteriel hypertension (PAH) typisk ikke gør det.
Andre typiske tegn på pulmonal hypertension omfatter en accentueret lungekomponent i den anden hjertelyd, en højre hjertekammer tredje hjertelyd og parasternal hiv, der indikerer en hypertrofieret højre ventrikel . Tegn på systemisk overbelastning som følge af højresidet hjertesvigt omfatter jugular venøs distension , ascites og hepatojugular reflux . Der søges også tegn på tricuspidinsufficiens og pulmonal regurgitation og er, hvis den er til stede, i overensstemmelse med tilstedeværelsen af pulmonal hypertension.
Årsager
Pulmonal hypertension er en patofysiologisk tilstand med mange mulige årsager. Denne tilstand ledsager faktisk ofte alvorlige hjerte- eller lungesygdomme. Et møde i Verdenssundhedsorganisationen i 1973 var det første forsøg på at klassificere pulmonal hypertension efter dens årsag, og der blev skelnet mellem primær PH (som følge af en sygdom i lungearterierne) og sekundær PH (resulterende sekundær til andre, ikke-vaskulære årsager) . Yderligere blev primær PH opdelt i "arteriel plexiform", "veno-okklusiv" og "tromboembolisk" form. I 1998 behandlede en anden konference i Évian-les-Bains årsagerne til sekundær PH. Efterfølgende tredje, fjerde og femte (2013) World Symposia om PAH har yderligere defineret klassificeringen af PH. Klassificeringen fortsætter med at udvikle sig baseret på forbedret forståelse af sygdomsmekanismerne.
Senest i 2015 blev WHO's retningslinjer opdateret af European Society of Cardiology (ESC) og European Respiratory Society (ERS). Disse retningslinjer er godkendt af International Society for Heart and Lung Transplantation og danner de nuværende rammer for forståelse og behandling af pulmonal hypertension.
Genetik
Mutationer i flere gener er blevet associeret med denne tilstand, disse inkluderer knoglemorfogenetisk proteinreceptor type 2 ( BMPR2 ) og eukaryotisk translation initieringsfaktor 2 alfa kinase 4 gen ( EIF2AK4 ).
Patogenese

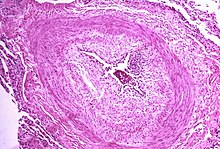
Patogenesen af pulmonal arteriel hypertension (WHO -gruppe I) involverer indsnævring af blodkar forbundet til og i lungerne. Dette gør det sværere for hjertet at pumpe blod gennem lungerne , da det er meget sværere at få vand til at strømme gennem et smalt rør i modsætning til et bredt. Over tid bliver de berørte blodkar stivere og tykkere i en proces kendt som fibrose . Mekanismerne, der er involveret i denne indsnævringsproces, omfatter vasokonstriktion , trombose og vaskulær ombygning (overdreven cellulær spredning, fibrose og reduceret apoptose/programmeret celledød i karvæggene forårsaget af betændelse , forstyrret metabolisme og dysregulering af visse vækstfaktorer ). Dette øger blodtrykket yderligere i lungerne og forringer deres blodgennemstrømning. Ligesom andre former for pulmonal hypertension resulterer disse ændringer i en øget arbejdsbyrde for højre side af hjertet. Den højre ventrikel er normalt en del af et lavtrykssystem, med systoliske ventrikulære tryk, der er lavere end dem, venstre ventrikel normalt møder. Som sådan kan den højre ventrikel ikke lige så godt klare højere tryk, og selvom højre ventrikels tilpasninger ( hypertrofi og øget kontraktilitet i hjertemusklen) i første omgang hjælper med at bevare slagvolumen , er disse kompenserende mekanismer i sidste ende utilstrækkelige; den højre ventrikelmuskel kan ikke få nok ilt til at opfylde sine behov, og højre hjertesvigt følger. Når blodet, der strømmer gennem lungerne, falder, modtager hjertets venstre side mindre blod. Dette blod kan også bære mindre ilt end normalt. Derfor bliver det sværere og sværere for venstre side af hjertet at pumpe for at levere tilstrækkelig ilt til resten af kroppen, især under fysisk aktivitet. Under den end-systoliske volumenfase i hjertecyklussen viste det sig, at den gaussiske krumning og den gennemsnitlige krumning af højre ventrikulære endokardievæg hos PH-patienter var signifikant forskellige i forhold til kontrollerne.
I PVOD (WHO-gruppe I ') sker indsnævring af pulmonal blodkar fortrinsvis (dog ikke udelukkende) i post-kapillære venøse blodkar. PVOD deler flere karakteristika med PAH, men der er også nogle vigtige forskelle, f.eks. Forskelle i prognose og respons på medicinsk behandling.
Vedvarende pulmonal hypertension hos den nyfødte opstår, når kredsløbet hos en nyfødt baby ikke tilpasser sig livet uden for livmoderen; det er kendetegnet ved høj modstandsdygtighed over for blodgennemstrømning gennem lungerne, højre-til-venstre hjerte-shunting og alvorlig hypoxæmi .
Patogenese ved pulmonal hypertension på grund af venstre hjertesygdom (WHO -gruppe II) er helt anderledes, idet indsnævring eller beskadigelse af lungeblodkar ikke er problemet. I stedet undlader det venstre hjerte at pumpe blod effektivt, hvilket fører til samling af blod i lungerne og modtryk i lungesystemet. Dette forårsager lungeødem og pleural effusion . I mangel af indsnævring af pulmonal blodkar beskrives det øgede modtryk som 'isoleret post-kapillær pulmonal hypertension' (ældre udtryk inkluderer 'passiv' eller 'proportionel' pulmonal hypertension eller 'pulmonal venøs hypertension'). Hos nogle patienter udløser det forhøjede tryk i lungekarrene imidlertid en overlejret komponent i fartøjets indsnævring, hvilket yderligere øger arbejdsbyrden på højre side af hjertet. Dette betegnes som 'post-kapillær pulmonal hypertension med en præ-kapillær komponent' eller 'kombineret post-kapillær og præ-kapillær pulmonal hypertension' (ældre udtryk inkluderer 'reaktiv' eller 'uden for proportioner' pulmonal hypertension).
Ved pulmonal hypertension på grund af lungesygdomme og/eller hypoxi (WHO -gruppe III ) forårsager lave iltniveauer i alveolerne (på grund af luftvejssygdomme eller lever i stor højde) indsnævring af lungearterierne. Dette fænomen kaldes hypoksisk pulmonal vasokonstriktion, og det er i første omgang en beskyttende reaktion designet til at stoppe for meget blodstrømning til områder af lungen, der er beskadiget og ikke indeholder ilt. Når den alveolære hypoxi er udbredt og forlænget, forekommer denne hypoxi-medierede vasokonstriktion på tværs af en stor del af det lungevaskulære leje og fører til en stigning i pulmonal arterielt tryk, med fortykkelse af lungekarvæggene, der bidrager til udviklingen af vedvarende pulmonal hypertension. Langvarig hypoxi inducerer også transkriptionsfaktoren HIF1A , som direkte aktiverer nedstrøms vækstfaktorsignalering, der forårsager irreversibel proliferation og ombygning af pulmonale arterielle endotelceller, hvilket fører til kronisk pulmonal arteriel hypertension.
I CTEPH (WHO Gruppe IV) menes den initierende hændelse at være blokering eller indsnævring af lungeblodkarene med uløste blodpropper; disse blodpropper kan føre til øget tryk og forskydningsspænding i resten af lungekredsløbet og udfælde strukturelle ændringer i karvæggene (ombygning) svarende til dem, der observeres ved andre former for alvorlig pulmonal hypertension. Denne kombination af fartøjsoklusion og vaskulær ombygning øger igen modstanden mod blodgennemstrømning, og trykket i systemet stiger.
Molekylær patologi
Den molekylære mekanisme for pulmonal arteriel hypertension (PAH) er endnu ikke kendt, men det menes, at endoteldysfunktionen resulterer i et fald i syntesen af endotel-afledte vasodilatorer såsom nitrogenoxid og prostacyclin . Desuden er der en stimulering af syntesen af vasokonstriktorer, såsom thromboxan og vaskulær endotelvækstfaktor (VEGF). Disse resulterer i en alvorlig vasokonstriktion og vaskulær glat muskulatur og adventitial hypertrofi karakteristisk for patienter med PAH.
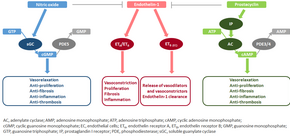
Nitrogenoxidopløseligt guanylatcyklasevej
Under normale forhold producerer den vaskulære endotel nitrogenoxid syntase nitrogenoxid fra L-arginin i nærvær af ilt.
Dette nitrogenoxid diffunderer ind i naboceller (herunder vaskulære glatte muskelceller og blodplader), hvor det øger aktiviteten af enzymopløseligt guanylatcyklase , hvilket fører til øget dannelse af cyklisk guanosinmonophosphat (cGMP) fra guanosintrifosfat (GTP). CGMP aktiverer derefter cGMP-afhængig kinase eller PKG (proteinkinase G). Aktiveret PKG fremmer vasorelaksation (via en reduktion af intracellulære calciumniveauer), ændrer ekspressionen af gener, der er involveret i sammentrækning af glatte muskelceller, migration og differentiering og hæmmer blodpladeaktivering . Nitrogenoxidopløseligt guanylatcyklasesignalering fører også til antiinflammatoriske virkninger.
Phosphodiesterase type 5 ( PDE5 ), som er rigeligt i lungevævet, hydrolyserer den cykliske binding af cGMP. Følgelig falder koncentrationen af cGMP (og dermed PKG -aktivitet).
Endothelin
Endothelin-1 er et peptid (omfattende 21 aminosyrer), der produceres i endotelceller. Det virker på endotelinreceptorerne ETA og ETB i forskellige celletyper, herunder vaskulære glatte muskelceller og fibroblaster, hvilket fører til vasokonstriktion, hypertrofi, proliferation, betændelse og fibrose. Det virker også på ETB -receptorer i endotelceller; dette fører til frigivelse af både vasokonstriktorer og vasodilatatorer fra disse celler og fjerner endothelin-1 fra systemet.
Prostacyclin (og thromboxan)
Prostacyclin syntetiseres fra arachidonsyre i endotelceller. I vaskulære glatte muskelceller bindes prostacyclin hovedsageligt til prostaglandin I -receptoren. Dette sender et signal om at øge adenylatcyclase -aktivitet, hvilket fører til øget syntese af cyklisk adenosinmonophosphat (cAMP). Dette fører igen til øget cAMP-afhængig proteinkinase eller PKA (proteinkinase A) aktivitet, hvilket i sidste ende fremmer vasodilatation og hæmmer celleproliferation. Prostacyclins signalering fører også til antitrombotiske, anti-fibrotiske og antiinflammatoriske virkninger. Niveauer af cAMP (som medierer de fleste af de biologiske virkninger af prostacyclin) reduceres med phosphodiesteraser 3 og 4. Vasokonstriktor -thromboxan syntetiseres også fra arachidonsyre. I PAH forskydes balancen væk fra syntese af prostacyclin til syntese af thromboxan.
Andre veje
De tre beskrevne veje er alle målrettet mod aktuelt tilgængelige medicinske behandlinger for PAH. Imidlertid er der identificeret flere andre veje, der også er ændret i PAH og undersøges som potentielle mål for fremtidige behandlinger. For eksempel aktiveres mitokondrialt enzym pyruvat dehydrogenase kinase (PDK) patologisk i PAH, hvilket forårsager et metabolisk skift fra oxidativ phosphorylering til glykolyse og fører til øget celleproliferation og nedsat apoptose. Ekspression af vasoaktivt tarmpeptid, en potent vasodilatator med antiinflammatoriske og immunmodulerende roller, reduceres i PAH, mens ekspressionen af dets receptor øges. Plasmaniveauer af serotonin, som fremmer vasokonstriktion, hypertrofi og proliferation, øges hos patienter med PAH, selv om serotonins rolle i patogenesen af PAH stadig er usikker. Udtrykket eller aktiviteten af flere vækstfaktorer (herunder trombocytafledt vækstfaktor , grundlæggende fibroblastvækstfaktor , epidermal vækstfaktor og vaskulær endotelvækstfaktor ) øges og bidrager til vaskulær ombygning i PAH. Andre faktorer, der ligger til grund for den proliferative tilstand af pulmonal vaskulære glatte muskelceller, inkluderer OPG og TRAIL . Kun fokusering på lungevaskulaturen giver et ufuldstændigt billede af PAH; den højre ventrikels evne til at tilpasse sig den øgede arbejdsbyrde varierer mellem patienterne og er en vigtig determinant for overlevelse. PAH's molekylære patologi i højre ventrikel undersøges derfor også, og nyere forskning har skiftet til at betragte kardiopulmonær enhed som et enkelt system frem for to separate systemer. Det er vigtigt, at ombygning i højre ventrikel er forbundet med øget apoptose; dette er i modsætning til pulmonal vaskulær ombygning, der involverer inhibering af apoptose.
Diagnose

Med hensyn til diagnosen pulmonal hypertension har den fem hovedtyper, og der skal udføres en række tests for at skelne pulmonal arteriel hypertension fra venøse, hypoksiske, tromboemboliske eller uklare multifaktorielle sorter. PAH diagnosticeres efter udelukkelse af andre mulige årsager til pulmonal hypertension.
Fysisk undersøgelse
En fysisk undersøgelse udføres for at lede efter typiske tegn på pulmonal hypertension (beskrevet ovenfor ), og en detaljeret familiehistorie etableres for at afgøre, om sygdommen kan være arvelig . En historie med eksponering for lægemidler såsom benfluorex (et fenfluraminderivat ), dasatinib , kokain , methamfetamin , ethanol, der fører til skrumpelever , og tobak, der fører til emfysem, anses for at være signifikant. Brug af selektive serotonin genoptagelseshæmmere under graviditeten (især sen graviditet) er forbundet med en øget risiko for, at barnet udvikler vedvarende pulmonal hypertension hos den nyfødte .
Ekkokardiografi
Hvis der er mistanke om pulmonal hypertension baseret på ovenstående vurderinger, udføres ekkokardiografi som det næste trin. En metaanalyse af Doppler-ekkokardiografi til forudsigelse af resultaterne af højre hjertekateterisering rapporterede en følsomhed og specificitet på henholdsvis 88% og 56%. Således kan Doppler -ekkokardiografi tyde på tilstedeværelsen af pulmonal hypertension, men kardisering af højre hjerte (beskrevet nedenfor) forbliver guldstandarden for diagnose af PAH. Ekkokardiografi kan også hjælpe med at opdage medfødt hjertesygdom som årsag til pulmonal hypertension.
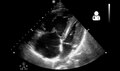
4 måneder gammel med pulmonal hypertension set ved ultralyd
4 måneder gammel med pulmonal hypertension set ved ultralyd
4 måneder gammel med pulmonal hypertension set ved ultralyd
Langvarig pulmonal hypertension
Ekskluder andre sygdomme
Hvis ekkokardiogrammet er kompatibelt med en diagnose af pulmonal hypertension, overvejes almindelige årsager til pulmonal hypertension (venstre hjertesygdom og lungesygdom), og yderligere tests udføres i overensstemmelse hermed. Disse tests omfatter generelt elektrokardiografi (EKG), lungefunktionstests, herunder lungediffusionskapacitet til kulilte og målinger af arteriel blodgas , røntgenstråler i brystet og computertomografi med høj opløsning (CT).
Ventilation/perfusion scintigrafi
Hvis hjertesygdomme og lungesygdomme er blevet udelukket, udføres en ventilation/perfusionsscanning for at udelukke CTEPH. Hvis der findes uovertrufne perfusionsdefekter, udføres yderligere evaluering ved CT -lungeangiografi, højre hjertekateterisering og selektiv pulmonal angiografi.
CT-scanning
Tegn på pulmonal hypertension ved CT -scanning af brystet er:
- Forstørrelse af lungestammen (målt ved dens forgrening). Det er imidlertid en dårlig forudsigelse for pulmonal hypertension hos patienter med interstitiel lungesygdom .
- En diameter på mere end 27 mm for kvinder og 29 mm for mænd foreslås som en afskæring .
- En cutoff på 31,6 mm kan være en mere statistisk robust hos personer uden interstitiel lungesygdom .
- Øget forhold mellem diameteren af hovedpulsåren (lungestammen) og den stigende aorta (målt ved dens bifurkation).
- Et forhold på 1,0 foreslås som en cutoff hos voksne.
- Cutoff ~ 1,09 hos børn.
- Øget diameterforhold mellem segmentale arterier og bronchi. Dette fund i tre eller fire lober i nærvær af en udvidet lungestamme (≥29 mm) og fravær af signifikant strukturel lungesygdom giver en specificitet på 100% for pulmonal hypertension.
- Malkalkalkning i centrale lungearterier ses hyppigst hos patienter med Eisenmenger syndrom .
Kateterisering i højre hjerte
Selvom pulmonal arterielt tryk (PAP) kan estimeres på grundlag af ekkokardiografi , giver trykmålinger med et Swan-Ganz-kateter indsat gennem højre side af hjertet den mest deciderede vurdering. [42] Pulmonal hypertension er defineret som en gennemsnitlig PAP på mindst 20 mm Hg (3300 Pa) i hvile, og PAH er defineret som prækapillær pulmonal hypertension (dvs. middelværdi PAP ≥ 20 mm Hg med pulmonal arteriel okklusionstryk [PAOP] ≤ 15 mm Hg og pulmonal vaskulær resistens [PVR]> 3 træenheder). PAOP og PVR kan ikke måles direkte med ekkokardiografi. Derfor kræver diagnose af PAH højresidig hjertekateterisering. Et Swan-Ganz kateter kan også måle hjerteeffekten; dette kan bruges til at beregne hjerteindekset, som er langt vigtigere ved måling af sygdommens sværhedsgrad end det pulmonale arterielle tryk. Gennemsnitlig PAP (mPAP) bør ikke forveksles med systolisk PAP (sPAP), som ofte rapporteres om ekkokardiogramrapporter. Et systolisk tryk på 40 mm Hg indebærer typisk et middeltryk på mere end 25 mm Hg. Groft, mPAP = 0,61 • sPAP + 2.
Andet
For mennesker, der anses for sandsynligt at have PAH baseret på ovenstående tests, bestemmes den specifikke associerede tilstand derefter baseret på fysisk undersøgelse, medicinsk/familiehistorie og yderligere specifikke diagnostiske tests (f.eks. Serologiske tests til påvisning af underliggende bindevævssygdom, HIV -infektion eller hepatitis, ultralyd for at bekræfte tilstedeværelsen af portalhypertension, ekkokardiografi/hjertemagnetisk resonansbilleddannelse for medfødt hjertesygdom, laboratorietest for schistosomiasis og højopløselig CT for PVOD og pulmonal kapillær hæmangiomatose). Rutinemæssig lungebiopsi frarådes hos patienter med PAH på grund af risikoen for patienten, og fordi resultaterne sandsynligvis ikke ændrer diagnosen og behandlingen.
Behandling
Behandling af pulmonal hypertension bestemmes af, om PH er arteriel, venøs, hypoksisk, tromboembolisk eller diverse. Hvis det er forårsaget af venstre hjertesygdom, er behandlingen at optimere venstre ventrikelfunktion ved brug af medicin eller at reparere/udskifte mitralventilen eller aortaklappen . Patienter med venstre hjertesvigt eller hypoxæmiske lungesygdomme ( pulje pulmonal hypertension i gruppe II eller III) bør ikke rutinemæssigt behandles med vasoaktive midler, herunder prostanoider, phosphodiesterasehæmmere eller endotelinantagonister, da disse er godkendt til den forskellige tilstand, der kaldes primær pulmonal arteriel hypertension. For at skelne mellem dem vil læger som minimum foretage hjertekateterisering af det højre hjerte, ekkokardiografi, CT på brystet, en seks minutters gåtest og test af lungefunktion . Brug af behandlinger til andre former for pulmonal hypertension hos patienter med disse tilstande kan skade patienten og spilde betydelige medicinske ressourcer.
Højdosis calciumkanalblokkere er anvendelige i kun 5% af IPAH patienter, som er vasoreactive ved Swan-Ganz kateter . Desværre er calciumkanalblokkere stort set blevet misbrugt og blev ordineret til mange patienter med ikke-vasoreaktivt PAH, hvilket førte til overdreven sygelighed og dødelighed. Kriterierne for vasoreaktivitet er ændret. Kun de patienter, hvis gennemsnitlige lungearteretryk falder med mere end 10 mm Hg til mindre end 40 mm Hg med en uændret eller øget hjerteeffekt, når de udfordres med adenosin , epoprostenol eller nitrogenoxid, betragtes som vasoreaktive. Af disse er kun halvdelen af patienterne lydhøre over for calciumkanalblokkere på lang sigt.
En række agenter er for nylig blevet introduceret til primær og sekundær PAH. Forsøgene, der understøtter brugen af disse midler, har været relativt små, og det eneste mål, der konsekvent blev brugt til at sammenligne deres effektivitet, er "6 minutters gåtest". Mange har ingen data om dødelighedsydelse eller tid til progression.
Vasoaktive stoffer
Mange veje er involveret i den unormale spredning og sammentrækning af pulmonal arteries glatte muskelceller hos patienter med pulmonal arteriel hypertension. Tre af disse veje er vigtige, da de er blevet målrettet mod lægemidler- endothelinreceptorantagonister , phosphodiesterase type 5 (PDE-5) -hæmmere og prostacyclinderivater.
Prostaglandiner
Prostacyclin ( prostaglandin I 2 ) betragtes almindeligvis som den mest effektive behandling af PAH. Epoprostenol (syntetisk prostacyclin ) gives via kontinuerlig infusion, der kræver et semi-permanent centralt venekateter . Dette leveringssystem kan forårsage sepsis og trombose . Prostacyclin er ustabil og skal derfor opbevares på is under administration. Da infusionen har en halveringstid på 3 til 5 minutter, skal infusionen være kontinuerlig, og afbrydelse kan være dødelig. Andre prostanoider er derfor blevet udviklet. Treprostinil kan gives intravenøst eller subkutant, men den subkutane form kan være meget smertefuld. En øget risiko for sepsis med intravenøs Remodulin er blevet rapporteret af CDC . Iloprost bruges også i Europa intravenøst og har en længere halveringstid. Iloprost var den eneste inhalerede form for prostacyclin godkendt til brug i USA og Europa, indtil den inhalerede form af treprostinil blev godkendt af FDA i juli 2009.
Endotelinreceptorantagonister
Moderat kvalitetsbevis tyder på, at endotelinreceptorantagonister forbedrer træningskapaciteten og reducerer symptomernes sværhedsgrad. Den dobbelte (ET A og ET B ) endothelin -receptorantagonist bosentan blev godkendt i 2001. Sitaxentan (Thelin) blev godkendt til brug i Canada, Australien, og EU, men ikke i USA. I 2010 trak Pfizer Thelin tilbage på verdensplan på grund af dødelige leverkomplikationer. Et lignende lægemiddel, ambrisentan , markedsføres som Letairis i USA af Gilead Sciences .s
Phosphodiesterase type 5 -hæmmere
Den amerikanske FDA godkendte sildenafil , en selektiv hæmmer af cGMP -specifik phosphodiesterase type 5 (PDE5), til behandling af PAH i 2005. Det markedsføres for PAH som Revatio. I 2009 godkendte de også tadalafil , en anden PDE5 -hæmmer, der blev markedsført under navnet Adcirca. PDE5 -hæmmere menes at øge vasodilatation af lungearterier og hæmme vaskulær ombygning og dermed sænke pulmonal arterielt tryk og pulmonal vaskulær modstand.
Tadalafil tages oralt såvel som sildenafil, og det absorberes hurtigt (serumniveauer kan påvises efter 20 minutter). T 1/2 ( biologisk halveringstid ) svæver omkring 17,5 timer hos raske forsøgspersoner. Desuden, hvis vi overvejer farmakoøkonomiske konsekvenser, ville patienter, der tager tadalafil, betale to tredjedele af omkostningerne ved sildenafilbehandling. Der er dog nogle negative virkninger af dette lægemiddel, såsom hovedpine, diarré, kvalme, rygsmerter, dyspepsi , rødme og myalgi .
Aktivatorer af opløselig guanylatcyklase
Opløselig guanylatcyklase (sGC) er den intracellulære receptor for NO . Fra april 2009 gennemgik sGC -aktivatorerne cinaciguat og riociguat kliniske forsøg til behandling af PAH.
Kirurgisk
Atrial septostomi er en kirurgisk procedure, der skaber en kommunikation mellem højre og venstre atria . Det lindrer trykket på højre side af hjertet, men på bekostning af lavere iltindhold i blodet ( hypoxi ). Lungetransplantation erstatter en kronisk tilstand med det igangværende behov for behandling. Der er en postoperativ median overlevelse på godt fem år.
Pulmonal tromboendarterektomi (PTE) er en kirurgisk procedure, der bruges til kronisk tromboembolisk pulmonal hypertension. Det er kirurgisk fjernelse af en organiseret blodprop (blodprop) sammen med slimhinden i lungearterien; det er en meget vanskelig, større procedure, der i øjeblikket udføres i et par udvalgte centre.
Overvågning
Etablerede retningslinjer for klinisk praksis dikterer hyppigheden af evaluering og overvågning af lungeknuder, patienter overvåges normalt gennem almindeligt tilgængelige tests såsom:
- Pulsoximetri
- Arterielle blodgas test
- Bryst røntgenstråler
- Serielle EKG -test
- Seriel ekkokardiografi
- Spirometri eller mere avancerede lungefunktionsundersøgelser
- 6 minutters gangtest
Prognose
PAH betragtes som en universelt dødelig sygdom, selvom overlevelsestiden kan variere mellem individer. Prognosen for pulmonal arteriel hypertension (WHO gruppe I) har en ubehandlet median overlevelse på 2-3 år fra diagnosetidspunktet, hvor dødsårsagen normalt er højre ventrikelsvigt ( cor pulmonale ). Overlevelsestiden er variabel og afhænger af mange faktorer. En nylig udfaldsundersøgelse af de patienter, der var startet behandling med bosentan (Tracleer) viste, at 89% af patienterne var i live efter 2 år. Med nye terapier stiger overlevelsesraten. For 2.635 patienter, der var tilmeldt registreringsdatabasen for at evaluere tidlig og langsigtet håndtering af lungearteriel hypertension (REVEAL Registry) fra marts 2006 til december 2009, var 1-, 3-, 5- og 7-års overlevelse 85%, 68 Henholdsvis%, 57%og 49%. For patienter med idiopatisk/familiær PAH var overlevelsesraten 91%, 74%, 65%og 59%. Dødeligheden er meget høj hos gravide kvinder med svær pulmonal arteriel hypertension (WHO -gruppe I). Graviditet beskrives undertiden som kontraindiceret hos disse kvinder.
Epidemiologi
Epidemiologien ved IPAH er omkring 125–150 dødsfald om året i USA, og på verdensplan er forekomsten ens med 4 tilfælde pr. Million. I dele af Europa (Frankrig) er indikationer imidlertid 6 tilfælde pr. Million IPAH. Kvinder har en højere forekomst end mænd (2–9: 1).
Andre former for PH er langt mere almindelige. Ved systemisk sklerodermi er forekomsten blevet estimeret til at være 8 til 12% af alle patienter; ved leddegigt er det sjældent. I systemisk lupus erythematosus er den imidlertid 4 til 14%, og ved seglcellesygdomme varierer den fra 20 til 40%. Op til 4% af de mennesker, der lider af lungeemboli, udvikler fortsat kronisk tromboembolisk sygdom, herunder pulmonal hypertension. En lille procentdel af patienter med KOL udvikler pulmonal hypertension uden anden sygdom for at forklare det høje tryk. På den anden side er fedme-hypoventilationssyndrom meget almindeligt forbundet med højre hjertesvigt på grund af pulmonal hypertension.
Forskning
For mennesker, der har arvet sygdommen, undersøges genterapi.
Bemærkelsesværdige sager
- Elaine Kaufman , amerikansk restauratør
- Ina Balin , amerikansk Broadway og tv -skuespiller
- Chloe Temtchine , amerikansk singer-songwriter
- Natalie Cole , amerikansk sangerinde
Se også
Referencer
Yderligere læsning
- Rubin LJ, Badesch DB (august 2005). "Evaluering og håndtering af patienten med pulmonal arteriel hypertension". Annals of Internal Medicine . 143 (4): 282–92. CiteSeerX 10.1.1.463.8466 . doi : 10.7326/0003-4819-143-4-200508160-00009 . PMID 16103472 . S2CID 28841269 .
- Abman SH, Hansmann G, Archer SL, Ivy DD, Adatia I, Chung WK, et al. (November 2015). "Pædiatrisk pulmonal hypertension: Retningslinjer fra American Heart Association og American Thoracic Society" . Cirkulation . 132 (21): 2037–99. doi : 10.1161/CIR.0000000000000329 . PMID 26534956 . S2CID 7412370 .
eksterne links
| Klassifikation | |
|---|---|
| Eksterne ressourcer |
| Scholia har et emne profil for pulmonal hypertension . |