Hormonerstatningsterapi - Hormone replacement therapy
Hormonerstatningsterapi ( HRT ), også kendt som hormonbehandling i overgangsalderen eller postmenopausal hormonbehandling , er en form for hormonbehandling, der bruges til at behandle symptomer forbundet med kvindelig overgangsalder . Disse symptomer kan omfatte hedeture , vaginal atrofi , accelereret hud ældning, vaginal tørhed , nedsat muskelmasse , seksuel dysfunktion , og knogletab . De er i høj grad relateret til det formindskede niveau af kønshormoner, der opstår i overgangsalderen.
De vigtigste hormonelle lægemidler, der bruges i HRT til menopausale symptomer, er østrogener og progestogener , blandt hvilke progesteron er det vigtigste naturligt forekommende kvindelige kønshormon og også en fremstillet medicin, der bruges i overgangsalderhormonbehandling. Selvom begge kan have symptomatiske fordele, tilføjes gestagen specifikt til østrogenregimer, når livmoderen stadig er til stede. Ubestemt østrogenbehandling fremmer endometriets fortykkelse og kan øge risikoen for kræft , mens gestagen reducerer denne risiko. Androgener som testosteron bruges undertiden også. HRT er tilgængelig på en række forskellige ruter .
De langsigtede virkninger af HRT på de fleste organsystemer varierer efter alder og tid siden den sidste fysiologiske eksponering for hormoner, og der kan være store forskelle i individuelle regimer, faktorer der har gjort det svært at analysere effekter. Den Kvinders Health Initiative (WHI) er en igangværende undersøgelse af over 27.000 kvinder, der begyndte i 1991, med den seneste analyser tyder på, at når iværksat inden for 10 år i forbindelse med overgangsalderen, HRT reducerer mortalitet af alle årsager og risici for koronar sygdom, osteoporose, og demens; efter 10 år er de gavnlige virkninger på dødelighed og koronar hjertesygdom ikke længere synlige, selvom der er reducerede risici for hofte- og hvirvelbrud og en øget risiko for venøs tromboemboli, når de tages oralt.
"Bioidentisk" hormonerstatning er en udvikling i det 21. århundrede og bruger fremstillede forbindelser med "nøjagtig samme kemiske og molekylære struktur som hormoner, der produceres i menneskekroppen." Disse er hovedsageligt steroider afledt af planter og kan være en komponent i enten registrerede farmaceutiske eller specialfremstillede sammensatte præparater, hvor sidstnævnte generelt ikke anbefales af tilsynsmyndigheder på grund af deres mangel på standardisering og formelt tilsyn. Bioidentisk hormonerstatning har utilstrækkelig klinisk forskning til at fastslå dets sikkerhed og virkning fra 2017.
De nuværende indikationer for brug fra United States Food and Drug Administration (FDA) omfatter kortvarig behandling af menopausale symptomer , såsom vasomotoriske hedeture eller vaginal atrofi , og forebyggelse af osteoporose .
Medicinske anvendelser
Godkendte anvendelser af HRT i USA omfatter kortvarig behandling af menopausale symptomer såsom hedeture og vaginal atrofi og forebyggelse af osteoporose. Den American College of Obstetrik og Gynækologi (ACOG) godkender HRT til symptomatisk lindring af symptomer på overgangsalderen, og går ind for dens anvendelse efter en alder af 65 i passende scenarier. Den nordamerikanske Menopause Society (NAMS) 2016 årlige møde nævnt, at HRT kan have flere fordele end risici hos kvinder før en alder af 60.
En konsensus -ekspertudtalelse udgivet af The Endocrine Society udtalte, at når det tages i løbet af perimenopausen eller de første år af overgangsalderen, bærer HRT færre risici end tidligere offentliggjort og reducerer alle dødsårsager i de fleste scenarier. Den amerikanske sammenslutning af endokrinologer (AACE) har også udgivet stillingtagen godkendelse af HRT i passende scenarier.
Kvinder, der modtager denne behandling, er normalt post- , peri- eller kirurgisk overgangsalder . Overgangsalderen er det permanente ophør af menstruation som følge af tab af follikelaktivitet i æggestokkene, defineret som begyndelsen tolv måneder efter den sidste naturlige menstruationscyklus. Dette tidspunkt på tolv måneder opdeler overgangsalderen i tidlige og sene overgangsperioder kendt som 'perimenopause' og 'postmenopause'. For tidlig overgangsalder kan opstå, hvis æggestokkene fjernes kirurgisk , som det kan gøres for at behandle kræft i æggestokkene eller livmoderen .
Demografisk er langt størstedelen af de tilgængelige data om postmenopausale amerikanske kvinder med samtidige allerede eksisterende tilstande og en gennemsnitsalder på over 60 år.
Overgangsalder symptomer
HRT gives ofte som en kortvarig lindring af menopausale symptomer under perimenopausen . Potentielle menopausale symptomer omfatter:
- Hot flashes - vasomotoriske symptomer
- Vulvovaginal atrofi - atrofisk vaginitis og tørhed
- Dyspareunia - smertefuldt samleje på grund af vaginal atrofi og mangel på smøring
- Knogletab - nedsat knoglemineraltæthed , som i sidste ende kan føre til osteopeni , knogleskørhed og tilhørende brud
- Nedsat seksuel lyst
- Defeminisering - formindsket feminin fedtfordeling og accelereret hudaldring
- Søvnforstyrrelser og ledsmerter
Den mest almindelige af disse er tab af seksualdrift og vaginal tørhed .
Hjerte sygdom

Virkningen af HRT i overgangsalderen ser ud til at være divergerende med lavere risiko, når den startes inden for fem år, men ingen effekt efter ti. Der kan være en stigning i hjertesygdomme, hvis HRT gives tyve år efter overgangsalderen. Denne variation har ført til, at nogle anmeldelser tyder på, at der ikke er nogen signifikant effekt på sygelighed. Desuden er der ingen forskel i langtidsdødelighed fra HRT, uanset alder.
En Cochrane -undersøgelse antydede, at kvinder, der startede HRT mindre end 10 år efter overgangsalderen, havde lavere dødelighed og koronar hjertesygdom uden nogen stærk effekt på risikoen for slagtilfælde og lungeemboli . Dem, der startede terapi mere end 10 år efter overgangsalderen, viste ringe effekt på dødelighed og koronar hjertesygdom, men en øget risiko for slagtilfælde. Begge terapier havde en tilknytning til blodpropper og lungeemboli.
HRT med østrogen og progesteron forbedrer også kolesteroltalet . Med overgangsalderen falder HDL , mens LDL , triglycerider og lipoprotein øges, mønstre der vender med østrogen. Ud over dette, HRT forbedrer hjerte sammentrækning , koronar blodgennemstrømning, sukker stofskifte , og nedsætter blodplade aggregering og plakdannelse . HRT kan fremme omvendt kolesteroltransport gennem induktion af kolesterol ABC -transportører . HRT resulterer også i en stor reduktion i det pro-trombotiske lipoprotein a . Undersøgelser om kardiovaskulær sygdom med testosteronbehandling er blevet blandet, hvoraf nogle tyder på ingen effekt eller en mild negativ effekt, selvom andre har vist en forbedring af surrogatmarkører som kolesterol, triglycerider og vægt. Testosteron har en positiv effekt på vaskulær endotelfunktion og tone med observationsstudier, der tyder på, at kvinder med lavere testosteron kan have større risiko for hjertesygdomme. Tilgængelige undersøgelser er begrænset af lille stikprøvestørrelse og undersøgelsesdesign. Lavt kønshormonbindende globulin, der opstår med overgangsalderen, er forbundet med øget kropsmasseindeks og risiko for type 2 -diabetes.
Blodpropper
Virkninger af hormonerstatningsterapi på dannelse af venøs blodprop og potentiale for lungeemboli kan variere med forskellige østrogen- og gestagenterapier og med forskellige doser eller anvendelsesmetoder. Sammenligninger mellem indgivelsesveje tyder på, at når østrogener påføres huden eller skeden, er der en lavere risiko for blodpropper, hvorimod risikoen for blodpropper og lungeemboli øges, når den bruges oralt. Hud- og vaginale ruter for hormonbehandling er ikke genstand for first -pass metabolisme og mangler derfor de anabolske virkninger, som oral terapi har på leversyntese af vitamin K -afhængige koagulationsfaktorer , hvilket muligvis forklarer, hvorfor oral behandling kan øge dannelsen af blodpropper.
Mens en anmeldelse fra 2018 viste, at det at tage progesteron og østrogen sammen kan reducere denne risiko, rapporterede andre anmeldelser en øget risiko for blodpropper og lungeemboli, når østrogen og gestagen blev kombineret, især når behandlingen blev startet 10 år eller mere efter overgangsalderen og når kvinderne var ældre end 60 år.
Risikoen for venøs tromboemboli kan reduceres med bioidentiske præparater, selvom forskning om dette kun er foreløbig.
| Type | Rute | Medicin | Odds ratio (95% CI ) |
|---|---|---|---|
| Menopausal hormonbehandling | Mundtlig |
Estradiol alene ≤1 mg/dag > 1 mg/dag |
1,27 (1,16–1,39)* 1,22 (1,09–1,37)* 1,35 (1,18–1,55)* |
|
Konjugerede østrogener alene ≤0,625 mg/dag > 0,625 mg/dag |
1,49 (1,39–1,60)* 1,40 (1,28–1,53)* 1,71 (1,51–1,93)* |
||
| Estradiol/medroxyprogesteronacetat | 1,44 (1,09–1,89)* | ||
|
Estradiol/dydrogesteron ≤1 mg/dag E2 > 1 mg/dag E2 |
1,18 (0,98–1,42) 1,12 (0,90–1,40) 1,34 (0,94–1,90) |
||
|
Estradiol/norethisteron ≤1 mg/dag E2 > 1 mg/dag E2 |
1,68 (1,57–1,80)* 1,38 (1,23–1,56)* 1,84 (1,69–2,00)* |
||
| Estradiol/norgestrel eller estradiol/drospirenon | 1,42 (1,00–2,03) | ||
| Konjugerede østrogener/medroxyprogesteronacetat | 2.10 (1.92–2.31)* | ||
|
Konjugerede østrogener/norgestrel ≤0,625 mg/dag CEE'er > 0,625 mg/dag CEE'er |
1,73 (1,57–1,91)* 1,53 (1,36–1,72)* 2,38 (1,99–2,85)* |
||
| Tibolone alene | 1,02 (0,90–1,15) | ||
| Raloxifene alene | 1,49 (1,24–1,79)* | ||
| Transdermal |
Estradiol alene ≤50 μg/dag > 50 μg/dag |
0,96 (0,88–1,04) 0,94 (0,85–1,03) 1,05 (0,88–1,24) |
|
| Estradiol / gestagen | 0,88 (0,73–1,01) | ||
| Vaginal | Estradiol alene | 0,84 (0,73–0,97) | |
| Konjugerede østrogener alene | 1,04 (0,76–1,43) | ||
| Kombineret prævention | Mundtlig | Ethinylestradiol/norethisteron | 2,56 (2,15–3,06)* |
| Ethinylestradiol/levonorgestrel | 2,38 (2,18–2,59)* | ||
| Ethinylestradiol/norgestimat | 2,53 (2,17–2,96)* | ||
| Ethinylestradiol/desogestrel | 4,28 (3,66–5,01)* | ||
| Ethinylestradiol/gestoden | 3,64 (3,00–4,43)* | ||
| Ethinylestradiol/drospirenon | 4,12 (3,43–4,96)* | ||
| Ethinylestradiol/cyproteronacetat | 4,27 (3,57–5,11)* | ||
| Bemærkninger: (1) Indlejrede case -control undersøgelser (2015, 2019) baseret på data fra QResearch og Clinic Practice Research Datalink (CPRD) databaser. (2) Bioidentisk progesteron var ikke inkluderet, men vides ikke at være forbundet med nogen yderligere risiko i forhold til østrogen alene. Fodnoter: * = Statistisk signifikant ( p <0,01). Kilder : Se skabelon. | |||
Slag
Flere undersøgelser tyder på, at muligheden for HRT-relateret slagtilfælde er fraværende, hvis behandlingen startes inden for fem år efter overgangsalderen, og at foreningen er fraværende eller endda forebyggende, når den gives ad ikke-orale veje. Risikoen for iskæmisk slagtilfælde blev øget i løbet af interventionsperioden i WHI, uden nogen signifikant effekt efter behandlingens ophør og ingen forskel i dødelighed ved langvarig opfølgning. Når oral syntetisk østrogen eller kombineret østrogen-gestagen-behandling er forsinket til 5 år fra overgangsalderen, har kohorteundersøgelser hos svenske kvinder antydet en forbindelse med hæmoragisk og iskæmisk slagtilfælde . En anden stor kohorte af danske kvinder antydede, at den specifikke indgivelsesvej var vigtig og fandt ud af, at selvom oral østrogen øgede risikoen for slagtilfælde, havde absorptionen gennem huden ingen indvirkning, og vaginal østrogen havde faktisk en reduceret risiko.
Endometrial cancer

Hos postmenopausale kvinder reducerer kontinuerligt kombineret østrogen plus progestin forekomsten af endometriecancer. Varigheden af gestagenterapi bør være mindst 14 dage pr. Cyklus for at forhindre endometriel sygdom.
Endometrial cancer er blevet grupperet i to former i forbindelse med hormonudskiftning. Type 1 er den mest almindelige, kan være forbundet med østrogenbehandling og er normalt lav. Type 2 er ikke relateret til østrogenstimulering og normalt højere kvalitet og dårligere prognose. Den endometriehyperplasi at ledningerne til endometriecancer med østrogenterapi kan forhindres ved samtidig administration af progestogen . Den omfattende brug af højdosis østrogener til prævention i 1970'erne menes at have resulteret i en signifikant stigning i forekomsten af type 1 endometriecancer.
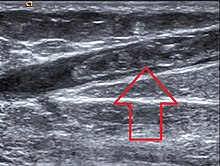
Paradoksalt nok fremmer progestogener væksten af livmoderfibroider , og en ultralyd i bækkenet kan udføres før HRT påbegyndes for at sikre, at der ikke er underliggende livmoder- eller endometrielæsioner.
Androgener stimulerer ikke endometrieproliferation hos postmenopausale kvinder og ser ud til at hæmme proliferationen induceret af østrogen i et vist omfang.
Der er ikke tilstrækkeligt bevis af høj kvalitet til at informere kvinder, der overvejer hormonbehandling, efter behandling for endometriecancer.
Brystkræft
Undersøgelser vedrørende sammenhæng mellem brystkræft og hormonudskiftning er inkonsekvente og varierer med udskiftningstype og tid siden overgangsalderen. Mens nogle evalueringer tyder på en øget risiko, reduceres den i andre. Denne inkonsekvens af effekt er blevet foreslået at indebære en mangel på meningsfuld indvirkning af HRT på brystkræftrisiko.
Der er en ikke-statistisk signifikant øget forekomst af brystkræft til hormonbehandling med syntetisk progesteron. Risikoen kan reduceres med bioidentisk progesteron, selvom den eneste prospektive undersøgelse, der antydede dette, var undermagt på grund af sjældenheden af brystkræft i kontrolpopulationen . Der har ikke været randomiserede kontrollerede forsøg til dato. Den relative risiko for brystkræft varierer også afhængigt af intervallet mellem overgangsalderen og HRT og vejen for syntetisk gestagenadministration.
Den seneste opfølgning af Women's Health Inititiative-deltagerne viste en lavere forekomst af brystkræft hos posthysterektomi-deltagere, der tog østrogen af heste alene, selvom den relative risiko var øget, hvis østrogen blev taget med medroxy-progesteron. Østrogen gives normalt kun alene i forbindelse med en hysterektomi på grund af virkningen af ubestemt østrogen på livmoderen.
HRT har været stærkere forbundet med risiko for brystkræft hos kvinder med lavere kropsmasseindeks (BMI'er). Der er ikke fundet nogen brystkræftforening med BMI'er på over 25. Nogle har foreslået, at fraværet af signifikant effekt i nogle af disse undersøgelser kan skyldes selektiv recept til overvægtige kvinder, der har en højere baseline -østron eller meget lavt progesteronserumniveauer efter oral administration, der fører til en høj tumorinaktiveringshastighed.
Evaluering af responsen af brystvævstæthed på HRT ved hjælp af mammografi ser ud til at hjælpe med at vurdere graden af brystkræftrisiko forbundet med terapi; kvinder med tæt eller blandet tæt brystvæv har en højere risiko for at udvikle brystkræft end dem med væv med lav densitet.
Mikroniseret progesteron ser ikke ud til at være forbundet med risiko for brystkræft, når det bruges i mindre end 5 år med begrænsede data, der tyder på en øget risiko, når det bruges i længere tid.
En retrospektiv Cox proportional hazards -analyse fra Richard Neapolitan godkendte den reducerede risiko for brystkræft med konjugeret brug af østrogenøst hestefoder, men antydede også, at konjugeret hesteøstrogen med medroxyprogesteronacetat var forbundet med en risikoreduktion i brystkræft, og at bioidentisk hormonbehandling ikke var forbundet med en statistisk signifikant effekt. Der har ikke været potentielle randomiserede kliniske forsøg, der sammenlignede de to indgivelsesveje med hensyn til brystkræft.
For kvinder, der tidligere har haft brystkræft, anbefales det først at overveje andre muligheder for menopausale virkninger, såsom bisphosphonater eller selektive østrogenreceptormodulatorer (SERM'er) til osteoporose, kolesterolsænkende midler og aspirin til hjerte-kar-sygdomme og vaginal østrogen for lokale symptomer. Observationsstudier af systemisk HRT efter brystkræft er generelt betryggende. Hvis HRT er nødvendig efter brystkræft, kan kun østrogenbehandling eller østrogenbehandling med et gestagen være sikrere muligheder end kombineret systemisk behandling. Hos kvinder, der er BRCA1- eller BRCA2 -mutationsbærere, synes HRT ikke at påvirke brystkræftrisikoen. Det relative antal kvinder, der bruger HRT, som også får regelmæssig screening -mammografi, er højere end hos kvinder, der ikke bruger HRT, en faktor, der er blevet foreslået at bidrage til forskellige brystkræftdetektionshastigheder i de to grupper.
Med androgenbehandling har prækliniske undersøgelser antydet en hæmmende effekt på brystvæv, selvom størstedelen af epidemiologiske undersøgelser tyder på en positiv sammenhæng.
| Terapi | <5 år | 5–14 år | 15+ år | |||
|---|---|---|---|---|---|---|
| Sager | RR (95% CI ) | Sager | RR (95% CI ) | Sager | RR (95% CI ) | |
| Østrogen alene | 1259 | 1,18 (1,10–1,26) | 4869 | 1,33 (1,28–1,37) | 2183 | 1,58 (1,51–1,67) |
| Ved østrogen | ||||||
| Konjugerede østrogener | 481 | 1,22 (1,09–1,35) | 1910 | 1,32 (1,25–1,39) | 1179 | 1,68 (1,57–1,80) |
| Estradiol | 346 | 1,20 (1,05–1,36) | 1580 | 1,38 (1,30–1,46) | 435 | 1,78 (1,58–1,99) |
| Estropipat (estronsulfat) | 9 | 1,45 (0,67–3,15) | 50 | 1,09 (0,79–1,51) | 28 | 1,53 (1,01–2,33) |
| Estriol | 15 | 1,21 (0,68–2,14) | 44 | 1,24 (0,89–1,73) | 9 | 1,41 (0,67–2,93) |
| Andre østrogener | 15 | 0,98 (0,46–2,09) | 21 | 0,98 (0,58–1,66) | 5 | 0,77 (0,27–2,21) |
| Efter rute | ||||||
| Orale østrogener | - | - | 3633 | 1,33 (1,27–1,38) | - | - |
| Transdermale østrogener | - | - | 919 | 1,35 (1,25–1,46) | - | - |
| Vaginale østrogener | - | - | 437 | 1,09 (0,97–1,23) | - | - |
| Østrogen og gestagen | 2419 | 1,58 (1,51–1,67) | 8319 | 2,08 (2,02–2,15) | 1424 | 2,51 (2,34–2,68) |
| Af gestagen | ||||||
| (Levo) norgestrel | 343 | 1,70 (1,49–1,94) | 1735 | 2,12 (1,99–2,25) | 219 | 2,69 (2,27–3,18) |
| Norethisteronacetat | 650 | 1,61 (1,46–1,77) | 2642 | 2,20 (2,09–2,32) | 420 | 2,97 (2,60–3,39) |
| Medroxyprogesteronacetat | 714 | 1,64 (1,50–1,79) | 2012 | 2,07 (1,96–2,19) | 411 | 2,71 (2,39–3,07) |
| Dydrogesteron | 65 | 1,21 (0,90–1,61) | 162 | 1,41 (1,17–1,71) | 26 | 2,23 (1,32–3,76) |
| Progesteron | 11 | 0,91 (0,47–1,78) | 38 | 2,05 (1,38–3,06) | 1 | - |
| Promegestone | 12 | 1,68 (0,85–3,31) | 19 | 2,06 (1,19–3,56) | 0 | - |
| Nomegestrolacetat | 8 | 1,60 (0,70–3,64) | 14 | 1,38 (0,75–2,53) | 0 | - |
| Andre gestagener | 12 | 1,70 (0,86–3,38) | 19 | 1,79 (1,05–3,05) | 0 | - |
| Efter progestogenfrekvens | ||||||
| Sammenhængende | - | - | 3948 | 2,30 (2,21–2,40) | - | - |
| Sporadisk | - | - | 3467 | 1,93 (1,84–2,01) | - | - |
| Progestogen alene | 98 | 1,37 (1,08–1,74) | 107 | 1,39 (1,11–1,75) | 30 | 2.10 (1.35–3.27) |
| Af gestagen | ||||||
| Medroxyprogesteronacetat | 28 | 1,68 (1,06–2,66) | 18 | 1,16 (0,68–1,98) | 7 | 3,42 (1,26–9,30) |
| Norethisteronacetat | 13 | 1,58 (0,77–3,24) | 24 | 1,55 (0,88–2,74) | 6 | 3,33 (0,81–13,8) |
| Dydrogesteron | 3 | 2,30 (0,49–10,9) | 11 | 3,31 (1,39–7,84) | 0 | - |
| Andre gestagener | 8 | 2,83 (1,04–7,68) | 5 | 1,47 (0,47–4,56) | 1 | - |
| Diverse | ||||||
| Tibolon | - | - | 680 | 1,57 (1,43–1,72) | - | - |
| Bemærkninger: Meta-analyse af verdensomspændende epidemiologiske beviser for menopausal hormonbehandling og brystkræftrisiko fra Collaborative Group on Hormonal Factors in Breast Cancer (CGHFBC). Fuldt justerede relative risici for nuværende versus aldrig-brugere af menopausal hormonbehandling. Kilde : Se skabelon. | ||||||
| Undersøgelse | Terapi | Hazard ratio (95% CI ) |
|---|---|---|
| E3N-EPIC: Fournier et al. (2005) | Østrogen alene | 1,1 (0,8–1,6) |
| Østrogen plus progesteron Transdermal østrogen Oralt østrogen |
0,9 (0,7–1,2) 0,9 (0,7–1,2) Ingen begivenheder |
|
| Østrogen plus progestin Transdermal østrogen Oralt østrogen |
1.4 (1.2–1.7) 1.4 (1.2–1.7) 1.5 (1.1–1.9) |
|
| E3N-EPIC: Fournier et al. (2008) | Oralt østrogen alene | 1,32 (0,76–2,29) |
| Oralt østrogen plus progestogen Progesteron Dydrogesteron Medrogestone Chlormadinonacetat Cyproteronacetat Promegestone Nomegestrolacetat Norethisteronacetat Medroxyprogesteronacetat |
Ikke analyseret en 0,77 (0,36–1,62) 2,74 (1,42–5,29) 2,02 (1,00–4,06) 2,57 (1,81–3,65) 1,62 (0,94–2,82) 1,10 (0,55–2,21) 2,11 (1,56–2,86) 1,48 (1,02–2,16) ) |
|
| Transdermal østrogen alene | 1,28 (0,98–1,69) | |
| Transdermal østrogen plus gestagen Progesteron Dydrogesteron Medrogestone Chlormadinonacetat Cyproteronacetat Promegestone Nomegestrolacetat Norethisteronacetat Medroxyprogesteronacetat |
1.08 (0.89-1.31) 1.18 (0.95-1.48) 2.03 (1.39-2.97) 1.48 (1.05-2.09) Ikke analyseret a 1.52 (1.19-1.96) 1.60 (1.28-2.01) Ikke analyseret a Ikke analyseret a |
|
| E3N-EPIC: Fournier et al. (2014) | Østrogen alene | 1,17 (0,99–1,38) |
| Østrogen plus progesteron eller dydrogesteron | 1,22 (1,11–1,35) | |
| Østrogen plus gestagen | 1,87 (1,71–2,04) | |
| CECILE: Cordina-Duverger et al. (2013) | Østrogen alene | 1,19 (0,69–2,04) |
| Østrogen-gestagen Progesteron Progestiner progesteronderivater Testosteron derivater |
1,33 (0,92–1,92) 0,80 (0,44–1,43) 1,72 (1,11–2,65) 1,57 (0,99–2,49) 3,35 (1,07–10,4) |
|
| Fodnoter: a = Ikke analyseret, færre end 5 tilfælde. Kilder : Se skabelon. | ||
| Undersøgelse | Terapi | Hazard ratio (95% CI ) |
|---|---|---|
| E3N-EPIC: Fournier et al. (2005) a | Transdermal østrogen plus progesteron <2 år 2-4 år ≥4 år |
0,9 (0,6–1,4) 0,7 (0,4–1,2) 1,2 (0,7–2,0) |
| Transdermal østrogen plus progestin <2 år 2-4 år ≥4 år |
1,6 (1,3–2,0) 1,4 (1,0–1,8) 1,2 (0,8–1,7) |
|
| Oralt østrogen plus progestin <2 år 2-4 år ≥4 år |
1,2 (0,9–1,8) 1,6 (1,1–2,3) 1,9 (1,2–3,2) |
|
| E3N-EPIC: Fournier et al. (2008) | Østrogen plus progesteron <2 år 2-4 år 4-6 år ≥6 år |
0,71 (0,44–1,14) 0,95 (0,67–1,36) 1,26 (0,87–1,82) 1,22 (0,89–1,67) |
| Østrogen plus dydrogesteron <2 år 2–4 år 4–6 år ≥6 år |
0,84 (0,51–1,38) 1,16 (0,79–1,71) 1,28 (0,83–1,99) 1,32 (0,93–1,86) |
|
| Østrogen plus andre gestagener <2 år 2–4 år 4–6 år ≥6 år |
1,36 (1,07–1,72) 1,59 (1,30–1,94) 1,79 (1,44–2,23) 1,95 (1,62–2,35) |
|
| E3N-EPIC: Fournier et al. (2014) | Østrogener plus progesteron eller dydrogesteron <5 år ≥5 år |
1,13 (0,99–1,29) 1,31 (1,15–1,48) |
| Østrogen plus andre gestagener <5 år ≥5 år |
1,70 (1,50–1,91) 2,02 (1,81–2,26) |
|
| Fodnoter: a = Oralt østrogen plus progesteron blev ikke analyseret, fordi der var et lavt antal kvinder, der brugte denne terapi. Kilder : Se skabelon. | ||
Livmoderhalskræft
HRT er forbundet med en øget risiko for kræft i æggestokkene , idet kvinder, der bruger HRT, har omkring et ekstra tilfælde af æggestokkræft pr. 1.000 brugere. Denne risiko formindskes, når gestagenbehandling gives samtidigt, i modsætning til østrogen alene, og falder også med stigende tid siden stop af HRT. Med hensyn til den specifikke undertype kan der være en højere risiko for serøs kræft , men ingen tilknytning til klare celler , endometrioid eller slimhindekræft i æggestokkene . Hormonbehandling hos overlevende kræft i æggestokkene efter kirurgisk fjernelse af æggestokkene menes generelt at forbedre overlevelsesraten.
Andre maligniteter
Kolorektal kræft
I WHI havde kvinder, der tog kombineret østrogen-progesteronbehandling, en lavere risiko for at få kolorektal cancer . Imidlertid var de kræftformer, de havde, mere tilbøjelige til at have spredt sig til lymfeknuder eller fjerne steder end tyktarmskræft hos kvinder, der ikke tog hormoner. Hos overlevende kolorektal kræft menes anvendelse af HRT at føre til lavere tilbagefaldsrisiko og generel dødelighed.
Livmoderhalskræft
Der ser ud til at være en signifikant reduceret risiko for cervikal squamoscellekræft hos postmenopausale kvinder behandlet med HRT og en svag stigning i adenocarcinom. Ingen undersøgelser har rapporteret en øget risiko for tilbagefald, når HRT bruges til overlevende af livmoderhalskræft.
Seksuel funktion
HRT kan hjælpe med manglen på seksuel lyst og seksuel dysfunktion, der kan opstå ved overgangsalderen. Epidemiologiske undersøgelser af kvinder mellem 40-69 år tyder på, at 75% af kvinderne forbliver seksuelt aktive efter overgangsalderen. Med stigende levetid lever kvinder i dag en tredjedel eller flere af deres liv i en postmenopausal tilstand, en periode hvor sund seksualitet kan være en integreret del af deres livskvalitet .
Nedsat libido og seksuel dysfunktion er almindelige problemer hos postmenopausale kvinder, en enhed henvist til hypoaktiv seksuel lystlidelse (HSDD); dets tegn og symptomer kan begge forbedres ved HRT. Flere hormonelle ændringer finder sted i løbet af denne periode, herunder et fald i østrogen og en stigning i follikelstimulerende hormon . For de fleste kvinder sker størstedelen af ændringen i de sene perimenopausale og postmenopausale faser. Fald i kønshormonbindende globulin (SHBG) og inhibin (A og B) forekommer også. Testosteron er til stede hos kvinder på et lavere niveau end mænd, når en højde på 30 år og falder gradvist med alderen; der er mindre variation under overgangsalderen i forhold til østrogen og progesteron.
En global erklæring om konsensusposition har oplyst, at postmenopausal testosteronerstatning til niveauer, der er omtrentlige premenopausale, kan være en effektiv behandling for HSDD. Sikkerhedsoplysninger til testosteronbehandling er ikke tilgængelige efter 2 års kontinuerlig behandling, men dosering over fysiologiske niveauer frarådes. Testosteronplaster har vist sig at genoprette seksuel lyst hos postmenopausale kvinder. Der er ikke tilstrækkelige data til at evaluere virkningen af testosteronerstatning på hjertesygdomme, brystkræft, idet de fleste forsøg har omfattet kvinder, der tager samtidig østrogen og progesteron, og med testosteronbehandling i sig selv af relativt kort varighed. I indstillingen af disse begrænsede data har testosteronbehandling ikke været forbundet med bivirkninger.
Ikke alle kvinder er lydhøre, især dem med allerede eksisterende seksuelle vanskeligheder. Østrogenudskiftning kan genoprette vaginale celler, pH -niveauer og blodgennemstrømning til skeden, som alle har en tendens til at forringes ved begyndelsen af overgangsalderen. Smerter eller ubehag ved sex ser ud til at være den mest lydhøre komponent over for østrogen. Det har også vist sig at have positive virkninger på urinvejene. Østrogen kan også reducere vaginal atrofi og øge seksuel ophidselse , hyppighed og orgasme .
Effekten af hormonudskiftning kan falde hos nogle kvinder efter lang tids brug. En række undersøgelser har også fundet ud af, at de kombinerede virkninger af østrogen/androgenerstatningsterapi kan øge libido og ophidselse over østrogen alene. Tibolone , et syntetisk steroid med østrogene, androgene og progestogene egenskaber, der er tilgængelig i Europa, har evnen til at forbedre humør, libido og fysisk symptomatologi. I forskellige placebokontrollerede undersøgelser er der set forbedringer i vasomotoriske symptomer, følelsesmæssig respons, søvnforstyrrelser, fysiske symptomer og seksuel lyst, selvom det også har en lignende risikoprofil som konventionel HRT.
Neurodegenerative lidelser
For forebyggelse foreslog WHI, at HRT kan øge risikoen for demens, hvis det påbegyndes efter 65 år, men har et neutralt resultat eller er neurobeskyttende for personer mellem 50-55 år. Andre undersøgelser i perimenopause har vist, at HRT konsekvent er forbundet med en lavere risiko for Alzheimers. Med Parkinsons er der en konsekvent mekanisme inden for grundvidenskab, der tyder på en beskyttende virkning, selvom kliniske og epidemiologiske undersøgelser viser, at de ikke har vist nogen sammenhæng eller utydelige resultater. En dansk undersøgelse antydede imidlertid en øget risiko for Parkinson med HRT, selvom dette kun var statistisk signifikant i cykliske doseringsplaner.
Med hensyn til behandling har randomiserede forsøg vist, at HRT forbedrer ledelses- og opmærksomhedsprocesser uden for demenssammenhæng hos postmenopausale kvinder, både hos dem, der er asymptomatiske og dem med let kognitiv svækkelse. Østrogenudskiftning ser ud til at forbedre motoriske symptomer og dagligdagens aktiviteter hos postmenopausale kvinder med Parkinsons, med betydelig forbedring af UPDRS -score . Kliniske forsøg har også vist, at testosteronerstatning er forbundet med små statistisk signifikante forbedringer i verbal læring og hukommelse hos postmenopausale kvinder. DHEA har ikke vist sig at forbedre den kognitive præstation efter overgangsalderen. Prækliniske undersøgelser indikerer, at endogent østrogen og testosteron er neurobeskyttende og kan forhindre amyloidaflejring i hjernen.
Muskel og knogle
Der er et stort fald i risikoen for hoftebrud under behandlingen; dette vedvarer, efter at HRT er stoppet, dog i mindre grad. Det hjælper også kollagendannelse , hvilket igen forbedrer intervertebral disk og knoglestyrke.
Hormonerstatningsterapi i form af østrogen og androgen kan være effektiv til at vende virkningerne af aldring på muskler. Lavere testosteron er forbundet med lavere knogletæthed og højere fri testosteron er forbundet med lavere hoftebrudshastigheder hos ældre kvinder. Testosteronbehandling, som kan bruges til nedsat seksuel funktion, kan også øge knoglemineraltætheden og muskelmassen.
Bivirkninger
Bivirkninger ved HRT forekommer med varierende hyppighed og omfatter:
almindelige
- Hovedpine
- Forstyrret mave , mavekramper eller oppustethed
- Diarré
- Appetit og vægtændringer
- Ændringer i kønsdrift eller ydeevne
- Nervøsitet
- Brune eller sorte pletter på huden
- Acne
- Hævelse af hænder, fødder eller underben på grund af væskeretention
- Ændringer i menstruationsstrømmen
- Bryst ømhed, forstørrelse eller udflåd
- Pludselig svært ved at bære kontaktlinser
Ualmindelig
- Dobbelt syn
- Alvorlige mavesmerter
- Gulfarvning af hud eller øjne
- Alvorlig depression
- Usædvanlig blødning
- Mistet appetiten
- Udslæt
- Lathed
- Feber
- Mørk urin
- Lys farvet skammel
- Chorea
Kontraindikationer
Følgende er absolutte og relative kontraindikationer til HRT:
Absolutte kontraindikationer
- Udiagnosticeret vaginal blødning
- Alvorlig leversygdom
- Graviditet
- Alvorlig kranspulsår
- Aggressiv bryst- , livmoder- eller æggestokkræft
Relative kontraindikationer
- Migræne hovedpine
- Brystkræftens historie
- Ovariecancer -historie
- Venøs trombose
- Livmoderfibroids historie
- Atypisk ductal hyperplasi af bryst
- Aktiv galdeblæresygdom ( cholangitis , cholecystitis )
- Godt differentieret og tidlig livmoderhalskræft - når behandlingen af maligniteten er fuldført, er ikke længere en absolut kontraindikation.
Historie og forskning
Ekstraktionen af CEE'er fra urinen fra gravide hopper førte til markedsføring i 1942 af Premarin , en af de tidligere former for østrogen, der skulle indføres. Fra den tid og frem til midten af 1970'erne blev østrogen administreret uden et supplerende gestagen. Fra 1975 begyndte undersøgelser at vise, at uden progestogen resulterede ubestemt østrogenbehandling med Premarin i en 8-fold øget risiko for endometriecancer , hvilket til sidst fik salget af Premarin til at styrte sammen. Det blev anerkendt i begyndelsen af 1980'erne, at tilsætning af et gestagen til østrogen reducerede denne risiko for endometriet. Dette førte til udviklingen af kombineret østrogen -gestagen -behandling, oftest med en kombination af konjugeret østrogen fra heste (Premarin) og medroxyprogesteron (Provera).
Forsøg
Women's Health Initiative-forsøgene blev udført mellem 1991 og 2006 og var de første store, dobbeltblinde , placebokontrollerede kliniske forsøg med HRT hos raske kvinder. Deres resultater var både positive og negative, hvilket tyder på, at der i løbet af selve hormonbehandlingen er stigninger i invasiv brystkræft , slagtilfælde og lungekoagler . Andre risici omfatter øget livmoderhalskræft , galdeblæresygdom og urininkontinens , mens fordelene omfatter nedsat hoftebrud , nedsat forekomst af diabetes og forbedring af vasomotoriske symptomer. Der er også en øget risiko for demens med HRT hos kvinder over 65 år, selvom det i yngre aldre ser ud til at være neurobeskyttende. Efter ophør af HRT fortsatte WHI med at observere sine deltagere og fandt ud af, at de fleste af disse risici og fordele forsvandt, selvom en vis stigning i risikoen for brystkræft fortsatte. Andre undersøgelser har også antydet en øget risiko for kræft i æggestokkene .
WHI -armen, der modtog kombineret østrogen- og gestagenterapi, blev lukket for tidligt i 2002 af dets dataovervågningsudvalg (DMC) på grund af opfattede sundhedsrisici, selvom dette skete et helt år efter, at dataene tyder på øget risiko blev manifesteret. I 2004 blev armen af WHI, hvor patienter efter hysterektomi blev behandlet med østrogen alene, også lukket af DMC. Klinisk medicinsk praksis ændret baseret på to parallelle Women's Health Initiative (WHI) undersøgelser af HRT. Tidligere undersøgelser var mindre, og mange var af kvinder, der elektivt tog hormonbehandling. En del af de parallelle undersøgelser fulgte over 16.000 kvinder i gennemsnit 5,2 år, hvoraf halvdelen tog placebo , mens den anden halvdel tog en kombination af CEE'er og MPA (Prempro). Dette WHI-østrogen-plus-gestagen-forsøg blev standset for tidligt i 2002, fordi foreløbige resultater antydede risici ved kombinerede CEE'er og gestagen oversteg deres fordele. Den første rapport om det standserede WHI-østrogen-plus-gestagen-studie udkom i juli 2002.
Indledende data fra WHI i 2002 foreslog, at dødeligheden var lavere, da HRT blev påbegyndt tidligere, mellem 50 til 59 år, men højere, når den begyndte efter 60 år. Hos ældre patienter var der en tilsyneladende øget forekomst af brystkræft , hjerteanfald , venøs trombose og slagtilfælde , selvom en reduceret forekomst af kolorektal cancer og knoglebrud . På det tidspunkt anbefalede WHI, at kvinder med ikke-kirurgisk overgangsalder tog den lavest mulige dosis HRT i den kortest mulige tid for at minimere de dermed forbundne risici. Nogle af WHI -fundene blev igen fundet i en større national undersøgelse foretaget i Det Forenede Kongerige , kendt som Million Women Study (MWS). Som et resultat af disse fund faldt antallet af kvinder, der tog HRT, voldsomt. I 2012 konkluderede United States Preventive Task Force (USPSTF), at de skadelige virkninger af kombineret østrogen- og progestinbehandling sandsynligvis oversteg deres fordele ved kronisk sygdomsforebyggelse.
I 2002, da den første WHI -opfølgende undersøgelse blev offentliggjort med HRT hos postmenopausale kvinder, havde både ældre og yngre aldersgrupper en lidt højere forekomst af brystkræft , og både hjerteanfald og slagtilfælde var øget hos ældre patienter, dog ikke hos yngre deltagere. Brystkræft var øget hos kvinder behandlet med østrogen og et gestagen, men ikke med østrogen og progesteron eller østrogen alene. Behandling med østrogen uden modstand (dvs. et østrogen alene uden gestagen) er kontraindiceret, hvis livmoderen stadig er til stede på grund af dets proliferative virkning på endometriet . WHI fandt også en reduceret forekomst af kolorektal cancer, når østrogen og et gestagen blev brugt sammen, og vigtigst af alt, en reduceret forekomst af knoglebrud. I sidste ende fandt undersøgelsen forskellige resultater for alle årsager til dødelighed med HRT og fandt, at det var lavere, når HRT blev påbegyndt i alderen 50–59 år, men højere, når det begyndte efter 60 år. Forfatterne af undersøgelsen anbefalede kvinder med ikke-kirurgisk overgangsalder tage den lavest mulige dosis hormoner i den korteste tid for at minimere risikoen.
Data offentliggjort af WHI foreslog supplerende østrogen øget risiko for venøs tromboembolisme og brystkræft, men var beskyttende mod osteoporose og tyktarmskræft , mens virkningen på hjerte -kar -sygdomme var blandet. Disse resultater blev senere understøttet i forsøg fra Det Forenede Kongerige, men ikke i nyere undersøgelser fra Frankrig og Kina. Genetisk polymorfisme synes at være forbundet med interindividuel variation i metabolisk respons på HRT hos postmenopausale kvinder.
| Klinisk resultat | Hypoteset effekt på risiko |
Østrogen og gestagen ( CE'er 0,625 mg/dag po + MPA 2,5 mg/dag po) (n = 16,608, med livmoder, 5,2–5,6 års opfølgning) |
Østrogen alene ( CE'er 0,625 mg/dag po) (n = 10,739, ingen livmoder, 6,8-7,1 års opfølgning) |
||||
|---|---|---|---|---|---|---|---|
| HR | 95% CI | AR | HR | 95% CI | AR | ||
| Koronar hjertesygdom | Er faldet | 1,24 | 1,00–1,54 | +6 / 10.000 PY'er | 0,95 | 0,79–1,15 | −3 / 10.000 PY'er |
| Slag | Er faldet | 1,31 | 1,02–1,68 | +8 / 10.000 PY'er | 1,37 | 1,09–1,73 | +12 / 10.000 PY'er |
| Lungeemboli | Øget | 2.13 | 1.45–3.11 | +10 / 10.000 PY'er | 1,37 | 0,90–2,07 | +4 / 10.000 PY'er |
| Venøs tromboemboli | Øget | 2.06 | 1,57–2,70 | +18 / 10.000 PY'er | 1,32 | 0,99–1,75 | +8 / 10.000 PY'er |
| Brystkræft | Øget | 1,24 | 1,02–1,50 | +8 / 10.000 PY'er | 0,80 | 0,62–1,04 | −6 / 10.000 PY'er |
| Kolorektal kræft | Er faldet | 0,56 | 0,38–0,81 | −7 / 10.000 PY'er | 1,08 | 0,75–1,55 | +1 / 10.000 PY'er |
| Endometrial cancer | - | 0,81 | 0,48–1,36 | −1 / 10.000 PY'er | - | - | - |
| Hoftebrud | Er faldet | 0,67 | 0,47–0,96 | −5 / 10.000 PY'er | 0,65 | 0,45–0,94 | −7 / 10.000 PY'er |
| Samlede brud | Er faldet | 0,76 | 0,69–0,83 | −47 / 10.000 PY'er | 0,71 | 0,64–0,80 | −53 / 10.000 PY'er |
| Total dødelighed | Er faldet | 0,98 | 0,82–1,18 | −1 / 10.000 PY'er | 1.04 | 0,91–1,12 | +3 / 10.000 PY'er |
| Globalt indeks | - | 1.15 | 1.03–1.28 | +19 / 10.000 PY'er | 1,01 | 1.09–1.12 | +2 / 10.000 PY'er |
| Diabetes | - | 0,79 | 0,67–0,93 | 0,88 | 0,77–1,01 | ||
| Galdeblære sygdom | Øget | 1,59 | 1,28–1,97 | 1,67 | 1.35–2.06 | ||
| Stressinkontinens | - | 1,87 | 1.61–2.18 | 2.15 | 1,77–2,82 | ||
| Opfordre til inkontinens | - | 1.15 | 0,99–1,34 | 1,32 | 1.10–1.58 | ||
| Perifer arteriesygdom | - | 0,89 | 0,63–1,25 | 1,32 | 0,99–1,77 | ||
| Formentlig demens | Er faldet | 2,05 | 1.21–3.48 | 1,49 | 0,83–2,66 | ||
| Forkortelser: CE'er = konjugerede østrogener . MPA = medroxyprogesteronacetat . po = per mundtlig . HR = fareforhold . AR = risiko, der kan tilskrives . PY = personår . CI = konfidensinterval . Bemærkninger: Prøvestørrelser (n) inkluderer placebo -modtagere, som var omkring halvdelen af patienterne. "Globalt indeks" defineres for hver kvinde som tidspunktet for tidligste diagnose for koronar hjertesygdom , slagtilfælde , lungeemboli , brystkræft , tyktarmskræft , endometriecancer (kun østrogen plus progestogruppe), hoftebrud og død af andre årsager. Kilder: Se skabelon. | |||||||
WHI rapporterede statistisk signifikante stigninger i brystkræft , koronar hjertesygdom , slagtilfælde og lungeemboli . Undersøgelsen fandt også statistisk signifikante fald i satserne for hoftebrud og tarmkræft . "Et år efter undersøgelsen blev stoppet i 2002, blev der offentliggjort en artikel, der angiver, at østrogen plus progestin også øger risikoen for demens." Konklusionen af undersøgelsen var, at HRT -kombinationen udgjorde risici, der opvejer de målte fordele. Resultaterne blev næsten universelt rapporteret som risici og problemer forbundet med HRT generelt, snarere end med Prempro, den specifikke patenterede kombination af CEE'er og MPA undersøgt.
Efter at den øgede koagulation, der blev fundet i de første WHI -resultater, blev rapporteret i 2002, reducerede antallet af fyldte Prempro -recepter med næsten halvdelen. Efter WHI -resultaterne fravalgte en stor procentdel af HRT -brugere dem, hvilket hurtigt blev efterfulgt af et kraftigt fald i brystkræftraten. Faldet i brystkræft er fortsat i de efterfølgende år. Et ukendt antal kvinder begyndte at tage alternativer til Prempro, såsom sammensatte bioidentiske hormoner, selvom forskere har hævdet, at sammensatte hormoner ikke er væsentligt forskellige fra konventionel hormonbehandling.
Den anden del af de parallelle undersøgelser omfattede kvinder, der var efter hysterektomi og derfor modtog enten placebo -gestagen eller CEE'er alene. Denne gruppe viste ikke de risici, der blev demonstreret i kombinationshormonundersøgelsen, og undersøgelsen, der kun var østrogen, blev ikke standset i 2002. Men i februar 2004 blev den også standset. Selvom der var en 23% reduceret forekomst af brystkræft hos deltagerne i østrogen-undersøgelsen, blev risikoen for slagtilfælde og lungeemboli øget let, hovedsageligt hos patienter, der begyndte HRT over 60 år.
Flere andre store undersøgelser og metaanalyser har rapporteret reduceret dødelighed for HRT hos kvinder yngre end 60 år eller inden for 10 år efter overgangsalderen og en diskutabel eller fraværende effekt på dødeligheden hos kvinder over 60 år.
Selvom forskning hidtil har været betydelig, er der behov for yderligere undersøgelser for fuldt ud at forstå forskelle i virkning for forskellige typer HRT og tidsrum siden overgangsalderen.
Tilgængelige formularer
Der er fem store humane steroidhormoner: østrogener, gestagener, androgener , mineralokortikoider og glukokortikoider . Østrogener og gestagener er de to, der oftest bruges i overgangsalderen. De fås i en lang række forskellige FDA-godkendte og ikke-FDA-godkendte formuleringer.
Hos kvinder med intakte livmoder gives østrogener næsten altid i kombination med gestagener, da langvarig ubestemt østrogenbehandling er forbundet med en markant øget risiko for endometrial hyperplasi og endometriecancer . Omvendt, hos kvinder, der har gennemgået en hysterektomi eller ikke har en livmoder, kræves der ikke et gestagen, og østrogen kan bruges alene. Der er mange kombinerede formuleringer, der omfatter både østrogen og gestagen.
Specifikke former for hormonerstatning omfatter:
- Østrogener - bioidentiske østrogener som østradiol og østriol , animalsk afledte østrogener som konjugerede østrogener (CEE'er) og syntetiske østrogener som ethinylestradiol
- Progestogener - bioidentisk progesteron og progestiner (syntetiske gestagener) som medroxyprogesteronacetat (MPA), norethisteron og dydrogesteron
- Androgener - bioidentisk testosteron og dehydroepiandrosteron (DHEA) og syntetiske anabolske steroider som methyltestosteron og nandrolon decanoat
Tibolone - en syntetisk medicin tilgængelig i Europa, men ikke USA - er mere effektiv end placebo, men mindre effektiv end kombinationshormonbehandling hos postmenopausale kvinder. Det kan have en reduceret risiko for bryst- og kolorektal cancer, selvom det omvendt kan være forbundet med vaginal blødning, endometriecancer og øge risikoen for slagtilfælde hos kvinder over 60 år.
Vaginal østrogen kan forbedre lokal atrofi og tørhed med færre systemiske virkninger end østrogener leveret af andre ruter. Nogle gange kan et androgen, generelt testosteron, tilføjes til behandling af nedsat libido .
Kontinuerlig kontra cyklisk
Dosering varieres ofte cyklisk for mere at efterligne ovariehormoncyklussen, idet østrogener tages dagligt og gestagener tages i cirka to uger hver måned eller hver anden måned, en tidsplan kaldet 'cyklisk' eller 'sekventielt kombineret'. Alternativt kan 'kontinuerlig kombineret' HRT gives med en konstant daglig hormondosis. Kontinuerlig kombineret HRT er forbundet med mindre kompleks endometriehyperplasi end cyklisk. Virkningen på brysttætheden ser ud til at være ens i begge behandlingstider.
| Rute/form | Østrogen | Lav | Standard | Høj | |||
|---|---|---|---|---|---|---|---|
| Mundtlig | Estradiol | 0,5-1 mg/dag | 1-2 mg/dag | 2-4 mg/dag | |||
| Estradiol valerat | 0,5-1 mg/dag | 1-2 mg/dag | 2-4 mg/dag | ||||
| Estradiolacetat | 0,45-0,9 mg/dag | 0,9-1,8 mg/dag | 1,8–3,6 mg/dag | ||||
| Konjugerede østrogener | 0,3-0,45 mg/dag | 0,625 mg/dag | 0,9-1,25 mg/dag | ||||
| Forstærkede østrogener | 0,3-0,45 mg/dag | 0,625 mg/dag | 0,9-1,25 mg/dag | ||||
| Estropipat | 0,75 mg/dag | 1,5 mg/dag | 3 mg/dag | ||||
| Estriol | 1-2 mg/dag | 2-4 mg/dag | 4-8 mg/dag | ||||
| Ethinylestradiol a | 2,5 μg/dag | 5–15 μg/dag | - | ||||
| Næsespray | Estradiol | 150 μg/dag | 300 μg/dag | 600 μg/dag | |||
| Transdermal plaster | Estradiol | 25 μg/dag b | 50 μg/dag b | 100 μg/dag b | |||
| Transdermal gel | Estradiol | 0,5 mg/dag | 1–1,5 mg/dag | 2-3 mg/dag | |||
| Vaginal | Estradiol | 25 μg/dag | - | - | |||
| Estriol | 30 μg/dag | 0,5 mg 2x/uge | 0,5 mg/dag | ||||
| IM eller SC injektion | Estradiol valerat | - | - | 4 mg 1x/4 uger | |||
| Estradiol cypionat | 1 mg 1x/3-4 uger | 3 mg 1x/3-4 uger | 5 mg 1x/3-4 uger | ||||
| Estradiolbenzoat | 0,5 mg 1x/uge | 1 mg 1x/uge | 1,5 mg 1x/uge | ||||
| SC -implantat | Estradiol | 25 mg 1x/6 måneder | 50 mg 1x/6 måneder | 100 mg 1x/6 måneder | |||
| Fodnoter: a = Ikke længere brugt eller anbefalet på grund af sundhedsmæssige bekymringer. b = Som et enkelt plaster påført en eller to gange om ugen (brugt i 3-4 dage eller 7 dage), afhængigt af formuleringen. Bemærk: Doser er ikke nødvendigvis ækvivalente. Kilder: Se skabelon. | |||||||
Administrationsvej
De lægemidler, der anvendes i overgangsalderen HRT, fås i mange forskellige formuleringer til brug på en række forskellige indgivelsesveje :
- Oral administration - tabletter , kapsler
- Transdermal administration - plastre , geler , cremer
- Vaginal administration - tabletter, cremer, stikpiller , ringe
- Intramuskulær eller subkutan injektion - opløsninger i hætteglas eller ampuller
- Subkutant implantat - kirurgisk indsatte pellets placeret i fedtvæv
- Mindre almindeligt sublingual , bukkal , intranasal og rektal administration samt intrauterine enheder
Nyere udviklede former for medicinlevering påstås at have øget lokal effekt lavere dosering, færre bivirkninger og konstante snarere end cykliske serumhormonniveauer. Transdermal og transvaginal østrogen undgår især metabolisme ved første gennemgang gennem leveren. Dette forhindrer igen en stigning i koagulationsfaktorer og akkumulering af antiøstrogene metabolitter, hvilket resulterer i færre negative bivirkninger, især med hensyn til hjerte-kar-sygdomme og slagtilfælde.
Bioidentisk hormonbehandling
Bioidentisk hormonbehandling (BHT) er brugen af hormoner, der er kemisk identiske med dem, der produceres i kroppen. Selvom tilhængere af BHT hævder fordele frem for ikke-bioidentisk eller konventionel hormonbehandling, genkender FDA ikke udtrykket 'bioidentisk hormon', idet der står, at der ikke er videnskabeligt bevis for, at disse hormoner er identiske med deres naturligt forekommende modparter. Der er imidlertid FDA -godkendte produkter, der indeholder hormoner klassificeret som 'bioidentisk'.
Bioidentiske hormoner kan bruges i enten farmaceutiske eller sammensatte præparater, hvor sidstnævnte generelt ikke anbefales af tilsynsmyndigheder på grund af deres mangel på standardisering og lovgivningsmæssigt tilsyn. De fleste klassifikationer af bioidentiske hormoner tager ikke højde for produkternes fremstilling, kilde eller leveringsmetode, og beskriver derfor både ikke-FDA-godkendte sammensatte produkter og FDA-godkendte lægemidler som 'bioidentiske'. Den britiske Menopause Society har udsendt en konsensus erklæring støtter sondringen mellem "sammensat" former (cBHRT), der beskrives som ureguleret, specialfremstillede af specialkemikalier apoteker og underlagt tunge markedsføring og "regulerede" farmaceutisk kvalitet formularer (rBHRT), der undergår formelle tilsyn af enheder som FDA og danner grundlaget for de fleste kliniske forsøg. Nogle praktiserende læger anbefaler, at sammensat bioidentisk HRT også anvender spyt- eller serumhormonaltest til at overvåge respons på terapi, en praksis, der ikke er godkendt af de nuværende kliniske retningslinjer i USA og Europa.
Bioidentiske hormoner i lægemidler kan have meget begrænsede kliniske data, uden hidtil randomiserede kontrollerede prospektive forsøg, der sammenligner dem med deres dyreafledte modstykker. Nogle prækliniske data har antydet en reduceret risiko for venøs tromboemboli , hjerte-kar-sygdomme og brystkræft . Fra 2012 godkendte retningslinjer fra North American Menopause Society , Endocrine Society , International Menopause Society og European Menopause and Andropause Society den reducerede risiko for bioidentiske lægemidler for dem med øget koagulationsrisiko.
En retrospektiv Cox -proportionalrisikoanalyse har antydet, at konjugeret hesteøstrogen og medroxyprogesteronacetat er forbundet med en risikoreduktion i brystkræft, mens bioidentisk hormonbehandling er forbundet med en lidt øget risiko.
Sammensætning
Sammensætning til HRT frarådes generelt af FDA og medicinsk industri i USA på grund af mangel på regulering og standardiseret dosering. Den amerikanske kongres indrømmede FDA eksplicit, men begrænset tilsyn med sammensatte lægemidler i en ændring af Federal Food, Drug and Cosmetic Act (FDCA) fra 1997 , men de har stødt på forhindringer i denne rolle siden dengang. Efter 64 patientdødsfald og 750 skadede patienter fra et udbrud af meningitis i 2012 på grund af forurenede steroidinjektioner, vedtog kongressen 2013 Drug Quality and Security Act , der godkendte oprettelse af FDA af en frivillig registrering for faciliteter, der fremstillede sammensatte lægemidler, og forstærkede FDCA -regler for traditionel sammensætning. DQSA og dens forstærkning af bestemmelse §503A i FDCA størkner FDA -myndigheden til at håndhæve FDCA -regulering mod sammensætninger af bioidentisk hormonbehandling.
I Det Forenede Kongerige på den anden side er sammensætning en reguleret aktivitet. Den medicin og sundhedsprodukter Regulatory Agency regulerer Sammenblandingen udføres under en Manufacturing Specials licens og General Pharmaceutical Råd regulerer Sammenblandingen udføres inden et apotek. Alt testosteron, der er foreskrevet i Det Forenede Kongerige, er bioidentisk, og dets anvendelse understøttes af National Health Service . Der er også markedsføringstilladelse for mandlige testosteronprodukter. National Institute for Health and Care Excellence guideline 1.4.8 siger: "overvej testosterontilskud til kvinder i overgangsalderen med lavt seksuelt begær, hvis HRT alene ikke er effektivt". Fodnoten tilføjer: "på tidspunktet for offentliggørelsen (november 2015) havde testosteron ikke en britisk markedsføringstilladelse for denne indikation hos kvinder. Bio-identisk progesteron bruges til IVF-behandling og til gravide kvinder, der er i risiko for for tidlig fødsel . "
Samfund og offentlig opfattelse
Wyeth kontrovers
Wyeth , nu et datterselskab af Pfizer , var et farmaceutisk selskab, der markedsførte HRT -produkterne Premarin (CEE'er) og Prempro (CEE'er + MPA). I 2009 resulterede retssager vedrørende Wyeth i frigivelse af 1.500 dokumenter, der afslørede praksis vedrørende reklame for disse lægemidler. Dokumenterne viste, at Wyeth bestilte snesevis af spøgelsesskrevne anmeldelser og kommentarer, der blev offentliggjort i medicinske tidsskrifter for at fremme udokumenterede fordele ved dets HRT -produkter, nedtone deres skader og risici og kaste konkurrerende behandlinger i et negativt lys. Fra midten af 1990'erne og fortsatte i over et årti, forfulgte Wyeth en aggressiv "publikationsplan" -strategi for at promovere sine HRT-produkter ved hjælp af spøgelsesskrevne publikationer. Det arbejdede hovedsageligt med DesignWrite, et medicinsk skrivefirma. Mellem 1998 og 2005 havde Wyeth 26 artikler om sine HRT -produkter, der blev offentliggjort i videnskabelige tidsskrifter.
Disse gunstige publikationer understregede fordelene og bagatelliserede risiciene ved dets HRT -produkter, især den "misforståelse", der er forbundet med dets produkter med brystkræft. Publikationerne forsvarede ikke-understøttede kardiovaskulære "fordele" ved sine produkter, nedtonede risici som brystkræft og fremmede off-label og uprøvede anvendelser som forebyggelse af demens, Parkinsons sygdom , synsproblemer og rynker . Derudover understregede Wyeth negative beskeder mod SERM raloxifen for osteoporose, instruerede forfattere til at understrege det faktum, at "alternative behandlingsformer er steget i brug siden WHI, selvom der ikke er meget tegn på, at de er effektive eller sikre ...", kaldet til sætter spørgsmålstegn ved kvaliteten og terapeutisk ækvivalens af godkendte generiske CEE -produkter og bestræbte sig på at sprede forestillingen om, at de unikke risici ved CEE'er og MPA var en klasseeffekt af alle former for menopausal HRT: "Samlet set tyder disse data på, at fordel/risiko -analysen der blev rapporteret i Women's Health Initiative kan generaliseres til alle postmenopausale hormonerstatningsprodukter. "
Efter offentliggørelsen af WHI -dataene i 2002 faldt aktiekurserne for medicinalindustrien, og et stort antal kvinder stoppede med at bruge HRT. Lagrene i Wyeth, der leverede Premarin og Prempro, der blev brugt i WHI -forsøgene, faldt med mere end 50%og blev aldrig helt genoprettet. Nogle af deres artikler som svar fremmede temaer som følgende: "WHI var fejlbehæftet; WHI var et kontroversielt forsøg; befolkningen undersøgt i WHI var upassende eller var ikke repræsentativ for den generelle befolkning af kvinder i overgangsalderen; resultater af kliniske forsøg bør ikke vejlede behandling for enkeltpersoner; observationsstudier er lige så gode som eller bedre end randomiserede kliniske forsøg; dyreforsøg kan vejlede i klinisk beslutningstagning; risiciene forbundet med hormonbehandling er blevet overdrevne; fordelene ved hormonbehandling er blevet eller vil blive bevist , og de seneste undersøgelser er en afvigelse. " Lignende fund blev observeret i en analyse fra 2010 af 114 lederartikler, anmeldelser, retningslinjer og breve fra fem branchebetalte forfattere. Disse publikationer promoverede positive temaer og udfordrede og kritiserede ugunstige forsøg som WHI og MWS. I 2009 blev Wyeth opkøbt af Pfizer i en aftale til en værdi af 68 milliarder dollars. Pfizer, et firma, der producerer Provera og Depo-Provera (MPA) og også har beskæftiget sig med medicinsk ghostwriting, fortsætter med at markedsføre Premarin og Prempro, som fortsat er bedst sælgende medicin.
Ifølge Fugh-Berman (2010), "trods endelige videnskabelige data om det modsatte, tror mange gynækologer stadig, at fordelene ved [HRT] opvejer risiciene hos asymptomatiske kvinder. Denne ikke-evidensbaserede opfattelse kan være et resultat af årtiers omhyggeligt orkestreret virksomhedsindflydelse på medicinsk litteratur. " Hele 50% af lægerne har udtrykt skepsis over for store forsøg som WHI og HERS. De positive opfattelser af mange læger af HRT på trods af store forsøg, der viser risici, der potentielt opvejer eventuelle fordele, kan skyldes indsatsen fra lægemiddelvirksomheder som Wyeth.
Popularitet
1990'erne viste et dramatisk fald i receptpligtigesatser, selvom de for nylig er begyndt at stige igen. Transdermal terapi, delvis på grund af dets manglende stigning i venøs tromboemboli, er nu ofte førstevalget for HRT i Storbritannien . Konjugat heste østrogen har i sondring en potentielt højere risiko for trombose og bruges nu ikke almindeligt i Storbritannien, erstattet af østradiolbaserede forbindelser med lavere tromboserisiko. Orale progestogenkombinationer, såsom medroxyprogesteronacetat, er ændret til dyhydrogesteron på grund af manglende tilknytning af sidstnævnte til venprop.
Noter
Referencer
eksterne links
- Overgangsalderbehandling , Hormonsundhedsnetværk, The Endocrine Society
- Seksuel sundhed og overgangsalder online , The North American Menopause Society
- Overgangsalder , US Food and Drug Administration



