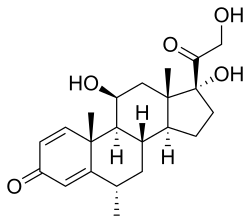
Methylprednisolon - Methylprednisolone
 | |
 | |
| Kliniske data | |
|---|---|
| Handelsnavne | Medrol, Depo-Medrol (som acetat ), Solu-Medrol (som succinat ), andre |
| Andre navne | 6α-methylprednisolon; 11β, 17,21-trihydroxy-6α-methyl-δ 1- progesteron; 11β, 17,21-Trihydroxy-6α-methylpregna-1,4-dien-3,20-dion |
| AHFS / Drugs.com | Monografi |
| MedlinePlus | a682795 |
| Licensdata | |
| Graviditet kategori |
|
| Ruter for administration |
Ved mund , IM (som acetat ), IA (som acetat ), IV (som succinat , suleptanat ) |
| ATC -kode | |
| Lovlig status | |
| Lovlig status | |
| Farmakokinetiske data | |
| Proteinbinding | 78% |
| Metabolisme | Lever primært, nyre , væv ; CYP3A4 |
| Eliminering halveringstid | 18-26 timer |
| Udskillelse | Urin |
| Identifikatorer | |
| |
| CAS -nummer | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| CHEMBL | |
| CompTox Dashboard ( EPA ) | |
| ECHA InfoCard |
100.001.343 |
| Kemiske og fysiske data | |
| Formel | C 22 H 30 O 5 |
| Molar masse | 374,477 g · mol −1 |
| 3D -model ( JSmol ) | |
| Smeltepunkt | 228 til 237 ° C (442 til 459 ° F) |
| Opløselighed i vand | 1,20x10+2 mg/ml (20 ° C) |
| |
| |
| (verificere) | |
Methylprednisolon (Depo-Medrol, Medrol, Solu-Medrol) er et syntetisk glukokortikoid , primært ordineret for dets antiinflammatoriske og immunsuppressive virkninger. Det bruges enten ved lave doser til kroniske sygdomme eller bruges samtidigt ved høje doser under akutte blusser. Methylprednisolon og dets derivater kan administreres oralt eller parenteralt.
Uanset indgivelsesvej integreres methylprednisolon systemisk som vist ved dets effektivitet for hurtigt at reducere inflammation under akutte blusser. Det er forbundet med mange bivirkninger, der kræver nedtrapning af stoffet, så snart sygdommen er under kontrol. Alvorlige bivirkninger omfatter iatrogen Cushings syndrom, hypertension, osteoporose, diabetes, infektion og hudatrofi.
Kemisk set er methylprednisolon et syntetisk pregnan steroidhormon afledt af hydrocortison og prednisolon . Det tilhører en klasse af syntetiske glukokortikoider og mere generelt kortikosteroider . Det fungerer som en mineralocorticoid og glucocorticoid receptoragonist. I sammenligning med andre eksogene glukokortikoider har methylprednisolon en højere affinitet til glucocorticoidreceptorer end til mineralocorticoidreceptorer.
Glukokortikoids navn blev afledt efter opdagelsen af deres involvering i regulering af kulhydratmetabolisme. De cellulære funktioner af glukokortikoider, såsom methylprednisolon, forstås nu at regulere homeostase, metabolisme, udvikling, kognition og inflammation. De spiller en afgørende rolle i tilpasning og reaktion på miljømæssig, fysisk og følelsesmæssig stress.
Methylprednisolon blev først syntetiseret og fremstillet af The Upjohn Company (nu Pfizer) og FDA godkendt i USA den 2. oktober 1957. I 2018 var det den 153. mest foreskrevne medicin i USA med mere end 4 millioner recepter. Methylprednisolon har været en ordineret behandling midt i COVID-19-pandemien , men der er ingen tegn på, at det hverken er sikkert eller effektivt til dette formål.
Farmakodynamik
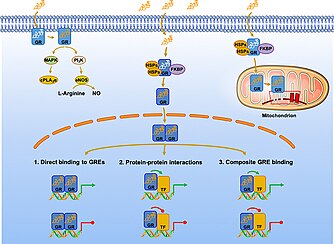
Methylprednisolon er et syntetisk glucocorticoid (GC), der udviser pleiotropiske virkninger på en række forskellige fysiologiske mekanismer. Imidlertid er de blevet ordineret grundigt for deres virkninger på betændelse og immunitet. Virkningerne af syntetiske glukokortikoider, såsom methylprednisolon, er afhængig af dets tilknytning til intracellulære glukokortikoidreceptorer (GR'er) og i mindre grad mineralocorticoidreceptorer (MR'er). GR'er er bredt fordelt i modsætning til MR'er, der viser en begrænset vævsfordeling. Ved denne mekanisme translokerer den ligandbundne receptor til kernen og modulerer genekspression.
Signaltransduktion
I fravær af endogene eller syntetiske GC'er er monomere GR'er placeret i cytoplasmaet og danner multiproteinkomplekser med varmechokproteiner (HSP'er), immunofiliner og andre chaperoner såsom src og p23. GR virker på en ligandafhængig måde, hvor komplekset holder GR i en inaktiv form med høj specificitet for liganden. Når methylprednisolon fra plasmaet eller interstitialvæsken diffunderer passivt hen over cellemembranen, binder det til GR, hvilket fremkalder en konformationsændring og GC-GR-dimerisering. Det blev tidligere antaget, at denne konformationsændring var nødvendig for at dissociere multiproteinkomplekset for at tillade den ligandbundne receptor at translokere til kernen. Nylige undersøgelser har imidlertid vist, at chaperoner spiller en rolle i atomimport. Det nu aktive methylprednisolon-GR-kompleks kan enten transducere ikke-genomiske ændringer i cytoplasmaet eller translokere til kernen og regulere transskriptionel aktivitet af målgener ved direkte, tethering eller sammensatte mekanismer.
Genomisk signalering
Genomiske mekanismer, uanset hvilken type, fremkalder reaktioner med en langsom begyndelse og en langsom spredning. Dette tilskrives varigheden af mRNA -transkription og translation. Glukokortikoider har evnen til at regulere omtrent 100 til 1000 gener med specificitet til celletype.
Tre hovedmekanismer har beskrevet, hvordan MP-GR-komplekset ændrer genekspression ved enten at binde til DNA eller transkriptionsmodulatorer. En mekanisme for genomisk signalering opstår, når MP-GR-komplekset direkte binder til DNA-sekvenser kaldet glucocorticoid responselementer (GRE'er). GRE'er er placeret i regulatoriske områder af målgener og formidler deres transaktivering eller transrepression. For eksempel forstyrrer aktiveringen af lipocortin 1 (ANAX1) negativt produktionen af prostaglandiner og leukotriener , kendte proinflammatoriske signaler. På samme måde er negative GRE'er (nGRE'er) ansvarlige for at undertrykke gener involveret i immuncelleaktivering.
Send transkriptionelle ændringer
Post-translationelle ændringer (PTM'er) bidrager også til methylprednisolonsignalering og kan producere genomiske og ikke-genomiske effekter. GR har indeholder flere steder for phosphorylering, sumoylering, ubiquitination og acetylering, der primært sker efter intracellulær methylprednisolonbinding til GR. PTM'er modulerer mange funktioner, herunder nuklear translokation, styrke og varighed af receptorsignalering og kofaktorinteraktion. Et specifikt eksempel er deacetylering med histondeacetylase 2 (HDACe) var nødvendig for transrepression af NF-KB.
Ikke-genomisk signalering
Mekanismerne for ikke-genomisk signalering adskiller sig fra genomisk signalering, men formidler alligevel lignende veje og giver terapeutisk relevans. Disse mekanismer er karakteriseret ved at have en hurtig begyndelse (mindre end 15 minutter), fordi de ikke er afhængige af tidskrævende transskription eller translation og ikke modificeres af transkriptionshæmmere.
Methylprednisoloninduceret ikke-genomisk signalering er klassificeret efter tre mekanismer: (1) cytoplasmatiske glukokortikoidreceptor (cGR) -medierede ikke-genomiske effekter, (2) membranbundne glukokortikoidreceptor (mGR) ikke-genomiske effekter og (3) fysiokemiske interaktioner med cellemembraner (ikke-specifikke ikke-genomiske effekter).
Proteiner, der dissocierer fra det aktiverede GC-cGR-kompleks, initierer intracellulære transkriptionsuafhængige mekanismer. Det er tegn på, at dissocieret SRC er ansvarlig for at hæmme frigivelsen af arachidonsyre (AA) fra cellemembranphospholipider. AA er påkrævet til syntese af inflammatoriske mediatorer (prostaglandiner og leukotriener) og dermed medierer AA -hæmning flere vigtige veje, såsom cellulær vækst, metabolisme og inflammation.
Tidligere undersøgelser identificerede mGR'er i lymfomceller, men det var først i 2004, at mGR'er blev identificeret i humane perifere mononukleære celler. Forekomsten af mGR'er varierer pr. Celletype med den højeste koncentration i B -lymfocytter på op til 12,3%, op til 9,2% i monocytter og fraværende fra T -lymfocytter. Undersøgelser har vist en positiv sammenhæng mellem de mGR-positive celler og sygdomsrelateret aktivitet. Der er ingen dokumenterede signalveje forbundet med mGR på nuværende tidspunkt. Nogle forskere antager, at høj sygdomsaktivitet aktiverer mGR -ekspression og ved administration af methylprednisolon skaber en negativ feedback -loop ved at inducere apoptose.
Høje koncentrationer af methylprednisoloninterkalat i plasma og mitokondrielle cellulære membraner. Denne forening ændrer membranens fysiokemiske egenskaber; aktivering af membranproteiner, ændring af cellulære funktioner og i sidste ende påvirkning af kationtransport gennem plasmamembranen og stimulering af protonlækagen hen over den indre mitokondriemembran. Hæmmet oxidativ fosforylering kompromitterer ATP -produktion, en vigtig energikilde til cellulær energimetabolisme og immunfunktion. In vivo-undersøgelser af Con-A-stimulerede thymocytter (hos rotter) og humane immunceller, der blev administreret høje doser methylprednisolon, har vist sig at hæmme respirationen på en dosisafhængig måde, hæmme plasmacalcium og natriumoptagelse og øge cytoplasmatisk calciumkoncentration. Den summative proces er som følger: Methylprednisolon interkalerer i plasmamembranen, forårsager fysiokemiske ændringer, aktiverer membranproteiner, der hæmmer plasmacalcium og natriumoptagelse (efterligner en energiunderskudstilstand). ATP -forbruget falder (ligner hæmmet respiration), hvilket resulterer i proteinpermeabilitet ved den indre mitokondriemembran og afkobling af oxidativ fosforylering. Af bemærkelsesværdig betydning blev DNA/RNA -syntese ikke hindret. Afhængigheden af husholdningsceller og immunceller til ATP resulterer i immunsuppression under ATP -underskud. Specifikke immunfunktioner, der udføres ved denne proces, er cytokinesis, migration, fagocytose, antigenbehandling og præsentation, antistofsyntese, cytotoksicitet og regulering.
HPA -aksen
Aktiveringen af hypothalamus-hypofyseaksen (HPA-aksen) stimulerer produktionen af endogene glukokortikoider i binyrebarken. HPA -aksen fortolker stimuli (stress, betændelse og døgnrytme) og transducerer en tilsvarende fysiokemisk reaktion. Glukokortikoider frigivet i blodet tjener som budbringer ved at binde til glukokortikoidreceptorer i en bred fordeling over kroppen, herunder selve HPA -aksen. Således overvåges det fysiologiske område af GC'er af den negative feedback -loop GC'er, der udøver på enhver del af HPA -aksen. Methylprednisolon efterligner strukturelt og funktionelt endogene corticoider og vil påvirke HPA -aksen på en lignende måde.
Farmakokinetik
Methylprednisolon er godkendt til oral og parenteral administration. Methylprednisolon (Medrol) til oral administration er tilgængelig i en tabletformulering i styrker på 2 mg, 4 mg, 8 mg, 16 mg eller 32 mg. Både methylprednisolonacetat (Depo-Medrol) og methylprednisolonsuccinat (Solu-Medrol) er godkendt til intramuskulær injektion. Depo-Medrol er desuden godkendt til intralesional, intraartikulær og blødt vævsinjektion. Depo-Medrol fås som steril vandig opløsning i styrker på 20 mg/ml, 40 mg/ml eller 80 mg/ml. Solu-Medrol er det eneste derivat af methylprednisolon, der er godkendt til intravenøs infusion, da det sterile pulver er opløseligt i vand og kan blandes med et fortyndingsmiddel. Styrker varierer fra 40 mg til 2 g.
Syntetiske glukokortikoider ligner endogene steroider i metabolismen, men adskiller sig i affinitet for glukokortikoid- og mineralokortikoidreceptorer, affinitet til proteinbinding, eliminationshastighed og metaboliske produkter.
Oral methylprednisolon absorberes let fra mave -tarmkanalen med en biotilgængelighed på 89,9%. I modsætning til endogene GC'er binder methylprednisolon ikke til glycoproteintranscortin (kortikosteroidbindende globulin, CBG), men har moderat proteinbinding til albumin. Farmakokinetikken for methylprednisolon er således lineær og viser ingen dosisafhængighed. Patienter, der udviser lave albuminkoncentrationer, risikerer at få bivirkninger under behandling med glukokortikoider. Oral methylprednisolon har en moderat fordeling i væv ved 1,38L/kg.
Methylprednisolon elimineres primært ved levermetabolisme og udskillelse af metabolitter via nyrerne; med renal udskillelse af uændret methylprednisolon på kun 1,3–9,2%. Methylprednisolon kan omdannes til methylprednison. Levermetabolisme medieres af 11 beta-hydroxysteroiddehydrogenaser (11 beta-HSD) og 20-ketosteroidreduktaser. Methylprednisolon gennemgår renal udskillelse af hydrofile inaktive metabolitter, herunder 20-carboxymelthylprednisolon og 6 [beta] -hydroxy-20 a-hydroxymethylprednisolon.
| Syntetisk glukokortikoid | Ækvivalent dosis (mg) | Antiinflammatorisk aktivitet 1 | Mineralocorticoid aktivitet 1 | Biologisk halveringstid (timer) | Referencer |
|---|---|---|---|---|---|
| Kort til mellemvirkende glukokortikoider | |||||
| Hydrocortison | 20 | 1 | 1 | 8-12 | |
| Kortison | 25 | 0,8 | 0,8 | 8-12 | |
| Prednison | 5 | 4 | 0,3 | 12-36 | |
| Prednisolon | 5 | 4 - 5 | 0,3 | 12-36 | |
| Methylprednisolon | 4 | 5 | 0,25-0,5 | 12-36 | |
| Meprednison | 4 | 5 | 0 | ||
| Mellemvirkende glukokortikoider | |||||
| Triamcinolon | 4 | 5 | 0 | 12-36 | |
| Paramethason | 2 | 10 | 0 | Ikke relevant | |
| Fluprednisolon | 1.5 | 15 | 0 | ||
| Langtidsvirkende glukokortikoider | |||||
| Betamethason | 0,6 | 25-40 | 0 | 36-72 | |
| Dexamethason | 0,75 | 30 | 0 | 36-72 | |
| Mineralokortikoider | |||||
| Fludrocortison | 2 | 10 | 250 | 18-36 | |
| Desoxycorticosteronacetat | 0 | 20 | |||
Medicinske anvendelser
Som tidligere nævnt er den primære anvendelse af methylprednisolon at undertrykke inflammatoriske og immunresponser. Methylprednisolon opnår dette primært ved at regulere antallet og funktionen af leukocytter, cytokiner og kemokiner. Dens udbredte inflammatoriske kontrol er befordrende ved brug på tværs af flere lidelser uanset patologi. Methylprednisolon ordineres sædvanligvis som kortvarig behandling for akutte blusser, som det ses ved akut gigtartig arthritis. Det kan ordineres under igangværende behandling i lavere doser, afhængigt af overvågning af bivirkninger. Doseringsstyrke og formulering er optimeret efter medicinsk brug.
Astma
I 2001-2002 fik 11,4% af patienterne diagnosticeret med astma og set ved et ambulant besøg orale kortikosteroider som en langsigtet kontrolbehandling. Det nationale astmauddannelses- og forebyggelsesprogram (NAEPP) angiver systemisk methylprednisolon i både kort- og langtidsbehandlinger for hurtigt at kontrollere og undertrykke vedvarende astma. Ved forværringer, der resulterer i et besøg på skadestuen (ED), foretrækkes oral methylprednisolon frem for intravenøs administration, medmindre der er problemer med vedhæftning eller opkastning. Oral methylprednisolon er mindre invasiv, og undersøgelser har vist, at tilsvarende virkning sammenlignet med intravenøs methylprednisolon. Dosis over 60-80 mg/dag eller 2 mg/kg/dag anbefales ikke, da det ikke har vist sig at ændre lungefunktion, indlæggelseshastighed eller opholdstid på hospitalet sammenlignet med lavere doser. Efter ED-udskrivning tilrådes det at ordinere et fem-dages kursus af methylprednisolon for at reducere sandsynligheden for tilbagefald eller abstinenssymptomer.
Reumatiske sygdomme
Methylprednisolon bruges til behandling af flere reumatiske sygdomme, såsom Systemic Lupus Erythematosus (SLE) og Reumatoid Arthritis (RA). Methylprednisolon dosering og administration for disse sygdomme er meget variabel på grund af varieret patofysiologi mellem sygdommene og hos patienter diagnosticeret med en given sygdom. I Lupus Nephritis, en almindelig manifestation af SLE, ordineres patienter ofte methylprednisolon samtidig med immunsuppressiva. Alvorlige manifestationer behandles ofte med Cyclophosphamid eller Rituximab og tre doser methylprednisolon IV-pulsbehandling (som anbefalet af ACR-retningslinjer) før skift til oral prednisolon og azathioprin til vedligeholdelse.
Intra-artikulære kortikosteroidinjektioner (IACI) er en andenlinie terapi til at lindre ledsmerter som følge af leddegigt. Det injiceres oftest i leddene i knæ og skuldre. Selvom injektionen er lokal, har undersøgelser vist systemisk absorption, hvilket fremgår af gavnlige virkninger på fjerne led. I et forsøg på at minimere HPA -undertrykkelse har FDA -retningslinjerne begrænset IACI'er til tre om året, med mindst 30 dage mellem injektionerne.
Primær eller sekundær adrenokortikal insufficiens
Methylprednisolon anbefales typisk ikke ved primær eller sekundær binyrebarkinsufficiens sammenlignet med andre kortikosteroider, der har en højere affinitet for mineralocorticoidreceptor- og saltbevarende egenskaber.
Mærkede angivelser
De mærkede indikationer nedenfor er kategoriseret efter indgivelsesvej og derefter efter medicinsk disciplin.
Oral methylprednisolon
- Allergi og immunologi: angioneurotisk ødem , astma , urticaria , sæsonbetonet eller flerårig allergisk rhinitis, lægemiddeloverfølsomhedsreaktioner og serumsygdom .
- Dermatologi: toksisk epidermal nekrolyse, atopisk dermatitis , kontaktdermatitis , pemphigus , erythema multiforme , Steven-Johnsons syndrom , bullous dermatitis herpetiformis, alvorlig seborrheisk dermatitis , eksfoliativ dermatitis, mycosis fungoides og alvorlig psoriasis .
- Endokrinologi: medfødt adrenal hyperplasi , hypercalcæmi forbundet med kræft , ikke -suppurativ thyroiditis og primær eller sekundær binyrebarkinsufficiens .
- Gastroenterologi: inflammatorisk tarmsygdom og ulcerøs colitis .
- Hæmatologi: erhvervet (autoimmun) hæmolytisk anæmi , idiopatisk trombocytopenisk purpura , sekundær trombocytopeni, erythroblastopeni, leukæmi , lymfom og medfødt (erythroid) hypoplastisk anæmi.
- Lunge: aspirationspneumonitis , kronisk berylliumsygdom , eosinofil lungebetændelse , symptomatisk sarkoidose og lungetuberkulose i forbindelse med antituberkulosekemoterapi.
- Nefrologi: nefrotisk syndrom , idiopatisk type eller sekundær til lupus nefritis .
- Neurologi: multipel sklerose .
- Oftalmologi: scleritis , retinal vaskulitis , uveitis , choroiditis, iritis, iridocyclitis, keratitis , optisk neuritis , allergisk konjunktivitis , allergiske hornhinde marginalsår, herpes zoster ophthalmicus , sympatisk oftalmi og chorioretinitis.
- Reumatologi: leddegigt , reumatisk karditis , akut gigtartritis , ankyloserende spondylitis , dermatomyositis og polymyositis , psoriasisartritis , systemisk lupus erythematosus , akut og subakut bursitis , synovitis af slidgigt, posttraumatisk artrose og epicondylitis .
- Diverse: trikinose med neurologisk eller myokardial involvering.
Parenteral methylprednisolon
- Intraartikulære eller bløde vævsinjektioner: akut gigtartig arthritis, akut og subakut bursitis, akut tenosynovitis, epicondylitis og synovitis af slidgigt.
- Intralesional injektioner: alopecia areata , discoid lupus erythematosus , keloider , granuloma annulare , lichen planus , lichen simplexronicus , psoriasisplakker, necrobiosis lipoidica diabeticorum .
- Intramuskulære injektioner er ordineret til behandling af mange af de samme tilstande, der er angivet til oral administration. Intramuskulære injektioner administreres som et alternativ til oral behandling.
Off-label indikationer
Nogle af de off-label-indikationer for methylprednisolon omfatter akut rygmarvsskade , akut respiratorisk nødsyndrom , alkoholisk hepatitis , hormonel genoplivning ved kadaverisk organgendannelse og kronisk obstruktiv lungesygdom .
Tilgængelige formularer
| Aktiv ingrediens | Mærke navn | ROA | Form | Styrke 1 | inaktive ingredienser |
|---|---|---|---|---|---|
| methylprednisolon | Medrol | Mundtlig | tablet | 2, 4, 8, 16, 32 mg | calciumstearat, majsstivelse, lactose, mineralolie, sorbinsyre, saccharose og erythrosinnatrium (kun 2 mg), FD&C gul nr. 6 (kun 8 og 32 mg) |
| methylprednisolon | Medrol | Mundtlig | tablet | 4 mg; 21 piller (dosispakke) | calciumstearat, majsstivelse, lactose, saccharose |
| methylprednisolonacetat | Depo-Medrol | Parenteral:
intraartikulært eller blødt væv, intralesional eller intramuskulært |
affjedring | 20, 40, 80 mg/ml | Polyethylenglycol 3350, Polysorbat 80, Monobasisk natriumphosphat, Dibasisk natriumphosphat USP, Benzylalkohol 2 tilsat som konserveringsmiddel |
| methylprednisolonacetat 3 | Depo-Medrol | Parenteral:
intraartikulært eller blødt væv, intralesional eller intramuskulært |
affjedring | 40 eller 80 mg/ml (enkeltdosis hætteglas) | Polyethylenglycol 3350
Myristyl-gamma-picoliniumchlorid |
| methylprednisolonsuccinat | Solu-Medrol | Parenteral:
intravenøs eller intramuskulær |
opløsning, rekonstitueret | 500, 1000, 2000 mg/hætteglas, 2000 mg med fortyndingsmiddel (flerdosis hætteglas) | monobasisk natriumphosphat vandfrit, dibasisk natriumphosphat tørret og lactose vandigt. Bakteriostatisk vand tilsat som fortyndingsmiddel med benzylalkohol 2 tilsat som konserveringsmiddel |
| methylprednisolonsuccinat 3 | Solu-Medrol | Parenteral:
intravenøs eller intramuskulær |
opløsning, rekonstitueret | 40, 125, 500, 1000 mg/hætteglas (enkeltdosis hætteglas) | monobasisk natriumphosphat vandfrit, dibasisk natriumphosphat tørret og lactose vandigt. |
Fodnoter:
1 Angiver forskellige styrker ved tilgængelige formularer. Er ikke tegn på hyppighed eller daglig kumulativ dosis; varierer efter patient og tilstand.
2 Benzylalkohol bør ikke bruges til nyfødte
3 Konserveringsfri formulering
Kontraindikationer
Methylprednisolon bør ikke tages oralt af mennesker, der har systemiske svampeinfektioner, med undtagelse af Depo-Medrol, når det administreres som en intraartikulær injektion til lokaliserede ledbetingelser. Methylprednisolon er kontraindiceret hos personer med kendt overfølsomhed over for methylprednisolon eller dets komponenter Steroider bør anvendes med forsigtighed til patienter med ulcerøs colitis, hjertesygdom eller hypertension, mavesår, nyreinsufficiens, osteoporose, myasthenia gravis, glaukom og diabetes. Psykiske manifestationer kan forekomme, mens du tager methylprednisolon, lige fra eufori, søvnløshed, personlighedsændringer til depression. Forsigtighed er nødvendig for patienter med disponerede psykoser, da psykotiske tendenser kan forværres, mens de tager kortikosteroider.
Solu-Medrol 40 mg dosering indeholder lactosemonohydrat fremstillet af komælk; Det bør ikke tages af nogen med kendt overfølsomhed over for mejeriprodukter eller dets komponenter. Alvorlige medicinske hændelser har været forbundet med epidural administration af Solu-Medrol og Depo-Medrol, herunder rygmarvsinfarkt, paraplegi, quadriplegia, kortikal blindhed og slagtilfælde. Intramuskulære injektioner bør ikke administreres til personer med idiopatisk trombocytopenisk purpura. Formuleringer af Solu-Medrol og Depo-Medrol, der indeholder benzylalkohol, er kontraindiceret til brug hos for tidligt fødte børn. Eksponering af neuralt væv for store mængder benzylalkohol har været forbundet med toksicitet og i sjældne tilfælde medført død.
Bivirkninger
Bivirkninger kan overskygge de terapeutiske virkninger af methylprednisolon.
Centralnervesystemet
Der er minimale kliniske diagnostiske kriterier til at definere de psykiske bivirkninger (PAE) forbundet med methylprednisolonbrug hos patienter med systemisk lupus erythematosus (SLE). Forekomsten varierer fra 1,3 til 62% af voksne behandlede patienter. Typen og sværhedsgraden af neuropsykiatriske symptomer varierer også betydeligt mellem patienterne, hvor 33% af patienterne rapporterede mild til moderat PAE og 5-10% rapporterede alvorlig PAE. Methylprednisolondosis og varighed har været impliceret i PAE -udviklingen. 20 mg/dag prednison (16 mg/dag methylprednisolon) er tærskeldoseringen for PAE -udvikling, der er aftalt i mange undersøgelser. Kortsigtet puls IV-behandling ved høje doser er forbundet med hurtig indtræden med maniske og hypomaniske symptomer, hvor så langvarig terapi giver anledning til depressive symptomer (selvmordsforsøg sjældent). PAE er reversible med behandlingsreduktion eller seponering.
Metabolisk og endokrin
Iatrogen Cushings syndrom er en direkte komplikation af glukokortikoidbehandling og den mest almindelige årsag til eksogent Cushings syndrom. Kliniske træk ved Cushings syndrom omfatter mange bivirkninger ved behandling med glukokortikoider. Traditionelle symptomer omfatter vægtøgning, myopati, osteoporose, øget risiko for infektion, hypertension og psykologisk effekt. Fedtdeponering er centraliseret på bagagerummet, mellem skuldrene ("bøffelpukkel") og i ansigtet ("månens ansigt"). Patientundervisning og udbyderovervågning er det første trin i genkendelse og diagnosticering af Iatrogenic Cushings syndrom. Eksogene glukokortikoider undertrykker produktion af adrenokortikotropisk hormon (ATCH), som kan verificeres ved AM biokemisk analyse. Begyndelsen af bivirkninger varierer; neuropsykiatriske symptomer kan opstå inden for få timer, mens osteoporose ville tage måneder at udvikle.
De metaboliske virkninger af at tage methylprednisolon involverer den kontinuerlige nedbrydning af proteiner til glukoneogenese øger nødvendigheden af insulin. Dette resulterer i hyperlipidæmi, vægtøgning, myopati, der kan få en patient til at gribe behandlingen.
Infektioner
Afsnittet Immundefekt angiver kendte patogener, der er bekymrende ved glukokortikoidinduceret immundefekt.
Muskuloskeletale
Osteoporose er en knoglesygdom karakteriseret ved et tab af knogletæthed, masse og arkitektur, der efterlader en patient modtagelig for brud. Verdenssundhedsorganisationen (WHO) definerer osteoporose hos kaukasiske postmenopausale kvinder som en knoglemineraltæthed (BMD) og en T -score på -2,5 eller mindre. Udbredelsen af osteoporose hos patienter med SLE varierer geografisk, og nogle tilskriver det BMD og T-score diagnostisk egnethed. Britiske 10,3%, kinesiske 21,7%The Canadian Clinical Practice Guidelines og The American College of Rheumatology har skiftet til at bruge en Z-score som en diagnostisk markør for osteoporose, men det er ikke lykkedes at finde en klinisk diagnostisk tærskel. Derudover viste en britisk undersøgelse, at BMD kan underrepræsentere en patient med SLE, da deres risiko for brud er 22% højere end den raske person.
Eksogene kortikosteroider fremkalder osteoporose ved at øge knogleresorption og reducere knogledannelse. Knogletab kan udtales inden for de første par måneder efter initiering af methylprednisolon med et konstant fald ved kronisk brug. Trabekulært knogletab i lænden går forud for kortikal knogletab i lårhalsen.
Udtømmende liste
Allergisk: allergiske eller overfølsomhedsreaktioner, anafylaktoid reaktion, anafylaksi og urticaria.
Kardiovaskulær: hypertension, kongestiv hjertesvigt hos modtagelige patienter, for tidlig aterosklerotisk sygdom, arytmier og mulig hyperlipidæmi.
Dermatologisk: nedsat sårheling, petechiae og ecchymoses, udtynding af huden, ansigts erytem og øget svedtendens.
Endokrine: Cushingoid -træk, vækstundertrykkelse hos børn, sekundær adrenokortikal og hypofysereaktion, menstruale uregelmæssigheder, nedsat kulhydratintolerance og latent diabetes mellitus. Hos patienter med diabetes øges behovet for insulin eller orale hypoglykæmiske midler.
Væske- og elektrolytforstyrrelser: natriumretention, væskeretention, kaliumtab, hypokalæmisk alkalose eller kongestiv hjertesvigt hos modtagelige patienter.
Mave -tarmkanalen: mavesår, pancreatitis, abdominal distension og ulcerøs esophagitis.
Metabolsk: proteinkatabolisme, der forårsager negativ nitrogenbalance.
Muskuloskeletale: muskelsvaghed, tab af muskelmasse, steroidmyopati, osteoporose, seneruptur (især akilles), frakturer i hvirvelkomprimering, aseptisk nekrose af lår- og lårhoveder og patologisk brud på lange knogler.
Neurologisk: øget intrakranielt tryk med papilledem, kramper, svimmelhed og hovedpine.
Oftalmisk: posterior sub-kapsel grå stær, øget intraokulært tryk, glaukom og exophthalmos.
Tilbagetrækning
Feedback af de eksogene glukokortikoider ved hypothalamus-hypofyse-adrenal (HPA) akse hæmmer udskillelsen af det corticotropinfrigivende hormon (CRH) og det adrenokortikotropiske hormon (ATCH) i henholdsvis hypothalamus og hypofysen. Langvarig undertrykkelse fører til utilstrækkelige reaktioner på fysiske og følelsesmæssige belastninger, såsom sygdom og traumer. Undertrykkelse af ATCH kan resultere i binyrehypoplasi eller sekundær binyreatrofi inden for 6 uger efter methylprednisolonbehandling, hvilket efterlader en patient i fare for at udvikle livstruende binyreinsufficiens-krise. Faktorer, der bidrager til omfanget af HPA -akse -undertrykkelse, omfatter steroidhormonstyrke (type forbindelse og indgivelsesvej), kumulativ dosis, behandlingsvarighed og samtidig medicinbrug. Enhver person, der har taget steroidhormoner i 2+ uger, risikerer at udvikle HPA -akseundertrykkelse. t Systemisk risiko for methylprednisolon er blevet markeret som moderat inden for klassen af syntetiske glukokortikoider.
Rådfør dig med din læge, inden du afbryder methylprednisolon af en eller anden grund. Pludselig ophør af lægemidlet forårsager almindeligvis forbigående uspecifikke symptomer såsom appetitløshed, mavebesvær, opkastning, døsighed, forvirring, hovedpine, feber, led- og muskelsmerter, skrællende hud og vægttab. Disse symptomer kan tilskrives steroidabstinenssyndrom, binyreinsufficiens eller tilbagefald af sygdomme. Dem, der har taget methylprednisolon som en langvarig behandling, kan gradvist tilspidses for at minimere abstinenssymptomer og risiko for tilbagefald. Hvis symptomerne forværres, har midlertidigt stigende methylprednisolondosering vist klinisk relevans. Undersøgelser, der testede patienter ved tilbagetrækning af methylprednisolon, viste vedvarende binyreinsufficiens, hvor en undersøgelse viste 15% efter 3 år. Der var imidlertid en lang række prævalenser og mangel på ensartethed i opfølgningstidslinjen.
Lægemiddelinteraktioner
Der udvises forsigtighed, når man tager methylprednisolon samtidigt med medicinen beskrevet nedenfor.
Enzyminducerende midler
Alle lægemidler, der falder inden for klassen af enzyminduktorer, øger clearance og reducerer halveringstiden for methylprednisolon ved samtidig administration. Phenobarbital , phenytoin , rifampin , carbamazepin og barbiturater øger leverenzymer og elimineringshastighed og reducerer dermed den immunosuppressive virkning af methylprednisolon. Øgede doser kan være nødvendige for at opnå den ønskede effekt af methylprednisolon.
Cytochrome P450 (CYP) 3A4 -hæmmere
Troleandomycin , ketoconazol og Clarithromycin hæmmer metabolisme; og kan reducere eliminationshastigheden og øge halveringstiden for methylprednisolon. Doseringerne bør reduceres tilsvarende for at undgå bivirkninger. En anden CYP 3A4-hæmmer, grapefrugtjuice, forlænger halveringstiden for oral methylprednisolon.
Orale præventionsmidler
Orale præventionsmidler hæmmer oxidative processer, hvilket fremhæves af dets evne til at reducere methylprednisolon -clearance.
P-glycoprotein-hæmmere
Methylprednisolon er vist at være et substrat for P-glycoprotein; dets hæmning menes at øge absorptionen og distributionen af methylprednison. Ingen klinisk relevans er blevet knyttet.
Ciclosporin, tacrolimus, sirolimus (Rapamycin)
Methylprednisolon og cyclosporin hæmmer stofskiftet og øger derfor sandsynligheden for at opleve bivirkninger forbundet med et af de enkelte lægemidler. Ud over kendte individuelle bivirkninger er der blevet rapporteret kramper.
Cox1 -hæmmere
Methylprednisolon kan øge eliminationshastigheden med kronisk højdosis aspirin . Patientens er modtagelige for øgede salicylatserumniveauer eller salicylattoksicitet ved ophør af methylprednisolon. Der bør udvises stor forsigtighed ved ordination af methylprednisolon og aspirin til patienter med hypoprothrombinæmi .
Antikoagulantia
Antikoagulantia udviser variable interaktioner; overvågning af koagulationsindeks anbefales for at opnå den ønskede effekt.

Fysiske egenskaber
Oral methylprednisolon (Medrol) og dets derivater er et hvidt, lugtfrit krystallinsk pulver. Dens opløselighed spænder fra praktisk talt uopløseligt i vand, meget let opløseligt i ether, let opløseligt i acetone og chloroform til svagt opløseligt i alkohol, dioxan og methanol. Methylprednisolonacetatsuspension (Depo-Medrol) er et 6-methylderivat af prednisolon, der smelter ved 215 grader Celsius med en vis nedbrydning. Methylprednisolon natriumsuccinat (Solu-Medrol) er natriumsuccinatesteren af methylprednisolon. I modsætning til opløselighederne ovenfor er methylprednisolonnatriumsuccinat opløseligt i vand og alkohol, let opløseligt i acetone og uopløseligt i chloroform
Kemiske egenskaber
Methylprednisolon, eller 6α-methylprednisolon, også kendt som 11β, 17,21-trihydroxy-6α-methylpregna-1,4-dien-3,20-dion, er en syntetisk pregnan steroid og et derivat af hydrocortison (11β, 17α, 21 -trihydroxypregn-4-en-3,20-dion) og prednisolon (11β, 17α, 21-trihydroxypregn-1,4-dien-3,20-dion). Der findes en række methylprednisolonestere med forskellige egenskaber og er blevet markedsført til medicinsk brug. De inkluderer methylprednisolonaceponat (Advantan), methylprednisolonacetat (Depo-Medrol), methylprednisolonsuccinat (Solu-Medrol) og methylprednisolonsuleptanat (Medrosol, Promedrol).
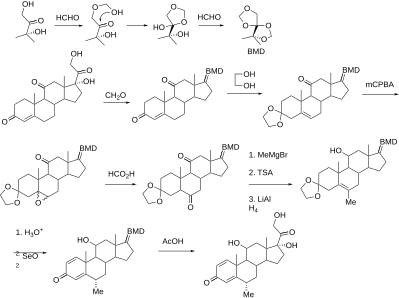
Syntese
Syntetiske steroider syntetiseres ud fra cholsyre og sapogeniner opnået fra henholdsvis kvæg og planter.
Historie, samfund og kultur
Methylprednisolon blev først syntetiseret og fremstillet af The Upjohn Company (nu Pfizer) og Food and Drug Administration (FDA) godkendt i USA den 2. oktober 1957. Patentet er siden udløbet, og generika er nu tilgængelige. I 2021 er den rangeret som den 153. mest foreskrevne medicin i USA med mere end fire millioner recepter. Det er sprunget fire pladser på ranglisten fra 2017. Methylprednisolon har været en ordineret terapi midt i COVID-19-pandemien , men der er ingen tegn på, at det hverken er sikkert eller effektivt til dette formål.
Referencer
eksterne links
- "Methylprednisolon" . Lægemiddeloplysningsportal . US National Library of Medicine.